Глазные капли с новокаином — можно ли капать в глаза
Профессия сварщика опасна: если нарушить технику безопасности, можно обжечь роговицу глаза. Существует недуг “Электроофтальмия”: он развивается в том случае, если глаз травмируется лучами сварочного аппарата. Главный признак электроофтальмии – боль в глазах. Человек также ощущает жжение в веках, у некоторых сварщиков возникает слезотечение. Ожог от сварки требует скорейшего лечения: следует обратиться к офтальмологу. Врач назначит капли, которые уменьшат болевой синдром и избавят от других симптомов недуга.
Область применения
Работа сварщика
Капли для глаз после сварки отличаются по составу и эффекту. Препарат подбирается индивидуально. Если ожог роговицы относительно легкий (1 – 2 степени), врач назначает капли и специальные гели. Ожог глаз 4-й степени наиболее опасный: в данном случае может потребоваться операция.
Если диагностирована электроофтальмия 1-й степени, офтальмолог назначает капли, которые снимают покраснение.
Третья степень электроофтальмии приводит к нарушению прозрачности роговицы. Капли нужны для устранения гиперемии, тянущих болей. Несвоевременное лечение приводит к утрате зрения.Препараты для глаз после сварки необходимы, но лишь в том случае, если имеются симптомы электроофтальмии. При развитии этой болезни можно чувствовать, будто в веке находится песчинка. Четвертая степень электроофтальмии – самая опасная. Прогрессирует некроз тканей, конъюнктивальная оболочка отторгается. Нужно немедленно обращаться к врачу, в противном случае, патологический процесс не остановится! Бывают случаи, когда электроофтальмия приводит к утрате зрения.
Читайте также инструкцию по применению Ципрофлоксацина каплей тут.
Недуг лечится комплексно. Капли, предназначенные для терапии ожогов, имеют в составе разные компоненты. При подборе лекарства врач учитывает степень болезни; принимаются во внимание особенности организма, противопоказания для конкретного пациента.
Особенности препаратов
Капли для глаз после сварки рекомендует офтальмолог. Самолечение недопустимо! Отдельно выпускаются средства, предназначенные для снятие отеков, отдельно – противовоспалительные составы, предотвращающие жжение и покраснение. Дозировка тоже назначается врачом.
Антигистаминные капли для глаз от аллергии, список находится в материале.
Если электроофтальмия сопровождается сильными болями, пациент использует средства с мощным обезболивающим эффектом. Они способны блокировать восприятие боли рецепторами глазного яблока: инстиллируют 2 раза в день. Другие лекарства оказывают мощный антибактериальный эффект, также устраняют боли, обеспечивает профилактику инфицирования.
Противовоспалительные средства восстанавливают слизистую роговицы, используются для профилактики осложнений электроофтальмии.
Список
- Средство “Эмокси-оптик” устраняет боли, вызванные электроофтальмией. Капли такого типа оказывают выраженный антибактериальный, антигипоксический, антиоксидантный эффект; назначаются при электроофтальмии 1-й и 2-й степени. Препарат используется и в том случае, если роговица воспалилась от контактных линз. По инструкции, глазные капли Эмокси-оптик назначают при кровоизлияниях в склеру. Он эффективен при осложнениях близорукости. Лекарство улучшает метаболизм в тканях глаза, оказывает регенерирующее воздействие.
- Лекарство “Ципролет” очень востребовано. Его назначают при ожоге глаз. Ципролет оказывает антибактериальное воздействие; действующим веществом является Ципрофлоксацин. Препарат может быть использован для лечения инфекционных болезней, связанных глазами. Он назначается при блефарите, кератите, хроническом конъюнктивите, язве роговицы.
 Ципролет восстанавливает ткани глаза при ожогах. Лекарство назначается и в том случае, если в глаз попадает инородное тело.
Ципролет восстанавливает ткани глаза при ожогах. Лекарство назначается и в том случае, если в глаз попадает инородное тело. - Средство “Тобропт” оказывает антибактериальный эффект и часто назначается при ожогах роговицы. Тобропт – это антибиотик, фармакологическая группа “Аминогликозиды”. Лекарство назначают в случае, если ожог сопровождается инфицированием. Согласно инструкции глазные капли Тобропт может быть назначен перед операцией на глазах или в восстановительный период. Грамотный прием препарат позволит избежать послеоперационных осложнений.
- Капли “Офтан дексаметазон” используется для лечения воспалительных и аллергических болезней. Лекарство отпускается по рецепту. Если не соблюдать дозировку, оно приводит к вирусным и грибковым осложнениям.
- Востребованным средством является Окомистин. Препарат обладает антисептическим эффектом, используется при ожогах роговицы (входят в состав комплексного лечения). Глазные капли Окомистин рекомендуют при ожогах роговицы, остром и хроническом конъюнктивите.
 Лекарство обеспечивает профилактику гнойных осложнений, используется при травмировании глаз.
Лекарство обеспечивает профилактику гнойных осложнений, используется при травмировании глаз. - “Наклоф” – препарат швейцарского производителя, обладает выраженным обезболивающим эффектом. Наклоф используется при ожогах роговицы. Также врач рекомендует его в послеоперационной период; цель применения – устранить болевой синдром.
- Для лечения электроофтальмии используется новокаин. В сравнении с другими лекарствами, он не оказывает столь мощный эффект. Цель применения новокаиновых капель – устранить боли в глазах. Лекарство может входить в состав комплексного лечения и использоваться наряду с другими каплями. Перед применением новокаина нужно получить консультацию у врача (он же назначит дозировку). Преимущество лекарства в том, что оно быстро снимает боли, тем самым облегчает общее самочувствие. Важно сказать, что новокаин востребован в медицине: он используется для лечения разных болезней.
Офтан дексаметазон глазные капли, информация здесь.
Капли для глаз Офтальмоферон
Капли для глаз Окуметил описаны в этой статье.
Капли для глаз Окапин https://eyesdocs.ru/medicinaoperacii/lekarstva/kapli-okapin-vitaminnyj-tonik-dlya-glaz.html
Рекомендации по применению
Применяйте капли для глаз в соответствии с рекомендациями врача. Каждое средство выпускается в индивидуальной упаковке: это может быть мини-капельница, стеклянный флакончик объемом 10-20 мл. Мини-капельницы удобны: чтобы их использовать, не нужно покупать пипетку.
Также читайте про Окомистин по ссылке.
При инстилировании надо следить за тем, что кончик мини-капельницы (или пипетки) не соприкасался с глазом. Если неосторожно проводить процедуру, можно травмировать роговицу. Передозировка приводит к побочным эффектам. Что касается новокаина, лучше использовать меньшее количество средства, нежели большее. Как правило, офтальмолог рекомендует по 2 капли новокаиновых капель в каждый глаз.
Если желаете, замените пипетку на шприц без иглы.
Видео
Выводы
Любое офтальмологические болезни опасны осложнениями (самое опасное – слепота). Терапия на ранних стадиях дает хорошие результаты: человек может полностью восстановить зрение. Для лечения тяжелых ожогов может потребоваться операция. В основном глазные капли содержат мощные вещества. Перед использованием данных средств лечения нужно консультироваться с врачом.
Также читайте в статье про то, какие капли для глаз от конъюнктивита лучше использовать.
НОВОКАИН 0,5% 100 МЛ.
 Ветеринарная аптека HorseVet. ОПИСАНИЕ
Ветеринарная аптека HorseVet. ОПИСАНИЕНовокаин 0,5% раствор для инъекций относится к группе местноанестезирующих препаратов.
СОСТАВ
Новокаин 0,5% раствор для инъекций в качестве действующего вещества в 100 мл содержит 0,5 г прокаина гидрохлорида, а в качестве вспомогательного вещества воду для инъекций до 100 мл.
Новокаин блокирует натриевые каналы, вытесняет кальций из рецепторов, расположенных на внутренней поверхности мембраны и, таким образом, препятствует генерации импульсов в окончаниях чувствительных нервов и проведению импульсов по нервным волокнам. Подавляет проведение не только болевых, но и импульсов другой модальности. При внутривенном введении оказывает общее действие на организм животных, уменьшает образование ацетилхолина и понижает возбудимость периферических холинреактивных систем, оказывает блокирующее влияние на вегетативные ганглии, уменьшает спазмы гладкой мускулатуры, понижает возбудимость мышцы сердца и возбудимость моторных зон коры головного мозга.
 В токсических дозах вызывает возбуждение, затем паралич центральной нервной системы. В организме быстро гидролизуется, образуя парааминобензойную кислоту и диэтиламиноэтанол, которые являются фармакологически активными веществами. После введения лекарственный препарат действует быстро и кратковременно.
В токсических дозах вызывает возбуждение, затем паралич центральной нервной системы. В организме быстро гидролизуется, образуя парааминобензойную кислоту и диэтиламиноэтанол, которые являются фармакологически активными веществами. После введения лекарственный препарат действует быстро и кратковременно.ПРИМЕНЕНИЕ
Новокаин 0,5% раствор для инъекций применяют, при необходимости предварительно разбавив стерильным изотоническим раствором натрия хлорида 0,9% или раствором Рингера-Локка до нужной концентрации. Необходимые разведения готовят непосредственно перед применением.
Для инфильтрационной анестезии препарат применяют в виде 0,25% — 0,5% раствора
Для анестезии по методу А.В. Вишневского (тугая ползучая инфильтрация) — 0,125% — 0,25% раствора
Для проводниковой анестезии — 1% — 2% раствора
В офтальмологии 0,5% раствор новокаина применяют при кератите, кератоконъюнктивите, периодическом воспалении глаз у лошадей (подглазничная блокада)
В акушерско-гинекологической практике растворы новокаина назначают при эндометритах, метритах, выпадении матки и влагалища, задержании последа у коров и коз (паранефральная блокада по А.

При серозно-катаральных маститах (блокада нервов вымени по Б.А. Башкирову или Д.Д. Логвинову) в виде 0,25% — 0,5% раствора.
Новокаин 0,5% раствор для инъекций применяют также в качестве растворителя для лекарственных препаратов.
Растворы новокаина применяют подкожно, внутримышечно. Концентрация раствора, доза, способ применения зависят от характера оперативного вмешательства или течения болезни, вида, массы, возраста животного и его состояния.
Максимальные дозы новокаина в мл на одно животное:
Вид животного 0,5% раствора
Лошади 500
Крупный рогатый скот 400
Мелкий рогатый скот 150
Свиньи 150
Собаки 100
Повторное введение растворов новокаина производят по показаниям.
ПОБОЧНЫЕ ЯВЛЕНИЯ
Продукция животного происхождения, полученная от животных после применения Новокаина 0,5% раствора для инъекций может быть использована без ограничений.

ПЕРЕДОЗИРОВКА
В рекомендуемых дозах не вызывает у животных побочного действия и осложнений. Применение Новокаина 0,5% раствора для инъекций не исключает использования других лекарственных препаратов. Препарат применяют, как правило, однократно.
ОСОБЫЕ УКАЗАНИЯ
Запрещается одновременное применение с сульфаниламидами.
Запрещается применение Новокаина 0,5% раствора для инъекций по истечении срока годности.
ХРАНЕНИЕ
Препарат следует хранить в сухом, темном, недоступном для детей месте при температуре от 0°С до 25°С. Срок годности – 3 года.
ФАСОВКА
Новокаин 0,5% раствор для инъекций выпускают расфасованным по 100 мл в стеклянных флаконах соответствующей вместимости, укупоренных резиновыми пробками, укреплёнными алюминиевыми.
Производитель : Россия
Анестезиология в отделении анестезиологии, реанимации и интенсивной терапии, стационар ЕМС в Москве
В ЕМС работает опытная команда анестезиологов. Весь процесс подготовки пациента к операции организован таким образом, чтобы минимизировать риск осложнений. Обязательной является консультация анестезиолога за несколько дней до операции. Пациент рассказывает об имеющихся изменениях здоровья, сопутствующих заболеваниях, аллергических реакциях, перенесенных ранее операциях. Анестезиолог оценивает результаты анализов, дополнительных методов исследования, обсуждает с пациентом планируемый вид анестезии, при необходимости назначает консультации специалистов, например, кардиолога при сложных проблемах с сердечно-сосудистой системой. С анестезиологом обязательно нужно обсудить принимаемые лекарства, некоторые из них необходимо отменить перед операцией. Утром в день операции анестезиолог обязательно еще раз встретится с пациентом, узнает самочувствие, настроение, ответит на возникшие вопросы. Анестезиолог внимательно сопровождает пациента в течение всего периода от подачи в операционную до перевода в стационар после операции.
Обязательной является консультация анестезиолога за несколько дней до операции. Пациент рассказывает об имеющихся изменениях здоровья, сопутствующих заболеваниях, аллергических реакциях, перенесенных ранее операциях. Анестезиолог оценивает результаты анализов, дополнительных методов исследования, обсуждает с пациентом планируемый вид анестезии, при необходимости назначает консультации специалистов, например, кардиолога при сложных проблемах с сердечно-сосудистой системой. С анестезиологом обязательно нужно обсудить принимаемые лекарства, некоторые из них необходимо отменить перед операцией. Утром в день операции анестезиолог обязательно еще раз встретится с пациентом, узнает самочувствие, настроение, ответит на возникшие вопросы. Анестезиолог внимательно сопровождает пациента в течение всего периода от подачи в операционную до перевода в стационар после операции.
В операционной медсестра-анестезистка подключает к пациенту монитор, который в заданном режиме в течение всей операции контролирует артериальное давление, электрокардиограмму, пульс, содержание кислорода в организме, частоту и объем дыхания пациента. При необходимости может контролироваться глубина сна пациента и степень мышечного расслабления. Врач-анестезиолог оценивает все жизненно важные параметры пациента, следит, чтобы пациенту не было больно, рассчитывает дозу и кратность введения различных лекарств.
При необходимости может контролироваться глубина сна пациента и степень мышечного расслабления. Врач-анестезиолог оценивает все жизненно важные параметры пациента, следит, чтобы пациенту не было больно, рассчитывает дозу и кратность введения различных лекарств.
Анестезия (наркоз или обезболивание) – это временная утрата чувствительности, в том числе и болевой, под действием различных медикаментов. Анестезия — важная составляющая оперативного вмешательства, во время операции она обеспечивает полное отсутствие ощущения боли. Анестезия проводится с высочайшей степенью ответственности.
Методы анестезии
Общая анестезия
Во время наркоза сон пациента поддерживается постоянным точно дозированным введением снотворных препаратов внутривенно (через установленный перед операцией пластиковый внутривенный катетер) или ингаляционно (вдыханием через маску). Отсутствие боли обеспечивают анальгетики, которые также вводятся в течение всей операции.
Дыхание пациента во время общей анестезии может быть самостоятельным, но чаще всего поддерживается с помощью дыхательных аппаратов, «подстраивающихся» под ритм и глубину дыхания человека. Во время коротких и несложных операций анестезиолог использует ларингеальную маску, через которую пациент дышит смесью кислорода, воздуха и анестетических газов. При более длительных операциях, требующих полного мышечного расслабления, где применяются мышечные релаксанты, проводится эндотрахеальный наркоз. Под медикаментозным сном пациенту в дыхательные пути вводится термопластическая трубка со специальной манжетой, которая полностью защищает легкие и позволяет проводить искусственную вентиляцию.
У пациентов с сопутствующими заболеваниями сердечно-сосудистой системы во время анестезии вводятся необходимые лекарства, поддерживающие работу сердца или нормализующие артериальное давление. У пациентов с сахарным диабетом контролируется уровень сахара в крови. При необходимости во время операции за короткое время может быть лабораторно исследован любой параметр.
Регионарная анестезия
Позволяет обезболивать отдельные зоны тела. Наиболее известны спинальная и эпидуральная анестезии, когда небольшим количеством местного анестетика блокируется проведение болевых и двигательных нервных импульсов нижней части тела. Под этим видом анестезии выполняется большинство операций на нижних конечностях. Для пациентов старших возрастных групп эта анестезия является альтернативным методом при протезировании коленных и тазобедренных суставов.
Регионарная анестезия применяется также при операциях на верхних конечностях. С помощью специального прибора точно определяется расположение нервного сплетения (в области шеи, подмышечной области или отдельных нервов на предплечье и кисти) и вводится местный анестетик. Через 20-30 минут рука теряет чувствительность и способность двигаться.
Блокада нервов длится 2-3 часа, затем постепенно восстанавливаются все обычные ощущения. Во время действия регионарной анестезии может поддерживаться легкий медикаментозный сон, исключающий «присутствие» пациента на операции. Этот вопрос обязательно обсуждается на консультации с анестезиологом перед операцией. По желанию пациента снотворные препараты не будут вводиться, и он сможет наблюдать за ходом операции на мониторе, не испытывая при этом никаких неприятных ощущений.
Этот вопрос обязательно обсуждается на консультации с анестезиологом перед операцией. По желанию пациента снотворные препараты не будут вводиться, и он сможет наблюдать за ходом операции на мониторе, не испытывая при этом никаких неприятных ощущений.
Регионарная анестезия также применяется для обезболивания в послеоперационном периоде, наиболее часто при операциях в области колена, голени, стопы, обеспечивая отсутствие боли на 8-12 часов.
Местная анестезия
В настоящее время применяется только при небольших операциях на поверхности тела. Разновидность местной анестезии – аппликационная, когда мазь с анестетиком наносится на кожу, и через 30-40 минут появляется возможность безболезненно производить пункцию вен для забора анализов крови.
Риски анестезии
Анестезия – безопасная манипуляция, но как и все медицинские процедуры имеет определенные риски. Осложнения, опасные для жизни (остановка сердца, дыхания, тяжелые аллергические реакции), наблюдаются крайне редко.
Однако риск при проведении анестезии считается повышенным, если:
-
У пациента есть какое-либо хроническое заболевание (гипертоническая болезнь, ишемическая болезнь сердца, астма, сахарный диабет и т.д.). Если эти заболевания хорошо компенсированы, риск повышается незначительно.
-
У пациента есть аллергия на какие-либо лекарственные препараты
-
Пациент курит, употребляет алкоголь и наркотики
-
Пациент невнимательно отнесся к рекомендациям по подготовке к операции и анестезии, например, не выдержал нужный временной интервал по ограничению в приеме пищи, либо не согласовал с анестезиологом прием своих лекарств.
Опасности при проведении общей анестезии
Во время общей анестезии защитные рефлексы угнетаются, поэтому существует опасность попадания желудочного содержимого в дыхательные пути, что может быть опасно для жизни. В связи с этим в течение 6 часов до начала операции нельзя употреблять пищу, а за 4 часа до операции не рекомендуется пить воду, жевать жевательную резинку, курить. Если пациент не следовал данному правилу, то в целях его безопасности операция откладывается или отменяется.
В связи с этим в течение 6 часов до начала операции нельзя употреблять пищу, а за 4 часа до операции не рекомендуется пить воду, жевать жевательную резинку, курить. Если пациент не следовал данному правилу, то в целях его безопасности операция откладывается или отменяется.
Важно сообщить анестезиологу о шатающихся зубах или съемных зубных протезах, так как во время эндотрахеального наркоза при постановке интубационной трубки есть возможность повреждения зубов или голосовых связок.
В редких случаях в раннем послеоперационном периоде может наблюдаться тошнота и рвота, что связано с индивидуальной реакцией на препараты для анестезии.
Во время наркоза снижен тонус мышц, поэтому при длительных операциях возможны так называемые позиционные сдавления нервов, что может привести к длящемуся до нескольких недель снижению чувствительности в какой-либо части тела.
Опасности при проведении регионарной анестезии
При снижении артериального давления, появлении головокружения, тошноты, затрудненного дыхания при проведении спинальной или эпидуральной анестезии сразу же сообщите об этом анестезиологу или медсестре. Специалисты примут необходимые меры для улучшения вашего состояния.
Специалисты примут необходимые меры для улучшения вашего состояния.
После операции, проведенной под спинальной или эпидуральной анестезией, в течение нескольких часов сохраняется снижение чувствительности в нижних конечностях. Также может быть затруднено опорожнение мочевого пузыря, при необходимости в мочевой пузырь вводят катетер.
После спинальной анестезии может возникнуть головная боль. Это редкое осложнение может потребовать нескольких дней постельного режима и приема обезболивающих препаратов.
Беседа с анестезиологом
Проведению анестезии всегда предшествует беседа с анестезиологом. Если у Вас есть вопросы, обязательно задайте их во время этой беседы! Вам выдадут анкету, где необходимо точно и подробно отметить все данные о состоянии Вашего здоровья, ранее перенесенных и имеющихся заболеваниях и применяемых в настоящее время лекарственных препаратах. Также необходима информация о ранее перенесенных операциях, возможной аллергии на лекарственные препараты и Ваших привычках (занятиях спортом, курении, употреблении алкоголя и т. д.). До операции Вы должны подписать форму согласия на операцию и проведение анестезии.
д.). До операции Вы должны подписать форму согласия на операцию и проведение анестезии.
Подготовка к операции
-
Перед хирургическим вмешательством и анестезией
-
Предупредите врача обо всех изменениях здоровья, в частности для женщин – о начале менструации или о возможной беременности
-
Откажитесь от приема алкоголя и курения за 12 часов до визита в клинику
-
Подготовьтесь к возможной госпитализации на срок более суток.
В день операции
-
Не принимайте еду за 6 часов и напитки за 4 часа до операции
-
Не используйте косметику, лак для ногтей, контактные линзы. Накрашенные или искусственные ногти могут затруднять работу накладываемого на палец датчика слежения за кислородом
-
Принимайте назначенные анестезиологом лекарства не более, чем с одним глотком воды
-
Утром в день операции примите душ
-
В клинику следует прийти в указанное в направлении время
-
Непосредственно перед операцией необходимо переодеться в специальное белье, выданное Вам медсестрой
-
Снимите и отдайте медицинской сестре в отделении все украшения и кольца, очки, контактные линзы и съемные зубные протезы
-
Непосредственно перед операцией посетите туалет
-
При необходимости возьмите с собой в операционную слуховой аппарат или ингалятор, применяемый при астме.

После операции
-
Восстановление после анестезии происходит в послеоперационной палате, где медицинский персонал наблюдает за дыханием, пульсом, артериальным давлением, болевыми ощущениями. При необходимости вводятся обезболивающие препараты и подается кислород. Если Вам была проведена спинальная анестезия, то контролируется также восстановление подвижности и чувствительности в нижних конечностях. В палату стационара Вы будете переведены только после пробуждения при условии удовлетворительного состояния.
-
В зависимости от сложности операции может потребоваться послеоперационное лечение в отделении интенсивной терапии.
-
После операции в области раны может возникнуть боль. Для ее предотвращения или лечения Вам будут вводиться обезболивающие лекарства. У разных людей даже при одинаковых операциях интенсивность болевых ощущений может сильно отличаться. Сильная боль способствует нарушению сна, вызывает страх и раздражительность.
 Чем быстрее будет достигнут контроль над болью, тем быстрее Вы восстановитесь после перенесенной операции. Не надо терпеть боль! Если Вы почувствовали боль, сообщите об этом медицинской сестре.
Чем быстрее будет достигнут контроль над болью, тем быстрее Вы восстановитесь после перенесенной операции. Не надо терпеть боль! Если Вы почувствовали боль, сообщите об этом медицинской сестре. -
Даже если операция проводится амбулаторно, и уже вечером Вы сможете уехать домой, покинуть клинику можно только с разрешения анестезиолога или хирурга. Необходимо, чтобы Вас сопровождал кто-то из друзей или близких (для детей сопровождающим не может быть человек, управляющий автомобилем). Все специальные рекомендации будут даны Вам перед выпиской из клиники.
В первые сутки после операции не рекомендуется:
-
Принимать алкоголь, снотворные или психотропные вещества, переедать вечером после операции
-
Управлять автомобилем или пользоваться другими потенциально опасными устройствами
-
Находиться в местах, требующих повышенного внимания, принимать важные решения
-
Оставаться в одиночестве в первые сутки после операции.

Противопоказания к анестезии
Врач не имеет право отказать пациенту в анестезии при проведении оперативного вмешательства.
Для каждого планового вмешательства есть определенный перечень видов анестезии, которые можно использовать. Вид анестезии для каждого пациента определяется во время консультации с анестезиологом перед операцией. Только оценив состояние пациента, сопутствующие заболевания, лекарственные препараты, которые он принимает, анестезиолог может сделать вывод о том, какая именно анестезия подходит конкретному пациенту при конкретной операции. Врач-анестезиолог совместно с пациентом составляет индивидуальный план анестезии.
Если у пациента в прошлом проявлялись аллергические реакции на лидокаин или новокаин, ему проведут анестезию с использованием других препаратов. Так же предварительно может быть рекомендована консультация аллерголога и проведение аллергопроб.
Противопоказания к общей анестезии:
— Тяжелое состояние пациента, когда риск анестезии может оказаться выше риска самой операции. Это может быть недавно перенесенный инфаркт миокарда, тяжелая сердечная или дыхательная недостаточность, недавно перенесенные операции.
Это может быть недавно перенесенный инфаркт миокарда, тяжелая сердечная или дыхательная недостаточность, недавно перенесенные операции.
— Анатомические особенности пациента (слишком высокий вес, короткая шея).
В этих случаях анестезиолог совместно с хирургом определяют, какое анестезиологическое пособие подойдет данному пациенту.
Противопоказания к регионарной анестезии (спинальная, эпидуральная):
— отказ самого пациента;
— инфекционный процесс в месте укола;
— татуировка в месте укола – относительное противопоказание; в ряде случаев можно ввести анестезию в другом месте или под другим углом.
Отсрочить проведение анестезии и самой операции врачам придётся в случаях:
— В случае общей анестезии — если пациент не выполнил рекомендации об отказе от приема пищи и жидкости перед операцией.
— В случае регионарной анестезии — если пациент недавно принял антикоагулянтный препарат (разжижающий кровь), и он продолжает действовать.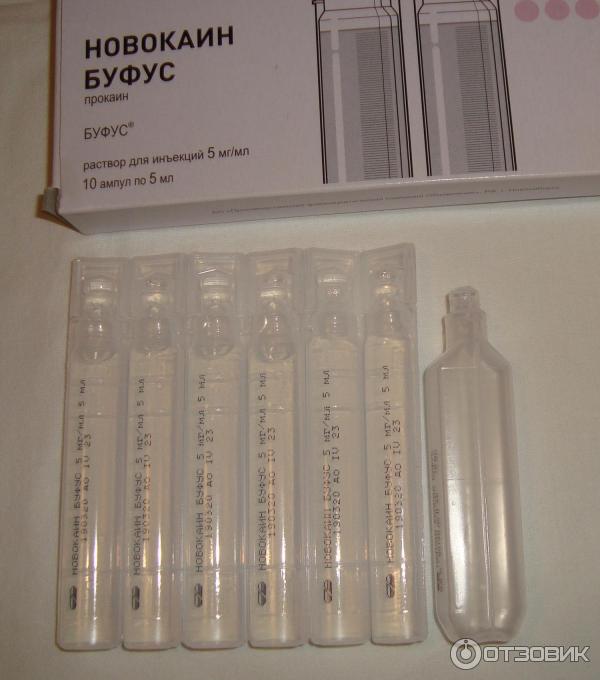 Тогда проведение анестезии возможно только после того, как закончится действие текущей дозы препарата.
Тогда проведение анестезии возможно только после того, как закончится действие текущей дозы препарата.
Благодаря новым технологиям и современным протоколам проведения анестезии НЕ являются противопоказаниями:
— активное кровотечение,
— тяжелый инфекционный процесс (сепсис),
— сердечно-сосудистые заболевания.
Показания к проведению манипуляций под медикаментозным сном в дополнение к местной анестезии:
— тяжелое психоэмоциональное состояние,
— поздний возраст и сопутствующие заболевания,
— детский возраст.
Рандомизированное контролируемое исследование эффективности лидокаинового геля по сравнению с тетракаиновыми каплями в качестве единственного местного анестетика при первичной хирургии птеригиума
Иссечение птеригиума — относительно простая амбулаторная процедура, выполняемая многими офтальмологами. Анестезия при иссечении птеригиума может быть достигнута введением ретробульбарной или перибульбарной анестезии. Однако сообщалось о серьезных осложнениях от инъекций. 17, 18 Другим вариантом является субконъюнктивальная инъекция.Однако такие недостатки, как кровоизлияние и отек ткани, могут скрывать операционное поле и плоскость, сообщалось о травмах мышц или мышечных оболочек и случайных перфорациях глазного яблока. 16
Однако сообщалось о серьезных осложнениях от инъекций. 17, 18 Другим вариантом является субконъюнктивальная инъекция.Однако такие недостатки, как кровоизлияние и отек ткани, могут скрывать операционное поле и плоскость, сообщалось о травмах мышц или мышечных оболочек и случайных перфорациях глазного яблока. 16
В последние годы стало популярным избегать инъекционной анестезии при офтальмологических процедурах. Многие катарактальные хирурги заменили традиционные методы ретробульбарной и перибульбарной инъекций местной анестезией. 10 Хирургия птеригиума является экстраокулярной процедурой и поэтому должна подходить для местной анестезии.Применение местной анестезии при птеригиуме имеет много преимуществ: (1) не требуется, чтобы врач наносил анестетик, и, таким образом, экономится драгоценное операционное время, (2) пациенты субъективно чувствуют себя более комфортно без необходимости инъекции глаза», (3) произвольные движения глаз сохраняются на протяжении всей операции, что позволяет обеспечить соответствующее хирургическое позиционирование под руководством хирурга, и (4) анатомические и тканевые плоскости остаются нетронутыми, что позволяет точно визуализировать, манипулировать и препарировать ткани.
Frutch-Pery применил беноксинат 0,4% для хирургии птеригиума. 7 Однако перед операцией требовалась одна капля каждую минуту в течение 10 минут, а также частое добавление капель (каждые 5 минут) на протяжении всей процедуры. Введение такого количества капель довольно обременительно и неудобно.
С другой стороны, гель лидокаина 2% широко используется для местной анестезии при урогенитальных и кожных процедурах; а также применялся в офтальмологии для трабекулэктомии, трансплантации роговицы и хирургии катаракты. 10, 19, 20, 21, 22 Все наши пациенты завершили операции с назначенным им лечением. Ни одному из пациентов в группе лидокаина или тетракаина не потребовался возврат к обычной инъекционной анестезии из-за неадекватной анестезии. В соответствии с обычной практикой в нашем центре никому из наших пациентов не давали седативных средств. В результате это не повлияет на воспоминания пациента о дискомфорте или боли, испытанных во время операции.
Показатели боли оказались относительно высокими в обеих группах. Поскольку это первое рандомизированное исследование, в котором сравнивалась эффективность лидокаинового геля и местных капель, другие показатели боли для прямого сравнения ограничены. Тем не менее, предыдущий отчет об оценке боли при субконъюнктивальной инъекции раствора лидокаина по сравнению с гелем лидокаина для местного применения дал средний балл боли 4,0 ± 1,01 в группе, получавшей гель. 13 Наш средний балл 3,03±2,35 для группы лидокаина во время удаления птеригиума меньше, чем сообщалось ранее. Кроме того, оценка боли при обоих исследованиях геля с лидокаином была выше, чем при операции по поводу косоглазия, при этом средняя оценка боли составила 2 балла.6. 12
Поскольку это первое рандомизированное исследование, в котором сравнивалась эффективность лидокаинового геля и местных капель, другие показатели боли для прямого сравнения ограничены. Тем не менее, предыдущий отчет об оценке боли при субконъюнктивальной инъекции раствора лидокаина по сравнению с гелем лидокаина для местного применения дал средний балл боли 4,0 ± 1,01 в группе, получавшей гель. 13 Наш средний балл 3,03±2,35 для группы лидокаина во время удаления птеригиума меньше, чем сообщалось ранее. Кроме того, оценка боли при обоих исследованиях геля с лидокаином была выше, чем при операции по поводу косоглазия, при этом средняя оценка боли составила 2 балла.6. 12
Все оценки пациентов были получены медсестрой операционной сразу после операции в послеоперационном периоде. Хирург также заполнил лист данных отдельно в кабинете хирурга сразу после операции. Таким образом, удалось избежать риска предвзятости хирурга, который мог выслушать ответы пациентов.
Две группы были сопоставимы по возрасту, размеру группы и распределению по полу. Вопреки нашим ожиданиям, основанным на нашем опыте в хирургии косоглазия, 12 , к нашему удивлению, не было существенной разницы в оценке боли у пациентов на стадии 2.Это может быть связано со следующими причинами: (1) операции были относительно простыми и быстрыми, без необходимости забора какого-либо трансплантата конъюнктивы, (2) во время процедуры «дополнительное» применение назначенных анестетиков было дано только перед удалением птеригиума, и (3) дополнительные капли, которые пациенту давали «по требованию», также могли предотвратить боль, которая могла бы возникнуть в противном случае. Однако для 3-го этапа при ушивании конъюнктивальной раны наблюдалась статистически значимая разница средних показателей боли.Вероятно, это связано с составом геля с увеличенным временем контакта с поверхностью глаза, что создает устойчивый эффект лидокаина. Еще одним преимуществом использования геля является его смазывающий эффект, исключающий необходимость смачивания роговицы во время операции. 12 Гель лидокаина 2% показал себя эффективным средством контроля боли в послеоперационном периоде. 14 Наше исследование также продемонстрировало, что 2% гель лидокаина для местного применения также безопасен и эффективен для анестезии при первичной хирургии птеригиума.
12 Гель лидокаина 2% показал себя эффективным средством контроля боли в послеоперационном периоде. 14 Наше исследование также продемонстрировало, что 2% гель лидокаина для местного применения также безопасен и эффективен для анестезии при первичной хирургии птеригиума.
К недостаткам тетракаиновых капель можно отнести необходимость нескольких введений до и во время операции, относительно короткое время контакта и возможность кумулятивной токсичности. Однако мы не наблюдали каких-либо осложнений эпителия роговицы или поверхности глаза ни во время, ни после операции ни в одной из групп.
В заключение следует отметить, что как местный гель лидокаина 2 %, так и глазные капли тетракаина 1 % могут считаться эффективными и безопасными анестетиками при хирургии птеригиума.Однако для лидокаина требуется гораздо меньшее количество дополнительных анестезирующих капель. Кроме того, 2% гель лидокаина имеет дополнительное преимущество в виде удобства применения, пролонгированного действия и смазывающего эффекта. «Безыгольная» анестезия будет интересна пациентам, которые могут быть обеспокоены глазными инъекциями и избеганием всех осложнений и травм, связанных с инъекциями.
«Безыгольная» анестезия будет интересна пациентам, которые могут быть обеспокоены глазными инъекциями и избеганием всех осложнений и травм, связанных с инъекциями.
Затылочный блок | Кедры-Синай
Во время блокады затылочного нерва около чайной ложки местного анестетика и стероидов вводят в кожу головы, где находится ствол нерва.Инъекцию делают в затылок, чуть выше шеи. Перед инъекцией кожа обезболивается. Для блокады нерва используется очень тонкая игла.
Если инъекция была сделана правильно, кожа головы на этой стороне головы быстро онемеет. Облегчение боли можно почувствовать иногда в течение нескольких минут. Врач может спросить, что пациент чувствует с точки зрения его или ее симптомов.
Если есть сильный отек нерва, стероиды уменьшат боль.Полный эффект от стероидов может не ощущаться в течение двух-трех дней. Их эффект более продолжительный — иногда недели или месяцы.
После блокады затылочного нерва пациент обычно может ехать домой и вернуться к обычной повседневной деятельности на следующий день. Действие местного анестетика может пройти через несколько часов, но действие стероида начинает усиливаться в течение следующих нескольких дней.
Действие местного анестетика может пройти через несколько часов, но действие стероида начинает усиливаться в течение следующих нескольких дней.
Наилучший ответ на блокаду затылочного нерва обычно дают пациенты, у которых боль возникла относительно недавно, а не давно.
Если первая блокада затылочного нерва не облегчает симптомы пациента в течение недели или двух, может потребоваться повторная инъекция. Дополнительные нервные блокады могут быть сделаны, чтобы держать симптомы под контролем.
С другой стороны, отсутствие результатов может быть признаком того, что затылочные нервы не являются источником боли, и необходимо провести дальнейшую работу по диагностике причины боли.
Редко проводится более трех блокад затылочного нерва в течение шести месяцев.Чем больше инъекций стероидов делается, тем выше вероятность побочных эффектов. Если необходимы более частые инъекции, вероятно, будет рассмотрен другой тип лечения.
Сюда могут входить:
- Перерезание нерва
- Уменьшение давления на нерв
- Уничтожение нервных клеток малыми дозами яда или радиочастотной энергии
- Установка стимулятора затылочного нерва.
 Это работает как кардиостимулятор в сердце.
Это работает как кардиостимулятор в сердце.
Людям с аллергией на стероиды или другие лекарства, входящие в состав блокады затылочного нерва, нельзя проводить эту процедуру. Людям, принимающим препараты для разжижения крови, страдающим активной инфекцией, плохо контролируемому диабету или сердечным заболеваниям, не следует проводить блокаду затылочного нерва до тех пор, пока их общее состояние здоровья не улучшится.
Лидокаин для инъекций BP с консервантом 1% — Краткое описание характеристик продукта (SmPC)
Эта информация предназначена для медицинских работников
Лидокаин для инъекций BP с консервантом 1 %
Каждый 1 мл содержит 10.0 мг лидокаина гидрохлорида, что соответствует 8,1 мг лидокаина.
Каждые 20 мл раствора содержат 200 мг лидокаина гидрохлорида
Полный список вспомогательных веществ см. в разделе 6.1
Раствор для инъекций.
Прозрачный и бесцветный раствор.
Лидокаин для инъекций используется в качестве местного анестетика.
Лидокаин для инъекций используется в качестве местного анестетика при подкожной инъекции.
Этот раствор не предназначен для внутривенного введения.Растворы лидокаина, содержащие консерванты, не следует использовать для спинальной, эпидуральной, каудальной или внутривенной регионарной анестезии.
Дозировку следует корректировать в зависимости от реакции пациента и места введения. Следует давать наименьшую концентрацию и наименьшую дозу, вызывающую требуемый эффект. Максимальная разовая доза для здоровых взрослых не должна превышать 200 мг, что соответствует 20 мл.
Детям, пожилым и ослабленным пациентам требуются меньшие дозы, соответствующие возрасту и физическому состоянию.
• Известная гиперчувствительность к лидокаину или другим анестетикам амидного типа
.• Известная гиперчувствительность к гидроксибензоатам
• Полная блокада сердца
• Гиповолемия
Как и другие местные анестетики, лидокаин следует применять с осторожностью у пациентов с эпилепсией, нарушениями сердечной проводимости (см. также раздел «Противопоказания»), застойной сердечной недостаточностью, брадикардией, тяжелым шоком, нарушениями функции дыхания или почек с клиренсом креатинина менее 10 мл/мин.Лидокаин метаболизируется в печени, поэтому его следует применять с осторожностью у пациентов с нарушением функции печени. Лидокаин не следует применять при острой порфирии.
также раздел «Противопоказания»), застойной сердечной недостаточностью, брадикардией, тяжелым шоком, нарушениями функции дыхания или почек с клиренсом креатинина менее 10 мл/мин.Лидокаин метаболизируется в печени, поэтому его следует применять с осторожностью у пациентов с нарушением функции печени. Лидокаин не следует применять при острой порфирии.
Пациенты с миастенией особенно чувствительны к действию местных анестетиков.
При введении местных анестетиков должны быть доступны помещения для реанимации.
Эффект местных анестетиков может быть снижен, если инъекция производится в воспаленную или инфицированную область.
Некоторые процедуры местной анестезии могут быть связаны с серьезными побочными реакциями, независимо от используемого местного анестетика.
• Ретробульбарные инъекции могут редко достигать черепного субарахноидального пространства, вызывая серьезные/тяжелые реакции, включая сердечно-сосудистый коллапс, апноэ, судороги и временную слепоту
• Ретро- и перибульбарные инъекции местных анестетиков несут низкий риск стойкой глазодвигательной дисфункции. Основные причины включают травму и/или местное токсическое воздействие на мышцы и/или нервы.
Основные причины включают травму и/или местное токсическое воздействие на мышцы и/или нервы.
Тяжесть таких тканевых реакций зависит от степени травмы, концентрации местного анестетика и продолжительности воздействия местного анестетика на ткани. По этой причине, как и для всех местных анестетиков, следует использовать наименьшую эффективную концентрацию и дозу местного анестетика.
Hameln Lidocaine Injection не рекомендуется для новорожденных. Оптимальная концентрация лидокаина в сыворотке, необходимая для предотвращения токсичности, такой как судороги и сердечные аритмии, в этой возрастной группе неизвестна.
Влияние лидокаина на другие лекарственные средства
Лидокаин следует использовать с осторожностью у пациентов, получающих другие местные анестетики или агенты, структурно родственные местным анестетикам амидного типа (например, антиаритмические средства, такие как мексилетин), поскольку системные токсические эффекты являются аддитивными. Специфические исследования взаимодействия с лидокаином и антиаритмическими препаратами класса III (например, амиодароном) не проводились, но рекомендуется соблюдать осторожность.
Может быть повышен риск усиленной и продолжительной нервно-мышечной блокады у пациентов, одновременно получающих миорелаксанты (например,г. суксаметоний).
Влияние других лекарственных средств на лидокаин
Может быть повышен риск желудочковой аритмии у пациентов, получающих одновременно антипсихотики, которые удлиняют или могут удлинить интервал QT (например, пимозид, сертиндол, оланзапин, кветиапин, зотепин) или антагонисты 5HT 3 (например, трописетрон, доласетрон).
Следует избегать одновременного применения хинупристин/дальфопристин.
Гипокалиемия, вызванная ацетазоламидом, петлевыми диуретиками и тиазидами, противодействует действию лидокаина.
Клиренс лидокаина может снижаться блокаторами бета-адренорецепторов (например, пропранололом) и циметидином, что требует снижения дозы лидокаина. Повышение уровня лидокаина в сыворотке также может происходить при приеме противовирусных препаратов (например, ампренавир, атазанавир, дарунавир, лопинавир).
Сообщалось о сердечно-сосудистом коллапсе после применения бупивакаина у пациентов, получавших верапамил и тимолол; лидокаин близок к бупивакаину.
Хотя адреналин (эпинефрин) при использовании в сочетании с лидокаином может снижать всасывание в сосудах, он значительно увеличивает опасность желудочковой тахикардии и фибрилляции при случайном внутривенном введении.
Беременность
Хотя исследования на животных не выявили признаков вреда для плода, лидокаин проникает через плаценту и не должен вводиться на ранних сроках беременности, за исключением случаев, когда считается, что преимущества перевешивают риски.
Лидокаин, вводимый путем местной перинеальной инфильтрации перед родами, быстро проникает в кровоток плода. Повышенный уровень лидокаина может сохраняться у новорожденного в течение не менее 48 часов после родов. Может возникнуть брадикардия плода или брадикардия новорожденного, гипотония или угнетение дыхания.
Лактация
Небольшие количества лидокаина секретируются в грудное молоко, и при применении лидокаина у кормящих матерей следует учитывать возможность аллергической реакции у младенца, хотя и отдаленной.
Если амбулаторная анестезия затрагивает участки тела, связанные с вождением автомобиля или работой с механизмами, пациентам следует рекомендовать избегать этих действий до полного восстановления нормальной функции.
Как и в случае с другими местными анестетиками, побочные реакции на лидокаин редки и обычно являются результатом повышения концентрации в плазме из-за случайного внутрисосудистого введения, чрезмерной дозы или быстрого всасывания из сильно сосудистых областей или могут быть результатом гиперчувствительности, идиосинкразии или сниженной толерантности. со стороны пациента.Системная токсичность в основном поражает центральную нервную систему и/или сердечно-сосудистую систему (см. также 4.9 Передозировка).
Растворы лидокаина, содержащие консерванты, не подходят для спинальной, эпидуральной или каудальной анестезии. Побочные эффекты, о которых сообщалось после введения растворов лидокаина без консервантов этим путем, включают гипотензию и отдельные случаи брадикардии и остановки сердца.
Нарушения иммунной системы
Реакции гиперчувствительности (аллергические или анафилактоидные реакции, анафилактический шок) – см. также Заболевания кожи и подкожной клетчатки).Кожные пробы на аллергию на лидокаин не считаются надежными.
Нервные и психические расстройства
Неврологические признаки системной токсичности включают головокружение или предобморочное состояние, нервозность, тремор, околоротовую парестезию, онемение языка, сонливость, судороги, кому.
Реакции нервной системы могут быть возбуждающими и/или угнетающими. Признаки стимуляции ЦНС могут быть кратковременными или вообще не проявляться, поэтому первыми признаками токсичности могут быть спутанность сознания и сонливость, за которыми следуют кома и дыхательная недостаточность.
Неврологические осложнения спинномозговой анестезии включают преходящие неврологические симптомы, такие как боль в нижней части спины, ягодицах и ногах. Эти симптомы обычно развиваются в течение двадцати четырех часов после анестезии и проходят в течение нескольких дней. Сообщалось об отдельных случаях арахноидита или синдрома конского хвоста с персистирующей парестезией, дисфункцией кишечника и мочевыводящих путей или параличом нижних конечностей после спинальной анестезии лидокаином и другими подобными препаратами. Большинство случаев были связаны с гипербарическими концентрациями лидокаина или длительной спинальной инфузией.
Сообщалось об отдельных случаях арахноидита или синдрома конского хвоста с персистирующей парестезией, дисфункцией кишечника и мочевыводящих путей или параличом нижних конечностей после спинальной анестезии лидокаином и другими подобными препаратами. Большинство случаев были связаны с гипербарическими концентрациями лидокаина или длительной спинальной инфузией.
Заболевания глаз
Затуманенное зрение, диплопия и преходящий амавроз могут быть признаками отравления лидокаином.
Двусторонний амавроз также может быть следствием случайной инъекции оболочки зрительного нерва во время офтальмологических процедур. Сообщалось о воспалении орбиты и диплопии после ретро- или перибульбарной анестезии (см. раздел 4.4 «Особые предупреждения и меры предосторожности при использовании»)
Болезни уха и лабиринта
Звон в ушах, гиперакузия
Сердечные и сосудистые заболевания
Сердечно-сосудистые реакции являются угнетающими и могут проявляться гипотензией, брадикардией, угнетением миокарда, сердечными аритмиями и, возможно, остановкой сердца или циркуляторным коллапсом.
Заболевания органов дыхания, грудной клетки или средостения
Одышка, бронхоспазм, угнетение дыхания, остановка дыхания
Желудочно-кишечные расстройства
Тошнота, рвота
Заболевания кожи и подкожной клетчатки
Сыпь, крапивница, отек (включая ангионевротический отек, отек лица)
Болезни крови и лимфатической системы
Метгемоглобинемия.
Сообщение о предполагаемых побочных реакциях
Важно сообщать о предполагаемых нежелательных реакциях после регистрации лекарственного средства. Это позволяет осуществлять постоянный мониторинг соотношения польза/риск лекарственного средства. Медицинских работников просят сообщать о любых предполагаемых нежелательных реакциях через схему желтой карточки по адресу: www.mhra.gov.uk/yellowcard.
Симптомы острой системной токсичности
Токсическое воздействие на центральную нервную систему проявляется симптомами нарастающей тяжести. Первоначально у пациентов могут наблюдаться околоротовая парестезия, онемение языка, головокружение, гиперакузия и шум в ушах. Нарушение зрения и мышечный тремор или подергивание мышц более серьезны и предшествуют возникновению генерализованных судорог. Эти признаки не следует принимать за невротическое поведение. Могут последовать потеря сознания и большие судорожные припадки, которые могут длиться от нескольких секунд до нескольких минут. Гипоксия и гиперкапния возникают быстро после судорог из-за повышенной мышечной активности, а также нарушения нормального дыхания и нарушения проходимости дыхательных путей.В тяжелых случаях может возникнуть апноэ. Ацидоз усиливает токсическое действие местных анестетиков.
Первоначально у пациентов могут наблюдаться околоротовая парестезия, онемение языка, головокружение, гиперакузия и шум в ушах. Нарушение зрения и мышечный тремор или подергивание мышц более серьезны и предшествуют возникновению генерализованных судорог. Эти признаки не следует принимать за невротическое поведение. Могут последовать потеря сознания и большие судорожные припадки, которые могут длиться от нескольких секунд до нескольких минут. Гипоксия и гиперкапния возникают быстро после судорог из-за повышенной мышечной активности, а также нарушения нормального дыхания и нарушения проходимости дыхательных путей.В тяжелых случаях может возникнуть апноэ. Ацидоз усиливает токсическое действие местных анестетиков.
Воздействие на сердечно-сосудистую систему может наблюдаться в тяжелых случаях. Гипотензия, брадикардия, аритмия и остановка сердца могут возникнуть в результате высоких системных концентраций с потенциально летальным исходом.
Восстановление происходит в результате перераспределения местного анестетика из центральной нервной системы и метаболизма и может быть быстрым, если только не было введено большое количество препарата.
Лечение острой токсичности
При появлении признаков острой системной токсичности введение анестетика следует немедленно прекратить.
Лечение потребуется, если возникают судороги и угнетение ЦНС. Целями лечения являются поддержание оксигенации, купирование судорог и поддержание кровообращения.
Следует установить проходимые дыхательные пути и ввести кислород вместе с искусственной вентиляцией легких (маска и мешок), если необходимо.Циркуляцию следует поддерживать инфузиями плазмы или внутривенными жидкостями. Если требуется дальнейшее поддерживающее лечение угнетения кровообращения, можно рассмотреть возможность использования вазопрессоров, хотя это сопряжено с риском возбуждения центральной нервной системы.
Если судороги не прекращаются спонтанно в течение 15-20 секунд, их можно купировать внутривенным введением диазепама или тиопентана натрия, принимая во внимание, что противосудорожные препараты могут также угнетать дыхание и кровообращение. Продолжительные судороги могут поставить под угрозу вентиляцию легких и оксигенацию пациента, поэтому следует рассмотреть возможность ранней эндотрахеальной интубации. В случае остановки сердца следует провести стандартные процедуры сердечно-легочной реанимации. Постоянная оптимальная оксигенация, вентиляция и поддержка кровообращения, а также лечение ацидоза имеют жизненно важное значение.
Продолжительные судороги могут поставить под угрозу вентиляцию легких и оксигенацию пациента, поэтому следует рассмотреть возможность ранней эндотрахеальной интубации. В случае остановки сердца следует провести стандартные процедуры сердечно-легочной реанимации. Постоянная оптимальная оксигенация, вентиляция и поддержка кровообращения, а также лечение ацидоза имеют жизненно важное значение.
Диализ имеет незначительное значение при лечении острой передозировки лидокаином.
Фармакотерапевтическая группа: местный анестетик, код АТС: N01BB02.
Лидокаин — местный анестетик амидной группы. Он используется для обеспечения местной анестезии в различных участках тела и действует путем ингибирования ионных рефлюксов, необходимых для инициации и проведения импульсов, тем самым стабилизируя мембрану нейронов. В дополнение к блокированию проводимости в нервных аксонах периферической нервной системы лидокаин оказывает важное влияние на центральную нервную систему и сердечно-сосудистую систему. После всасывания лидокаин может вызвать стимуляцию ЦНС с последующей депрессией.В сердечно-сосудистой системе он действует в первую очередь на миокард, где может вызывать снижение электрической возбудимости, скорости проводимости и силы сокращения.
После всасывания лидокаин может вызвать стимуляцию ЦНС с последующей депрессией.В сердечно-сосудистой системе он действует в первую очередь на миокард, где может вызывать снижение электрической возбудимости, скорости проводимости и силы сокращения.
Лидокаин всасывается из мест инъекции, в том числе из мышц, и скорость его всасывания определяется такими факторами, как место введения и сосудистый состав тканей. За исключением внутрисосудистого введения, самые высокие уровни в крови наблюдаются после блокады межреберных нервов, а самые низкие — после подкожного введения.Лидокаин связывается с белками плазмы, в том числе с альфа-1-кислотным гликопротеином. Препарат проникает через гематоэнцефалический и плацентарный барьеры.
Лидокаин метаболизируется в печени, и около 90 % введенной дозы подвергается N-деалкилированию с образованием моноэтилглицинексилидида и глицинексилидида, оба из которых могут способствовать терапевтическим и токсическим эффектам лидокаина. Происходит дальнейший метаболизм и метаболиты выводятся с мочой с менее чем 10 % неизмененного лидокаина. Период полувыведения лидокаина после внутривенной болюсной инъекции составляет от одного до двух часов, но у пациентов с нарушением функции печени он может быть продлен.
Период полувыведения лидокаина после внутривенной болюсной инъекции составляет от одного до двух часов, но у пациентов с нарушением функции печени он может быть продлен.
Никакой дополнительной информации, кроме той, которая включена в Сводку характеристик продукта.
Хлорид натрия Ph. Eur.
Метилгидроксибензоат Ph. Eur. (1,7 мг/мл)
Пропилгидроксибензоат Ph. Eur. (0,3 мг/мл)
Кислота соляная Ph. Eur. (КС)
Гидроксид натрия Ph. Eur. (КС)
Вода для инъекций Ph. Eur.
Лидокаин вызывает осаждение амфотерицина, метогекситона натрия и сульфадиазина натрия при инъекции глюкозы.Рекомендуется избегать смесей лидокаина и тринитрата глицерина
Держите контейнер во внешней картонной упаковке для защиты от света.
Хранить при температуре от 10°C до 25°C.
Флакон из прозрачного стекла типа II, 20 мл и 50 мл, с пробкой из хлорбутилкаучука, пластиковой внешней крышкой и внутренним алюминиевым кольцом. Упакованы в картонные коробки по 10 флаконов.
Использовать по указанию врача.
Хамельн Фарма ООО
Nexus, Глостерский бизнес-парк
Глостер, GL3 4AG
Великобритания
Обезболивающие глазные капли — Американская академия офтальмологии
Что такое обезболивающие глазные капли?
Боль в глазах может быть вызвана множеством причин.Чаще всего это происходит после операции на глазах, травмы глаза или инфекции. Это также симптом глазной аллергии и иногда сухости глаз. Для облегчения и заживления офтальмолог может назначить обезболивающие глазные капли.
Как правило, для облегчения боли используются три различных типа глазных капель. В том числе:
- НПВП (нестероидные противовоспалительные препараты): действие этих глазных капель заключается в уменьшении количества вещества в организме, которое усиливает ощущение боли и вызывает отек.Их можно использовать при заживлении после операции на глазах, травм или инфекций и воспалений.

- Кортикостероиды: как и НПВП, кортикостероиды уменьшают количество веществ в организме, вызывающих отек и воспаление. Эти препараты также можно использовать при лечении глазных операций, травм или инфекций.
- Местные анестетики: эти глазные капли, вызывающие анестезию, назначаются вашим офтальмологом, чтобы блокировать передачу болевых сигналов по нервным окончаниям глаза в мозг. (Знаете ли вы, что в роговице больше нервных окончаний, чем в любой другой части тела? Вот почему тыкать себе в глаз так больно!) Они используются для более удобного обследования глаз (например, при измерении глазного давления). и блокировать боль во время операции на глазах.
Почему я не могу купить обезболивающие глазные капли без рецепта?
Большинство обезболивающих глазных капель доступны только по рецепту по нескольким важным причинам:
- Когда вы обратитесь к офтальмологу для облегчения боли в глазах, он сможет найти и устранить фактическую причину вашей боли и, возможно, сохранить ваше зрение.

- Ваш офтальмолог знает правильный тип и дозу глазных капель для лечения вашего состояния глаз и назначит их специально для вас.
- Некоторые глазные капли могут вызвать дополнительные проблемы со здоровьем. Например, они могут привести к проблемам с поверхностью вашего глаза, глазной инфекции или другим осложнениям, если они используются чрезмерно или используются неправильно. Ваш офтальмолог убедится, что вы знаете, как часто использовать глазные капли и как правильно их закапывать.
- Назначая вам обезболивающие глазные капли, ваш врач может внимательно следить за состоянием ваших глаз и следить за тем, чтобы вы получали необходимую помощь в нужное время.
Если аллергия или сухость глаз вызывают пощипывание или жжение в глазах, могут помочь некоторые глазные капли, отпускаемые без рецепта (без рецепта). Например, искусственные слезы без консервантов можно использовать так часто, как это необходимо, для облегчения жжения и сухости глаз. Тем не менее, другие безрецептурные капли, предназначенные для устранения красноты раздраженных глаз, могут на самом деле вызвать больше проблем с красными глазами, если их использовать слишком часто.
Безопасны ли обезболивающие глазные капли?
Обезболивающие глазные капли с обезболивающим эффектом назначаются только врачом и не продаются без рецепта.При использовании под наблюдением офтальмолога эти обезболивающие глазные капли безопасны.
Капли для обезболивания глаз могут иметь некоторые побочные эффекты, например:
- вызывает нечеткое зрение,
- повышает чувствительность к свету,
- вызывает слезотечение или покраснение глаз,
- вызывает у вас пульсирующую боль или жжение в глазах,
- вызывает онемение носа и носовых пазух, когда капли соскальзывают из глаза в носовые пазухи.
Слишком частое использование обезболивающих глазных капель (будь то из-за частых осмотров глаз или их использования без наблюдения врача) может вызвать проблемы со здоровьем. Обязательно сообщите своему офтальмологу, если вы используете эти капли, и они их не прописали.
НПВП от боли в глазах безопасны, если их использовать точно так, как их прописал врач. Они могут иметь некоторые побочные эффекты, в том числе:
Они могут иметь некоторые побочные эффекты, в том числе:
Кортикостероиды от боли в глазах также, как правило, безопасны, если их использовать точно по назначению офтальмолога.Тем не менее, они обычно не предназначены для использования в течение длительного времени, так как могут вызвать некоторые проблемы. Например, использование кортикостероидных глазных капель дольше, чем рекомендуется, может вызвать повышение глазного давления и привести к проблемам с глаукомой. Длительное использование может даже привести к катаракте и возможной глазной инфекции. Вы также можете заметить неприятный вкус в горле или во рту через несколько минут после того, как поместите их в глаза. Ваш офтальмолог будет использовать эти капли в ограниченном количестве для облегчения боли в глазах при лечении проблемы, вызывающей вашу боль.
Сравнительное исследование местной и ретробульбарной анестезии при сложной хирургии катаракты | Хирургия | JAMA Офтальмология
Цели Оценить и сравнить уровни дискомфорта пациента и периоперационных осложнений при факоэмульсификации и имплантации складной интраокулярной линзы под местной лидокаин гидрохлоридом и ретробульбарной анестезией у пациентов с катарактой, у которых также были эксфолиативный синдром, увеит, задние синехии, факодонез или ранее проведенные внутриглазные операции.
Дизайн Проспективное рандомизированное контролируемое исследование было проведено в 2 учреждениях.
Участники В общей сложности 476 глаз 476 пациентов с различными хорошо установленными факторами риска соответствовали критериям включения. На 238 глазах факоэмульсификацию проводили под ретробульбарной анестезией, на остальных 238 глазах местную анестезию.
Вмешательства Всем пациентам была проведена временная факоэмульсификация чистой роговицы и имплантация складной интраокулярной линзы.Пациентам под ретробульбарной анестезией однократно (3,5–5,5 мл) вводили в ретробульбарное пространство комбинацию 0,75% бупивакаина гидрохлорида, 2% лидокаина и гиалуронидазы. Пациенты в группе местной анестезии получили минимум 5 доз (примерно 40 мкл на дозу) 2% лидокаина для местного применения. Никаких внутрикамерных инъекций каких-либо анестетиков не производилось.
Показатели основных результатов Количество осложнений и нежелательных явлений. Об интраоперационных условиях судил хирург (П.C.J. или F.K.J.), а 10-балльную визуальную аналоговую шкалу использовали сразу после операции для оценки общей тяжести интраоперационной боли у каждого пациента.
Об интраоперационных условиях судил хирург (П.C.J. или F.K.J.), а 10-балльную визуальную аналоговую шкалу использовали сразу после операции для оценки общей тяжести интраоперационной боли у каждого пациента.
Результаты Общая частота интраоперационных осложнений составила 1,9% при разрыве капсулы, 3,8% при разрыве связочного аппарата, 1,5% при потере стекловидного тела и 1,0% при выпадении радужной оболочки. Помимо частоты потери стекловидного тела, которая была значительно ( P = 0,041) ниже в группе местной анестезии, не было обнаружено статистически значимых различий в интраоперационных и ранних послеоперационных осложнениях между группами.Дополнительная инъекция в заднее субтеноново пространство потребовалась в 1,3% случаев в группе с местной анестезией и в 0,8% в группе с ретробульбарной анестезией. Хемоз (2,5%), субконъюнктивальное кровоизлияние (1,7%) и периорбитальная гематома (0,8%) наблюдались только в группе ретробульбарной анестезии. Средние баллы + SE боли, оцененные пациентами, составили 0,84 + 1,30 в группе местной анестезии и 0,73 + 1,50 в группе ретробульбарной анестезии ( P = 0,41). Предпочтения пациентов в отношении местной анестезии (91%) оказались значительно выше ( P = .01) выше, чем при ретробульбарной анестезии (62%). Хирурги обнаружили, что интраоперационные трудности, связанные с анестезией, были немного ниже в группе ретробульбарной анестезии (8%), чем в группе местной анестезии (14%).
Предпочтения пациентов в отношении местной анестезии (91%) оказались значительно выше ( P = .01) выше, чем при ретробульбарной анестезии (62%). Хирурги обнаружили, что интраоперационные трудности, связанные с анестезией, были немного ниже в группе ретробульбарной анестезии (8%), чем в группе местной анестезии (14%).
Выводы Связанные с операцией осложнения и дискомфорт пациента были одинаковыми для двух методов анестезии. Местная анестезия оправдана как средство повышения безопасности, не вызывающее дискомфорта у пациента даже в сложных случаях хирургии катаракты.
РЕТРОБУЛЬБАРНАЯ ИНЪЕКЦИЯ анестетиков уже более века используется в хирургии катаракты. Несмотря на различные модификации, которые были разработаны на протяжении десятилетий для снижения потенциального риска повреждения интраорбитальных структур, «слепое» введение иглы в ретробульбарное пространство никогда не было полностью свободным от нескольких осложнений, угрожающих зрению и жизни. 1 -5 Местная анестезия была впервые предложена Fichman 6 в качестве привлекательной альтернативы традиционному методу введения местных анестетиков, что приводит к более быстрому восстановлению зрения и высокой удовлетворенности пациентов.К преимуществам местной анестезии относятся простота применения, минимальный или отсутствующий дискомфорт при введении, быстрое начало анестезии и, что наиболее важно, устранение потенциальных рисков, связанных с ретробульбарными инъекциями. 6 -10 В дополнение ко всем этим преимуществам методика экономична, позволяет избежать нежелательных косметических побочных эффектов и позволяет мгновенно восстановить зрение. Однако местная анестезия лишь блокирует окончания тройничного нерва, обеспечивая в лучшем случае «полное» обезболивание глаза.Зрительный нерв и двигательные нейроны пациента обычно не поражаются, что приводит к полностью сохраненной подвижности глаз. Хотя предыдущие отчеты 5 -10 указывают на то, что местная анестезия безопасна и эффективна при большинстве неосложненных операций по удалению катаракты, различные исследования 7 ,11 предполагают, что местную анестезию не следует рассматривать при наличии тяжелых сопутствующих глазных патологий.
1 -5 Местная анестезия была впервые предложена Fichman 6 в качестве привлекательной альтернативы традиционному методу введения местных анестетиков, что приводит к более быстрому восстановлению зрения и высокой удовлетворенности пациентов.К преимуществам местной анестезии относятся простота применения, минимальный или отсутствующий дискомфорт при введении, быстрое начало анестезии и, что наиболее важно, устранение потенциальных рисков, связанных с ретробульбарными инъекциями. 6 -10 В дополнение ко всем этим преимуществам методика экономична, позволяет избежать нежелательных косметических побочных эффектов и позволяет мгновенно восстановить зрение. Однако местная анестезия лишь блокирует окончания тройничного нерва, обеспечивая в лучшем случае «полное» обезболивание глаза.Зрительный нерв и двигательные нейроны пациента обычно не поражаются, что приводит к полностью сохраненной подвижности глаз. Хотя предыдущие отчеты 5 -10 указывают на то, что местная анестезия безопасна и эффективна при большинстве неосложненных операций по удалению катаракты, различные исследования 7 ,11 предполагают, что местную анестезию не следует рассматривать при наличии тяжелых сопутствующих глазных патологий. Манипуляции с радужной оболочкой или растяжение цилиарной и цинулярной тканей, которые могут быть неизбежны во время хирургического вмешательства в сложных случаях, могут раздражать неанестезированные окончания цилиарного нерва и приводить к дискомфорту пациента и непреднамеренным движениям глаз, что ставит под угрозу общую безопасность процедуры.В то время как это привело к тому, что все большее число хирургов стали вводить дополнительные анестетики путем внутрикамерной инъекции или в дополнение к ирригационной жидкости, используемой во время внутриглазной фазы операции, этот недостаток вынудил других 14 для отказа от местной анестезии в пользу перибульбарной инъекции.
Манипуляции с радужной оболочкой или растяжение цилиарной и цинулярной тканей, которые могут быть неизбежны во время хирургического вмешательства в сложных случаях, могут раздражать неанестезированные окончания цилиарного нерва и приводить к дискомфорту пациента и непреднамеренным движениям глаз, что ставит под угрозу общую безопасность процедуры.В то время как это привело к тому, что все большее число хирургов стали вводить дополнительные анестетики путем внутрикамерной инъекции или в дополнение к ирригационной жидкости, используемой во время внутриглазной фазы операции, этот недостаток вынудил других 14 для отказа от местной анестезии в пользу перибульбарной инъекции.
Насколько нам известно, проспективных исследований, анализирующих соотношение риск-польза местной и ретробульбарной анестезии в потенциально сложных случаях хирургии катаракты, не проводилось.Чтобы изучить эффективность и безопасность местной анестезии, мы разработали проспективное рандомизированное контролируемое клиническое исследование, которое будет проведено в 2 университетских центрах, в котором сравнивали ретробульбарную анестезию с только местной анестезией у пациентов с катарактой, у которых были осложнения и которым была проведена прозрачная роговичная анестезия. факоэмульсификация и имплантация складной интраокулярной линзы (ИОЛ). Помимо оценки связанных с анестезией, интраоперационных и ранних послеоперационных осложнений, мы также документировали оценку боли у пациента и интраоперационные состояния, оцененные хирургом (P.C.J. или F.K.J.), чтобы получить информацию, которая может помочь указать, какой тип анестезии предпочтительнее в сложных случаях хирургии катаракты.
факоэмульсификация и имплантация складной интраокулярной линзы (ИОЛ). Помимо оценки связанных с анестезией, интраоперационных и ранних послеоперационных осложнений, мы также документировали оценку боли у пациента и интраоперационные состояния, оцененные хирургом (P.C.J. или F.K.J.), чтобы получить информацию, которая может помочь указать, какой тип анестезии предпочтительнее в сложных случаях хирургии катаракты.
С 1 апреля 1998 г. по 1 июня 1999 г. непрерывная когорта из 1135 глаз 1135 пациентов подходила для операции факоэмульсификации и имплантации складной ИОЛ с местной или ретробульбарной анестезией в любом из двух участвующих университетских глазных центров.Пациенты были проспективно распределены в группу местной или ретробульбарной анестезии с использованием таблицы случайных чисел. Все пациенты, включенные в исследование, имели как минимум 1 из следующих глазных сопутствующих заболеваний: эксфолиативный синдром, увеит, аксиальную миопию (≥26 мм), аксиальную дальнозоркость (≤21,0 мм), недостаточное расширение зрачка (≤3 мм), задние синехии, факодонез или предшествующие внутриглазные операции (периферическая иридэктомия, фильтрующая хирургия глаукомы, кератопластика или витрэктомия плоской части глаза). Пациентов исключали из исследования, если у них в анамнезе были аллергические реакции на гидрохлорид лидокаина или другие местные анестетики, нарушения слуха, деменция, нарушение движения глаз или чрезмерное беспокойство; имел плохую фиксацию из-за нистагма или косоглазия; или не были носителями языка, используемого в операционной.Другие противопоказания к участию в исследовании включали сложные патологические особенности переднего сегмента, которые могли препятствовать правильной визуализации передней камеры во время операции или могли вызвать проблемы, влияющие на подготовку четкого туннеля роговицы, такие как обширное помутнение роговицы в результате сфероидной дегенерации или маргинальное истончение роговицы. продуцируется маргинальной дегенерацией Терриена. Перед операцией было получено информированное согласие.
Пациентов исключали из исследования, если у них в анамнезе были аллергические реакции на гидрохлорид лидокаина или другие местные анестетики, нарушения слуха, деменция, нарушение движения глаз или чрезмерное беспокойство; имел плохую фиксацию из-за нистагма или косоглазия; или не были носителями языка, используемого в операционной.Другие противопоказания к участию в исследовании включали сложные патологические особенности переднего сегмента, которые могли препятствовать правильной визуализации передней камеры во время операции или могли вызвать проблемы, влияющие на подготовку четкого туннеля роговицы, такие как обширное помутнение роговицы в результате сфероидной дегенерации или маргинальное истончение роговицы. продуцируется маргинальной дегенерацией Терриена. Перед операцией было получено информированное согласие.
Администрация анестезии
Пациенты в группе ретробульбарной анестезии получили пероральную седацию 5. От 1 до 10,2 мг мидазолама гидромалеата (Dormicum; Hoffmann-La Roche AG, Гренцах, Германия) за 30 минут до однократной инъекции раствора 0,5% бупивакаина гидрохлорида, 2% лидокаина и 0,5 мл гиалуронидазы (видазы), 3,75 МЕ /мл в ретробульбарное пространство. Объем блока составлял от 3,5 до 5,5 мл в зависимости от массы тела пациента. Окулярная компрессия в течение 10 минут была достигнута с использованием модифицированного баллона Honan. Перед операцией эффективность блока оценивал хирург (П.C.J. или F.K.J.) и считались удовлетворительными, только если сохранялась минимальная подвижность глаз или круговая функция.
От 1 до 10,2 мг мидазолама гидромалеата (Dormicum; Hoffmann-La Roche AG, Гренцах, Германия) за 30 минут до однократной инъекции раствора 0,5% бупивакаина гидрохлорида, 2% лидокаина и 0,5 мл гиалуронидазы (видазы), 3,75 МЕ /мл в ретробульбарное пространство. Объем блока составлял от 3,5 до 5,5 мл в зависимости от массы тела пациента. Окулярная компрессия в течение 10 минут была достигнута с использованием модифицированного баллона Honan. Перед операцией эффективность блока оценивал хирург (П.C.J. или F.K.J.) и считались удовлетворительными, только если сохранялась минимальная подвижность глаз или круговая функция.
Пациенты в группе местной анестезии получили минимум 5 доз (примерно 40 мкл на дозу) 2% лидокаина для местного применения. Четыре дозы вводили в верхнюю и нижнюю слепые мешочки за 10 и 5 минут до операции, перед наложением салфеток и непосредственно перед первоначальным разрезом роговицы. Последняя доза вводилась до начала факоэмульсификации.Протокол, установленный для прорывной боли, допускал дополнительные 80 мкл 2% лидокаина и 40 мкл кокаина. Если это не было эффективным в течение 2 минут, пациенту делали субконъюнктивальную инъекцию 0,75% бупивакаина. Прорывная боль устранялась таким же образом в группе ретробульбарной анестезии.
Если это не было эффективным в течение 2 минут, пациенту делали субконъюнктивальную инъекцию 0,75% бупивакаина. Прорывная боль устранялась таким же образом в группе ретробульбарной анестезии.
Все хирургические процедуры были выполнены в 1 из 2 университетских глазных центров 1 из 2 хирургов (P.C.J. или F.K.J.), которые выполняли операции по удалению катаракты под местной анестезией с 1995 года, используя стандартизированную технику факоэмульсификации прозрачной роговицы. Всем пациентам была проведена временная факоэмульсификация чистой роговицы и имплантация складной ИОЛ. Был сделан височный разрез роговицы с использованием трехэтапного разреза, в то время как глазное яблоко было иммобилизовано кольцом Thornton-Fine. За этим последовал парацентез двух боковых портов, каждый на 90° от височного меридиана, чтобы можно было проводить последующие процедуры. Они включали вискоэластическую инъекцию, непрерывный криволинейный капсулорексис, гидродиссекцию, гидроделинеацию, эндокапсулярную факоэмульсификацию, бимануальную аспирацию оставшегося кортикального материала хрусталика и, наконец, имплантацию складной ИОЛ в мешок. При необходимости зрачок расширяли сфинктеротомией или крючками для ретракции радужной оболочки. После имплантации ИОЛ и удаления вязкоупругого вещества зрачок сужали внутрикамерным введением 0,01% карбахола (Миостат; Alcon Surgical, Форт-Уэрт, Техас). Рану проверяли на утечку жидкости путем легкого сжатия губкой, и ни одному из пациентов не потребовалось наложение швов для закрытия раны. Все пациенты получали идентичный местный режим в послеоперационном периоде, включая 50 мг мезлоциллина (Байпен; Байер, Леверкузен, Германия) и 2 мг ацетата дексаметазона (Фортекортин; Мерк, Кельн, Германия), которые вводили субконъюнктивально сразу после операции.Во время послеоперационного восстановления каждый пациент получал топические кортикостероидные капли и комбинацию кортикостероида и мази с антибиотиком на ночь, дозу быстро снижали в зависимости от степени послеоперационного воспаления.
При необходимости зрачок расширяли сфинктеротомией или крючками для ретракции радужной оболочки. После имплантации ИОЛ и удаления вязкоупругого вещества зрачок сужали внутрикамерным введением 0,01% карбахола (Миостат; Alcon Surgical, Форт-Уэрт, Техас). Рану проверяли на утечку жидкости путем легкого сжатия губкой, и ни одному из пациентов не потребовалось наложение швов для закрытия раны. Все пациенты получали идентичный местный режим в послеоперационном периоде, включая 50 мг мезлоциллина (Байпен; Байер, Леверкузен, Германия) и 2 мг ацетата дексаметазона (Фортекортин; Мерк, Кельн, Германия), которые вводили субконъюнктивально сразу после операции.Во время послеоперационного восстановления каждый пациент получал топические кортикостероидные капли и комбинацию кортикостероида и мази с антибиотиком на ночь, дозу быстро снижали в зависимости от степени послеоперационного воспаления.
По завершении операции каждому пациенту показывали визуальную аналоговую шкалу боли с числовыми и описательными оценками от 0 (отсутствие боли) до 10 (сильная боль), как описано Стивеном. 15 Пациентов просили использовать эту 10-балльную шкалу для оценки уровня боли, ощущаемой во время операции, включая боль, ощущаемую после проведения местной или ретробульбарной анестезии.Если пациенты не могли прочитать напечатанные цифры и описательный текст на шкале боли, врач (TSD) читал их пациенту. Кроме того, записывалось любое словесное выражение боли, которое пациенты делали во время операции (например, при манипуляциях с радужной оболочкой). Хирурга (P.C.J. или F.K.J.) также попросили сообщить о возникших трудностях, связанных с условиями операции. Варианты ответа хирурга: «без затруднений»,
«слегка трудный», «умеренно сложный», «трудный» и «чрезвычайно сложный».» Хирурга попросили заполнить форму сразу после операции.
15 Пациентов просили использовать эту 10-балльную шкалу для оценки уровня боли, ощущаемой во время операции, включая боль, ощущаемую после проведения местной или ретробульбарной анестезии.Если пациенты не могли прочитать напечатанные цифры и описательный текст на шкале боли, врач (TSD) читал их пациенту. Кроме того, записывалось любое словесное выражение боли, которое пациенты делали во время операции (например, при манипуляциях с радужной оболочкой). Хирурга (P.C.J. или F.K.J.) также попросили сообщить о возникших трудностях, связанных с условиями операции. Варианты ответа хирурга: «без затруднений»,
«слегка трудный», «умеренно сложный», «трудный» и «чрезвычайно сложный».» Хирурга попросили заполнить форму сразу после операции.
Критерием исхода было количество осложнений и нежелательных явлений, возникших периоперационно, интраоперационно и в течение 24 часов после операции; оценки боли у пациентов; и интраоперационные условия по оценке хирурга. Кроме того, после завершения процедуры пациентов спрашивали, будет ли применяемый тип анестезии предпочтительным для них в случае дальнейших операций на глазах.
Кроме того, после завершения процедуры пациентов спрашивали, будет ли применяемый тип анестезии предпочтительным для них в случае дальнейших операций на глазах.
Показатели результатов сравнивались с использованием непарного теста t . Показатели боли для каждой группы сравнивали с использованием двустороннего критерия Манна-Уитни для непараметрической статистики. Двумерный анализ проводили с использованием теста χ 2 .
Из 512 пациентов, перенесших первую операцию по удалению катаракты глаза в 2 участвующих центрах, 476 соответствовали критериям включения и согласились участвовать в этом рандомизированном проспективном исследовании.Средний возраст + SD всех пациентов составил 72,7 ± 6,3 года (диапазон от 45 до 91 года), 63% из них были женщинами (таблица 1). Двести тридцать восемь глаз были рандомизированы в группу местной анестезии, а 238 — в группу ретробульбарной анестезии. Различия между 2 исследуемыми группами по возрасту и полу не были статистически значимыми ( P = 0,31). Предоперационные потенциальные факторы риска для факоэмульсификации и имплантации ИОЛ представлены в таблице 2. Статистических различий между двумя исследуемыми группами не было.
Различия между 2 исследуемыми группами по возрасту и полу не были статистически значимыми ( P = 0,31). Предоперационные потенциальные факторы риска для факоэмульсификации и имплантации ИОЛ представлены в таблице 2. Статистических различий между двумя исследуемыми группами не было.
Осложнения были разделены на связанные с анестезией, интраоперационные и осложнения в течение 24 часов после операции (табл. 3). Осложнения, связанные с анестезией, значительно различались между двумя группами. Ни одному пациенту не потребовалось изменение типа анестезии для завершения операции по удалению катаракты. Связанные с анестезией хемоз, периорбитальная гематома и субконъюнктивальное кровоизлияние встречались только в группе ретробульбарной анестезии и никогда не приводили к полной отмене или существенной отсрочке запланированного оперативного вмешательства.
Помимо потери стекловидного тела, которая значительно чаще встречалась в группе ретробульбарной анестезии, частота других интраоперационных осложнений существенно не различалась между 2 исследуемыми группами. При рассмотрении всех 476 глаз наиболее частым осложнением был зональный разрыв, за которым следовали разрыв капсулы и потеря стекловидного тела. Имплантация гаптики в борозды с оптическим захватом или без него через капсулорексис потребовалась у 6 пациентов: 2 в группе местной анестезии и 4 в группе ретробульбарной анестезии.Причины имплантации бороздчатой ИОЛ включали ожидаемую слабость связочного аппарата или слезотечение в 3 глазах, недопустимо малый передний капсулорексис с суженным зрачком в 1 и разрыв капсулы с передней витрэктомией в 2. У 2 пациентов с обширными дефектами связочного аппарата и серьезным ухудшением общего состояния, переднекамерная ИОЛ была предпочтительнее вторичной ИОЛ с швом борозды. Интраоперационный выпадение радужной оболочки в туннельный разрез произошло на 4 глазах в группе местной анестезии и на 1 глазе в группе ретробульбарной анестезии.
При рассмотрении всех 476 глаз наиболее частым осложнением был зональный разрыв, за которым следовали разрыв капсулы и потеря стекловидного тела. Имплантация гаптики в борозды с оптическим захватом или без него через капсулорексис потребовалась у 6 пациентов: 2 в группе местной анестезии и 4 в группе ретробульбарной анестезии.Причины имплантации бороздчатой ИОЛ включали ожидаемую слабость связочного аппарата или слезотечение в 3 глазах, недопустимо малый передний капсулорексис с суженным зрачком в 1 и разрыв капсулы с передней витрэктомией в 2. У 2 пациентов с обширными дефектами связочного аппарата и серьезным ухудшением общего состояния, переднекамерная ИОЛ была предпочтительнее вторичной ИОЛ с швом борозды. Интраоперационный выпадение радужной оболочки в туннельный разрез произошло на 4 глазах в группе местной анестезии и на 1 глазе в группе ретробульбарной анестезии.
В первые 24 часа ни в одной из 2 исследуемых групп не наблюдалось тяжелых осложнений. Преходящее повышение давления на 30 мм рт. ст. встречалось наиболее часто, но не потребовало повторного хирургического вмешательства ни у одного пациента. Фибринозная водянистая реакция была вторым наиболее частым осложнением, но успешно лечилась интенсивным местным применением кортикостероидов у каждого пациента. Отек роговицы, приводящий к временной потере максимально корригированной остроты зрения, наблюдался на 6 глазах в каждой из 2 групп.Задержка коркового вещества наблюдалась у 3 пациентов с суженными зрачками. Во всех случаях материал хрусталика в конечном итоге рассасывался спонтанно при повторном хирургическом вмешательстве. У одного пациента, перенесшего витрэктомию pars plana, развилась временная несостоятельность раны через 1 из 2 боковых разрезов.
ст. встречалось наиболее часто, но не потребовало повторного хирургического вмешательства ни у одного пациента. Фибринозная водянистая реакция была вторым наиболее частым осложнением, но успешно лечилась интенсивным местным применением кортикостероидов у каждого пациента. Отек роговицы, приводящий к временной потере максимально корригированной остроты зрения, наблюдался на 6 глазах в каждой из 2 групп.Задержка коркового вещества наблюдалась у 3 пациентов с суженными зрачками. Во всех случаях материал хрусталика в конечном итоге рассасывался спонтанно при повторном хирургическом вмешательстве. У одного пациента, перенесшего витрэктомию pars plana, развилась временная несостоятельность раны через 1 из 2 боковых разрезов.
Несмотря на некоторые очевидные тенденции (таблица 4), наблюдаемые осложнения и предоперационные факторы риска не могли быть коррелированы или подвергнуты статистическому анализу, поскольку количество смешанных переменных давало недостаточное количество для каждой категории в таблицах сопряженности, а несколько пациентов с осложнениями были вне диапазона приемлемости для обычных статистических тестов.
Баллы боли, о которых сообщили пациенты после операции, показаны на рисунке 1. Двести два пациента (85%) в группе местной анестезии и 219 (92%) в группе ретробульбарной анестезии сообщили о минимальном дискомфорте (максимальная оценка 2). или отсутствие боли (0 баллов). Среднее значение оценки боли + SD в группе местной анестезии составило 0,84 + 1,30 (диапазон 0–7), а в группе ретробульбарной анестезии — 0,73 + 1,50 (диапазон 0–5). Разница между средними показателями боли не была статистически значимой ( P = .41). О беспокойстве перед введением анестезии сообщалось у 55 пациентов (23%) в ретробульбарной группе; ни один из тех, кто должен был получить местную анестезию, не сообщил о беспокойстве. Во время применения анестезии примерно 17% в ретробульбарной группе выражали дискомфорт (балл боли ≥4), в то время как только 2% в группе местного применения сообщили об усилении жжения в глазу (балл боли ≥2). Во время операции манипулирование радужной оболочкой, расширение передней камеры, внутрикамерное введение ацетилхолина хлорида и вращение ИОЛ чаще всего приводили к вербализации пациентом дискомфорта. Предпочтения пациентов в отношении местной или ретробульбарной анестезии различались между двумя группами. В группе местной анестезии только 9% пациентов сказали, что они выбрали бы другой тип анестезии (ретробульбарную или общую анестезию) для второго глаза, в то время как 23% пациентов в группе ретробульбарной анестезии предпочли бы местную анестезию. или общая анестезия ( P = .01).
Предпочтения пациентов в отношении местной или ретробульбарной анестезии различались между двумя группами. В группе местной анестезии только 9% пациентов сказали, что они выбрали бы другой тип анестезии (ретробульбарную или общую анестезию) для второго глаза, в то время как 23% пациентов в группе ретробульбарной анестезии предпочли бы местную анестезию. или общая анестезия ( P = .01).
Интраоперационные условия по оценке хирурга показаны в таблице 5.У большинства пациентов в обеих группах хирург сообщил об отсутствии затруднений или незначительных затруднениях.
Методы бесшовного разреза прозрачной роговицы завоевали популярность среди катарактальных хирургов благодаря многим преимуществам, которые они предлагают, включая сокращение манипуляций с тканями глаза и времени операции. 16 Только местная анестезия позволяет избежать потенциально серьезных осложнений, связанных с ретробульбарной и перибульбарной анестезией. 1 -4 С момента своего появления местная анестезия становится все более популярной, о чем свидетельствует ежегодный обзор стилей практики и предпочтений членов Американского общества катарактальной и рефракционной хирургии. 17 По данным прошлогоднего исследования, использование местной анестезии увеличилось с 8% в 1995 г. до 14% в 1996 г. и до 37% в 1998 г. Однако ее использование варьировалось в зависимости от объема операции, увеличиваясь на 22% для хирургов, проводящих от 0 до 5 процедур по удалению катаракты в месяц и на 63% для тех, кто делает более 51 операции, причем последний показатель увеличился с 40% в 1996 году.
1 -4 С момента своего появления местная анестезия становится все более популярной, о чем свидетельствует ежегодный обзор стилей практики и предпочтений членов Американского общества катарактальной и рефракционной хирургии. 17 По данным прошлогоднего исследования, использование местной анестезии увеличилось с 8% в 1995 г. до 14% в 1996 г. и до 37% в 1998 г. Однако ее использование варьировалось в зависимости от объема операции, увеличиваясь на 22% для хирургов, проводящих от 0 до 5 процедур по удалению катаракты в месяц и на 63% для тех, кто делает более 51 операции, причем последний показатель увеличился с 40% в 1996 году.
С другой стороны, местная анестезия при определенных обстоятельствах может быть более сложной для хирурга и, по-видимому, особенно трудна для пациентов, требующих большего количества внутриглазных манипуляций, чем обычно, например, у пациентов с маленьким зрачком. Однако цель должна заключаться в том, чтобы позволить более широкому кругу пациентов пользоваться преимуществами местной анестезии. Настоящее исследование, сравнивающее местную анестезию с ретробульбарной инъекционной анестезией в потенциально сложных случаях хирургии катаракты, убедительно показывает, что местная анестезия может обеспечить безопасные условия операции даже в более сложных условиях без какого-либо заметного снижения комфорта пациента.
Настоящее исследование, сравнивающее местную анестезию с ретробульбарной инъекционной анестезией в потенциально сложных случаях хирургии катаракты, убедительно показывает, что местная анестезия может обеспечить безопасные условия операции даже в более сложных условиях без какого-либо заметного снижения комфорта пациента.
Наши данные, показывающие 1,5% разрыва капсулы с потерей стекловидного тела и 1,9% разрыва капсулы без потери стекловидного тела, находятся в пределах диапазона уровней осложнений, зарегистрированных в других сериях 18 -24 невыбранных случаев. В настоящем исследовании частота только разрыва капсулы существенно не отличалась между двумя группами анестезии, в то время как частота потери стекловидного тела была значительно выше в группе ретробульбарной инъекции. Тем не менее, не было существенной разницы в отношении других осложнений, возникающих во время операции или в течение 24 часов после операции между двумя группами.Статистический анализ частоты осложнений, наблюдаемых в связи с предшествующими сопутствующими глазными заболеваниями, не выявил существенных различий, вероятно, из-за относительной редкости таких нежелательных явлений (табл. 4). Тем не менее эксфолиативный синдром, особенно связанный с меньшими зрачками, по-видимому, увеличивает риск разрыва задней капсулы. В то время как предыдущая внутриглазная операция сопровождалась разрывом капсулы только в 2 случаях, разрывы связочного слоя были наиболее частыми осложнениями на этих глазах.Частота интраоперационных осложнений и проблем в раннем послеоперационном периоде, а также их корреляция с потенциальными факторами риска в целом сопоставимы с таковыми в других исследованиях. 18 -24
4). Тем не менее эксфолиативный синдром, особенно связанный с меньшими зрачками, по-видимому, увеличивает риск разрыва задней капсулы. В то время как предыдущая внутриглазная операция сопровождалась разрывом капсулы только в 2 случаях, разрывы связочного слоя были наиболее частыми осложнениями на этих глазах.Частота интраоперационных осложнений и проблем в раннем послеоперационном периоде, а также их корреляция с потенциальными факторами риска в целом сопоставимы с таковыми в других исследованиях. 18 -24
Интраоперационное выпадение радужной оболочки наблюдалось в 1% случаев в обеих группах. Хотя это и не является статистически значимым, пролапс радужки чаще возникал в группе местной анестезии (1,7%), чем в группе ретробульбарной анестезии (0,4%). Выпадение радужной оболочки чаще всего происходит в глазах с интраоперационно повышенным внутриглазным давлением, особенно в глазах с дальнозоркостью или нанофтальмом, но также возникает у тревожных пациентов с более высокой вероятностью сокращения экстраокулярных мышц. В то время как распределение измерений осевой длины глаза было одинаковым в 2 исследуемых группах, экстраокулярное сокращение мышц, вероятно, происходит только в группе местной анестезии без моторной блокады, что может объяснить наблюдаемые межгрупповые различия для этого осложнения. Более того, у пациентов, получавших ретробульбарную анестезию, окулопрессию выполняли рутинно, чтобы противодействовать возможному повышению давления во время операции, но эту предоперационную меру нельзя использовать у пациентов, получающих местную анестезию.Транзиторные послеоперационные осложнения, такие как отек роговицы, несостоятельность раны, повышение внутриглазного давления и плазмоидная или фибринозная реакция передней камеры, были одинаковыми в 2 группах и, несмотря на то, что это исследование было серией отобранных пациентов с высоким риском, были менее выражены. чаще, чем в других исследованиях. 18 -24 Осложнения, связанные с анестезией, преобладали, как и ожидалось, в ретробульбарной группе.
В то время как распределение измерений осевой длины глаза было одинаковым в 2 исследуемых группах, экстраокулярное сокращение мышц, вероятно, происходит только в группе местной анестезии без моторной блокады, что может объяснить наблюдаемые межгрупповые различия для этого осложнения. Более того, у пациентов, получавших ретробульбарную анестезию, окулопрессию выполняли рутинно, чтобы противодействовать возможному повышению давления во время операции, но эту предоперационную меру нельзя использовать у пациентов, получающих местную анестезию.Транзиторные послеоперационные осложнения, такие как отек роговицы, несостоятельность раны, повышение внутриглазного давления и плазмоидная или фибринозная реакция передней камеры, были одинаковыми в 2 группах и, несмотря на то, что это исследование было серией отобранных пациентов с высоким риском, были менее выражены. чаще, чем в других исследованиях. 18 -24 Осложнения, связанные с анестезией, преобладали, как и ожидалось, в ретробульбарной группе. Хемоз, субконъюнктивальное кровоизлияние и периорбитальная гематома наблюдались исключительно в группе ретробульбарной анестезии.Но эти нежелательные явления не представляли существенной клинической проблемы, поскольку ни у одного пациента запланированное хирургическое вмешательство не было предотвращено или отсрочено.
Хемоз, субконъюнктивальное кровоизлияние и периорбитальная гематома наблюдались исключительно в группе ретробульбарной анестезии.Но эти нежелательные явления не представляли существенной клинической проблемы, поскольку ни у одного пациента запланированное хирургическое вмешательство не было предотвращено или отсрочено.
В первую очередь нас интересовала возможная потребность в дополнительной параокулярной анестезии в группе с местной анестезией. Предыдущие исследования 9 -11,14 показали, что усиление манипуляций с радужной оболочкой и растяжение тканей сосудистой оболочки, неизбежные во время операции в сложных случаях, раздражают пациентов, находящихся под местной анестезией, которым могут потребоваться дополнительные анестезиологические мероприятия.Однако между нашими исследовательскими группами мы не наблюдали каких-либо статистически значимых различий в отношении дополнительной параокулярной инъекции анестетика. Аналогичным образом, показатели боли, о которых сообщали пациенты сразу после завершения операции, существенно не отличались между группами. Подобного сходства между средними показателями боли в двух исследуемых группах не наблюдалось ни в одном из предыдущих исследований. 5 ,7 ,8,14 ,25 Аномалия еще более сбивает с толку, поскольку мы не использовали, как утверждают другие, 9 -14,25
Подобного сходства между средними показателями боли в двух исследуемых группах не наблюдалось ни в одном из предыдущих исследований. 5 ,7 ,8,14 ,25 Аномалия еще более сбивает с толку, поскольку мы не использовали, как утверждают другие, 9 -14,25
3 -48 дополнительное внутрикамерное использование инъекции неконсервированного лидокаина в нашем исследовании.Действительно, в то время, когда был установлен наш протокол исследования, потенциальные токсические эффекты внутрикамерного применения лидокаина на различные внутриглазные структуры, особенно на эндотелий роговицы и сетчатку, все еще вызывали серьезные опасения в литературе. Помимо инстилляции лидокаина внутрикамерно, были предложены различные другие меры для облегчения дискомфорта пациента, связанного с внутриглазными манипуляциями. К ним относятся «адекватная циклоплегия» для минимизации растяжения связок и цилиарной мышцы
29 или опускание бутылки с раствором для промывания для минимизации внутриглазного гидростатического давления. 30 Однако ни одна из этих мер обычно не применяется в случаях осложненной катаракты. Единственным объяснением отсутствия каких-либо различий между группами анестетиков в отношении комфорта пациента во время факоэмульсификации является то, что перед некоторыми потенциально раздражающими предоперационными или интраоперационными этапами, такими как закапывание анестезирующих глазных капель, ретробульбарная инъекция, манипуляции с радужной оболочкой, гидродиссекция, активация ирригационной линии или имплантации ИОЛ, хирурги регулярно сообщали пациенту, что следующий маневр может быть «чувствуемым или даже слегка болезненным».« Мы считаем этот вербальный контакт с пациентом на протяжении всей хирургической процедуры чрезвычайно полезным, если не решающим, для комфортной и безопасной процедуры катаракты под местной анестезией. Более того, мы считаем, что низкий уровень дискомфорта у наших пациентов, получающих местную анестезию также может быть объяснено скоростью, с которой была выполнена факоэмульсификация, и осторожностью, которую мы проявляли во время внутриглазных манипуляций.
30 Однако ни одна из этих мер обычно не применяется в случаях осложненной катаракты. Единственным объяснением отсутствия каких-либо различий между группами анестетиков в отношении комфорта пациента во время факоэмульсификации является то, что перед некоторыми потенциально раздражающими предоперационными или интраоперационными этапами, такими как закапывание анестезирующих глазных капель, ретробульбарная инъекция, манипуляции с радужной оболочкой, гидродиссекция, активация ирригационной линии или имплантации ИОЛ, хирурги регулярно сообщали пациенту, что следующий маневр может быть «чувствуемым или даже слегка болезненным».« Мы считаем этот вербальный контакт с пациентом на протяжении всей хирургической процедуры чрезвычайно полезным, если не решающим, для комфортной и безопасной процедуры катаракты под местной анестезией. Более того, мы считаем, что низкий уровень дискомфорта у наших пациентов, получающих местную анестезию также может быть объяснено скоростью, с которой была выполнена факоэмульсификация, и осторожностью, которую мы проявляли во время внутриглазных манипуляций. Это предположение было подтверждено нашим наблюдением, что даже в этих хирургически более сложных глазах только 9% из группы местной анестезии сказали, что они предпочли бы другой тип анестезии для второго глаза, в то время как 23% пациентов в группе ретробульбарной анестезии хотели бы другой вид анестезии.
Это предположение было подтверждено нашим наблюдением, что даже в этих хирургически более сложных глазах только 9% из группы местной анестезии сказали, что они предпочли бы другой тип анестезии для второго глаза, в то время как 23% пациентов в группе ретробульбарной анестезии хотели бы другой вид анестезии. Акинезия глазного яблока обычно не достигается при местной анестезии, что делает операцию по удалению катаракты в сложных случаях, возможно, еще более сложной для хирурга. Как и ожидалось, общее хирургическое состояние, оцененное хирургом, благоприятствовало использованию ретробульбарной анестезии. Однако межгрупповая разница в оценке хирурга не была статистически значимой. Эти результаты противоречат результатам аналогичного исследования 7 , сравнивающего местную анестезию с ретробульбарной, но согласуются с результатами Uusitalo et al, 25 , которые обнаружили, что параокулярная инъекция значительно менее сложна.Отсутствие акинезии не было клинически значимым, так как дополнительная параокулярная анестезия не потребовалась ни у одного пациента для продолжения операции. Хирурги неоднократно отмечали, что некоторые пациенты просто не замечали непреднамеренного движения глаз во время операции, а мышечные спазмы считались причиной повышения внутриглазного давления у некоторых пациентов. Во время операции хирурги обнаружили, что минимизация движений глаз во время капсулорексиса является наиболее важной. Фотофобию, причину движения глаз у некоторых пациентов, можно преодолеть, просто уменьшив яркость операционного микроскопа.Было обнаружено, что необходимость затемнения источника света в группе с местной анестезией не усложняет хирургическую процедуру.
Хирурги неоднократно отмечали, что некоторые пациенты просто не замечали непреднамеренного движения глаз во время операции, а мышечные спазмы считались причиной повышения внутриглазного давления у некоторых пациентов. Во время операции хирурги обнаружили, что минимизация движений глаз во время капсулорексиса является наиболее важной. Фотофобию, причину движения глаз у некоторых пациентов, можно преодолеть, просто уменьшив яркость операционного микроскопа.Было обнаружено, что необходимость затемнения источника света в группе с местной анестезией не усложняет хирургическую процедуру.
Таким образом, по сравнению с ретробульбарной анестезией местная анестезия обеспечивает хорошие хирургические условия для хирурга и комфортные операционные условия для пациента, даже в сложных случаях с сопутствующими глазными заболеваниями. Это исследование показывает, что сложную операцию по удалению катаракты можно проводить под местной анестезией без ущерба для безопасности процедуры.В то время как осложнения, связанные с операцией под местной анестезией, были аналогичны осложнениям, возникающим при использовании ретробульбарных инъекций, осложнения, связанные с анестезией, наблюдались исключительно в группе ретробульбарных инъекций. Хотя результаты оценки боли во время проведения анестезии благоприятствовали местной технике, оценки пациентов во время и вскоре после анестезии статистически не различались в группах местной и ретробульбарной анестезии. Тот факт, что хирурги в группе с местной анестезией столкнулись с большими трудностями, связанными с анестезией, при операции по удалению катаракты, позволяет сделать вывод, что в сложных случаях хирургия катаракты предъявляет более высокие требования к хирургу, использующему местную анестезию.Тем не менее, мы считаем, что местная анестезия оправдана для повышения безопасности и комфорта пациента даже в сложных случаях хирургии катаракты и, вероятно, станет предпочтительным типом анестезии при факоэмульсификации с малым разрезом и имплантации складной ИОЛ, особенно при так называемой хирурги большого объема. Предпочтение пациентами местной анестезии неуклонно растет и требует всех усилий по отказу от более инвазивных форм анестезии, чтобы хирургию катаракты можно было действительно назвать «минимально инвазивной».
Хотя результаты оценки боли во время проведения анестезии благоприятствовали местной технике, оценки пациентов во время и вскоре после анестезии статистически не различались в группах местной и ретробульбарной анестезии. Тот факт, что хирурги в группе с местной анестезией столкнулись с большими трудностями, связанными с анестезией, при операции по удалению катаракты, позволяет сделать вывод, что в сложных случаях хирургия катаракты предъявляет более высокие требования к хирургу, использующему местную анестезию.Тем не менее, мы считаем, что местная анестезия оправдана для повышения безопасности и комфорта пациента даже в сложных случаях хирургии катаракты и, вероятно, станет предпочтительным типом анестезии при факоэмульсификации с малым разрезом и имплантации складной ИОЛ, особенно при так называемой хирурги большого объема. Предпочтение пациентами местной анестезии неуклонно растет и требует всех усилий по отказу от более инвазивных форм анестезии, чтобы хирургию катаракты можно было действительно назвать «минимально инвазивной».
Принято к публикации 27 января 2000 г.
Оттиски: Филипп С. Якоби, доктор медицинских наук, кафедра офтальмологии, Кельнский университет, Джозеф-Штельзманнштрассе 9, 50931 Кельн, Германия (электронная почта: [email protected]).
2. Салливан КЛБраун GCForman дополненная реальность и другие. Ретробульбарная анестезия и обструкция сосудов сетчатки. Офтальмология. 1983; J Рефракционная хирургия катаракты. 1997;23277- 283Google ScholarCrossref 6.Fichman
РА Использование только местной анестезии при хирургии катаракты. J Рефракционная хирургия катаракты. 1996;22612- 614Google ScholarCrossref 7.Patel
Э.А.Карлсон
ТАКрандалл
А
и другие. Сравнение местной и ретробульбарной анестезии при хирургии катаракты. Офтальмология. 1996;1031196-1203Google ScholarCrossref 8.Zehetmayer
MRadax
Ускорпик
С
и другие.Местная и ретробульбарная анестезия в хирургии ясной роговичной катаракты. J Рефракционная хирургия катаракты. 1996;22480- 484Google ScholarCrossref 9.Koch
PS Эффективность 2% желе лидокаина в качестве местного средства при хирургии катаракты. J Рефракционная хирургия катаракты.
J Рефракционная хирургия катаракты. 1997;23277- 283Google ScholarCrossref 6.Fichman
РА Использование только местной анестезии при хирургии катаракты. J Рефракционная хирургия катаракты. 1996;22612- 614Google ScholarCrossref 7.Patel
Э.А.Карлсон
ТАКрандалл
А
и другие. Сравнение местной и ретробульбарной анестезии при хирургии катаракты. Офтальмология. 1996;1031196-1203Google ScholarCrossref 8.Zehetmayer
MRadax
Ускорпик
С
и другие.Местная и ретробульбарная анестезия в хирургии ясной роговичной катаракты. J Рефракционная хирургия катаракты. 1996;22480- 484Google ScholarCrossref 9.Koch
PS Эффективность 2% желе лидокаина в качестве местного средства при хирургии катаракты. J Рефракционная хирургия катаракты. 1999;25632- 634Google ScholarCrossref 10.Tseng
Щен
FK Рандомизированное клиническое исследование комбинированной местной и внутрикамерной анестезии при хирургии катаракты. Офтальмология. 1998;1052007– 2011Google ScholarCrossref 12.Жабры
JPCerichio
МРаанан
MG Неконсервированный лидокаин для контроля дискомфорта во время операции по удалению катаракты с использованием местной анестезии. J Рефракционная хирургия катаракты. 1997;23545- 550Google ScholarCrossref 13.Koch
PS Ирригация передней камеры 1% лидокаином без консервантов для анестезии во время операции по удалению катаракты. J Рефракционная хирургия катаракты. 1997;23551- 554Google ScholarCrossref 14.Fukasaku
ХМаррон
JA Точечная анестезия: новый подход к местной глазной анестезии. J Рефракционная хирургия катаракты.
1999;25632- 634Google ScholarCrossref 10.Tseng
Щен
FK Рандомизированное клиническое исследование комбинированной местной и внутрикамерной анестезии при хирургии катаракты. Офтальмология. 1998;1052007– 2011Google ScholarCrossref 12.Жабры
JPCerichio
МРаанан
MG Неконсервированный лидокаин для контроля дискомфорта во время операции по удалению катаракты с использованием местной анестезии. J Рефракционная хирургия катаракты. 1997;23545- 550Google ScholarCrossref 13.Koch
PS Ирригация передней камеры 1% лидокаином без консервантов для анестезии во время операции по удалению катаракты. J Рефракционная хирургия катаракты. 1997;23551- 554Google ScholarCrossref 14.Fukasaku
ХМаррон
JA Точечная анестезия: новый подход к местной глазной анестезии. J Рефракционная хирургия катаракты. 1994;20468- 471Google ScholarCrossref 15.Стивен
JD Новый метод местной анестезии для экстракции катаракты путем субтеноновой инфильтрации в одном квадранте. Br J Офтальмол. 1992;76670- 674Google ScholarCrossref 16.Kershner
RM Анатомия роговицы и бесконтактная техника. Отлично
И.Х.Фичман
RAGrabow
кровати Хирургия катаракты с разрезом прозрачной роговицы и местная анестезия. Thorofare, NJ SLACK Inc1993;79-84Google Scholar17.обучение
DV Практические стили и предпочтения членов ASCRS: опрос 1998 года. J Рефракционная хирургия катаракты. 1999;25851- 859Google Scholar18.Norregaard
JCBernth-Petersen
Пбеллан
л
и другие. Интраоперационная клиническая практика и риск ранних осложнений после экстракции катаракты в США, Канаде, Дании и Испании. Офтальмология.
1994;20468- 471Google ScholarCrossref 15.Стивен
JD Новый метод местной анестезии для экстракции катаракты путем субтеноновой инфильтрации в одном квадранте. Br J Офтальмол. 1992;76670- 674Google ScholarCrossref 16.Kershner
RM Анатомия роговицы и бесконтактная техника. Отлично
И.Х.Фичман
RAGrabow
кровати Хирургия катаракты с разрезом прозрачной роговицы и местная анестезия. Thorofare, NJ SLACK Inc1993;79-84Google Scholar17.обучение
DV Практические стили и предпочтения членов ASCRS: опрос 1998 года. J Рефракционная хирургия катаракты. 1999;25851- 859Google Scholar18.Norregaard
JCBernth-Petersen
Пбеллан
л
и другие. Интраоперационная клиническая практика и риск ранних осложнений после экстракции катаракты в США, Канаде, Дании и Испании. Офтальмология. 1999;10642- 48Google ScholarCrossref 19.Willerscheidt
АБХили
MLIИрландия
M Исходы операции по удалению катаракты: важность сопутствующих заболеваний в сочетании случаев. J Рефракционная хирургия катаракты. 1995;21177- 181Google ScholarCrossref 20.Голландия
GNEarl
DTWheeler
Северная Каролина
и другие. Результаты стационарной и амбулаторной хирургии катаракты: историческое когортное сравнение. Офтальмология. 1992;99845-852Google ScholarCrossref 22.Nishi
O Потеря стекловидного тела при имплантации линзы в заднюю камеру. J Рефракционная хирургия катаракты. 1987;13424- 427Google ScholarCrossref 23.Chambles
WS Частота осложнений переднего и заднего сегмента в более чем 3000 случаях экстракапсулярной экстракции катаракты: интактные и открытые капсулы. Внутриглазной имплантат J Am Soc.
1999;10642- 48Google ScholarCrossref 19.Willerscheidt
АБХили
MLIИрландия
M Исходы операции по удалению катаракты: важность сопутствующих заболеваний в сочетании случаев. J Рефракционная хирургия катаракты. 1995;21177- 181Google ScholarCrossref 20.Голландия
GNEarl
DTWheeler
Северная Каролина
и другие. Результаты стационарной и амбулаторной хирургии катаракты: историческое когортное сравнение. Офтальмология. 1992;99845-852Google ScholarCrossref 22.Nishi
O Потеря стекловидного тела при имплантации линзы в заднюю камеру. J Рефракционная хирургия катаракты. 1987;13424- 427Google ScholarCrossref 23.Chambles
WS Частота осложнений переднего и заднего сегмента в более чем 3000 случаях экстракапсулярной экстракции катаракты: интактные и открытые капсулы. Внутриглазной имплантат J Am Soc. 1985;11146- 148Google ScholarCrossref 24.Chitkara
ДКСмердон
DL Факторы риска, осложнения и результаты экстракапсулярной экстракции катаракты. J Рефракционная хирургия катаракты. 1997;23570- 574Google ScholarCrossref 25.Uusitalo
RJMaunuksela
ELPaloheimo
М
и другие. Переход на местную анестезию при хирургии катаракты. J Рефракционная хирургия катаракты. 1999;25432- 440Google ScholarCrossref 26.Crandall
А.С.Забриски
Н.А.Патель
БСК
и другие.Сравнение комфорта пациента во время операции по удалению катаракты с местной анестезией по сравнению с местной анестезией и внутрикамерным введением лидокаина. Офтальмология. 1999;10660- 66Google ScholarCrossref 27.Garcia
АЛурейро
Флимао
Асампайо
Ильхарко
J Промывание передней камеры 1% раствором лидокаина без консервантов в качестве дополнения к местной анестезии.
1985;11146- 148Google ScholarCrossref 24.Chitkara
ДКСмердон
DL Факторы риска, осложнения и результаты экстракапсулярной экстракции катаракты. J Рефракционная хирургия катаракты. 1997;23570- 574Google ScholarCrossref 25.Uusitalo
RJMaunuksela
ELPaloheimo
М
и другие. Переход на местную анестезию при хирургии катаракты. J Рефракционная хирургия катаракты. 1999;25432- 440Google ScholarCrossref 26.Crandall
А.С.Забриски
Н.А.Патель
БСК
и другие.Сравнение комфорта пациента во время операции по удалению катаракты с местной анестезией по сравнению с местной анестезией и внутрикамерным введением лидокаина. Офтальмология. 1999;10660- 66Google ScholarCrossref 27.Garcia
АЛурейро
Флимао
Асампайо
Ильхарко
J Промывание передней камеры 1% раствором лидокаина без консервантов в качестве дополнения к местной анестезии. J Рефракционная хирургия катаракты. 1998;24403- 406Google ScholarCrossref 28.Belluccis
Р.Морселли
Спуччи
В
и другие.Внутриглазное проникновение местного лидокаина 4%. J Рефракционная хирургия катаракты. 1999;25643- 647Google ScholarCrossref 30.Novak
КДКоч
DD Местная анестезия для факоэмульсификации: начальная серия из 20 случаев с последующим наблюдением в течение одного месяца. J Рефракционная хирургия катаракты. 1995;21672- 675Google ScholarCrossref
J Рефракционная хирургия катаракты. 1998;24403- 406Google ScholarCrossref 28.Belluccis
Р.Морселли
Спуччи
В
и другие.Внутриглазное проникновение местного лидокаина 4%. J Рефракционная хирургия катаракты. 1999;25643- 647Google ScholarCrossref 30.Novak
КДКоч
DD Местная анестезия для факоэмульсификации: начальная серия из 20 случаев с последующим наблюдением в течение одного месяца. J Рефракционная хирургия катаракты. 1995;21672- 675Google ScholarCrossrefТрабекулэктомия после операции: не сбиться с пути
Трабекулэктомии были золотым стандартом лечения глаукомы на протяжении многих лет.До сих пор они по-прежнему являются нашим лучшим способом достижения очень низкого внутриглазного давления в глаукоматозном глазу. Однако операция связана с многочисленными потенциальными осложнениями. Вот почему, когда дело доходит до трабекулэктомии, последующее наблюдение является сложной частью.
Вот почему, когда дело доходит до трабекулэктомии, последующее наблюдение является сложной частью. Имея это в виду, я хотел бы поделиться своим многолетним послеоперационным опытом с тысячами этих пациентов в надежде, что кое-что из того, что я узнал, может помочь другим хирургам и пациентам достичь наилучших возможных результатов.
Последующее наблюдение (когда все хорошо)
После завершения самой трабекулэктомии я обычно осматриваю пациента на следующий день, а затем через неделю для подгонки съемных швов. После этого, в зависимости от ВГД, я приду к пациенту либо через одну, либо через две недели, потому что к трем неделям — за исключением гипотонической ситуации — все конъюнктивальные и съемные швы обычно снимаются.
Я стремлюсь поддерживать ВГД на уровне 15–20 мм рт. ст. в первый день после операции; это позволяет зрению вернуться к норме (или близкой к норме), чтобы пациент мог возобновить повседневную деятельность. В большинстве случаев давление слегка повышено по отношению к цели, что идеально в этот момент, потому что мы хотим избежать гипотонии. В зависимости от моего целевого давления съемный шов можно нарезать уже в первый день или в течение первых трех недель. (Моей целью обычно является снижение ВГД на 50 процентов.)
В большинстве случаев давление слегка повышено по отношению к цели, что идеально в этот момент, потому что мы хотим избежать гипотонии. В зависимости от моего целевого давления съемный шов можно нарезать уже в первый день или в течение первых трех недель. (Моей целью обычно является снижение ВГД на 50 процентов.)
Снятие швов производится на щелевой лампе с помощью иглы или лезвия и ювелирных щипцов. Иногда, если давление повышено, я использую лазер с линзой Блюменталя или Хоскинса, чтобы разрезать внутренние швы.Тем не менее, я обычно оставляю лазер на более поздний послеоперационный период, потому что в большинстве случаев давление можно контролировать, сняв один съемный шов; поток немедленно увеличивается, и ВГД снижается.
Я обычно держу пациента в каплях антибиотика в течение недели, а также стероиды четыре раза в день. в течение двух недель, т.и.д. в течение двух недель, два раза в день в течение двух недель и один раз в день в течение двух недель перед остановкой. Я также прописываю НПВП один раз в день в течение как минимум шести недель. (Примечание: я не назначаю НПВП вместе со стероидом, если в глазу много аномалий эпителия роговицы.)
Я также прописываю НПВП один раз в день в течение как минимум шести недель. (Примечание: я не назначаю НПВП вместе со стероидом, если в глазу много аномалий эпителия роговицы.)
| ||||||||||
Одна из причин, по которой я продолжаю принимать НПВП в течение такого периода времени, заключается в том, что я считаю, что низкие уровни воспаления, приводящие к рубцеванию, являются серьезной причиной неудач трабекулэктомии.
 Это то, что может быть нелегко заметить при щелевой лампе, но НПВП поможет предотвратить или облегчить это. Мы также рекомендуем пациенту использовать слезы, чтобы глазу было комфортно.
Это то, что может быть нелегко заметить при щелевой лампе, но НПВП поможет предотвратить или облегчить это. Мы также рекомендуем пациенту использовать слезы, чтобы глазу было комфортно.Если через три недели все будет хорошо, я снова приду к пациенту через месяц, или он вернется к направившему врачу. Если не все хорошо, то я вижу пациента так часто, как это необходимо.
Послеоперационный осмотр
Когда вы осматриваете пациента в первый день после операции, очень важно быть внимательным наблюдателем, потому что нет другого способа убедиться, что все в порядке.Например, если зрение пациента в первый послеоперационный день идеальное, это обычно означает, что давление недостаточно низкое. С другой стороны, размытое зрение может означать несколько разных вещей. Возможно, давление слишком низкое или находится на ожидаемом уровне, а может быть, даже слишком высокое из-за отека роговицы или из-за того, что кровь блокирует костную кость, вызывая повышение давления. Вот почему очень важно тщательно проверить роговицу, глубину передней камеры, степень воспаления и субконъюнктивального кровоизлияния, а также количество крови возле верхнего лоскута.
Вот почему очень важно тщательно проверить роговицу, глубину передней камеры, степень воспаления и субконъюнктивального кровоизлияния, а также количество крови возле верхнего лоскута.
|

Признаки, на которые следует обращать внимание в первый день после операции, включают отек роговицы, указывающий на слишком высокое давление, и складки эндотелия, указывающие на слишком низкое давление. Последнее обычно связано с мелированием передней камеры.
Управление мелкой камерой
Мелкость передней камеры часто возникает, когда ВГД меняется с высокого на низкий. Одновременно вы можете увидеть развитие отслойки сосудистой оболочки, жидкость в супрахориоидальном пространстве, которая толкает хрусталиково-радужную диафрагму вперед и еще больше уплощает камеру.Это порочный круг, потому что одно подпитывает другое.
Неглубокая передняя камера требует различных уровней реагирования в зависимости от степени тяжести. Тяжесть оценивается по четырем уровням: степень 0 означает, что камера неглубокая, но эндотелий не касается других тканей, даже на периферии; 1-я степень предполагает наличие периферического соприкосновения, но камера все еще сформирована в других местах. Если камера находится между классами 0 и 1, мы просто внимательно наблюдаем за пациентом, посещая его через неделю и каждую последующую неделю.
Если камера находится между классами 0 и 1, мы просто внимательно наблюдаем за пациентом, посещая его через неделю и каждую последующую неделю.
Степень 2 подразумевает, что эндотелий касается средней части радужной оболочки, но не зрачка; степень 3 означает, что эндотелий, хрусталик и радужка соприкасаются. 2-я степень очень серьезна, потому что она может ухудшиться и перейти в 3-ю степень. Чтобы восстановить анатомию и устранить угрозу камеры 3-й степени, мы обычно восстанавливаем камеру на щелевой лампе с информированного согласия пациента.
|
 иголка. 3 степень — неотложная медицинская помощь; вам нужно немедленно реформировать переднюю камеру. Если камера 2 или 3 степени, мы видим пациента каждый день или каждые пару дней, чтобы убедиться, что камера не стала еще более мелкой.
иголка. 3 степень — неотложная медицинская помощь; вам нужно немедленно реформировать переднюю камеру. Если камера 2 или 3 степени, мы видим пациента каждый день или каждые пару дней, чтобы убедиться, что камера не стала еще более мелкой.Всякий раз, когда имеется неглубокая камера, следует расширить зрачок, чтобы отодвинуть линзо-ирисовую диафрагму назад.Перемещение хрусталика и ирисовой диафрагмы назад может привести к тому, что цилиарное тело станет более водянистым, тем самым углубив камеру и повысив давление. Примерно в 80% случаев это приведет к исчезновению отслоения хориоидеи. Для этого мы обычно используем 1% атропин два-три раза в день. (Однако мы избегаем применения атропина у пациентов с заболеваниями предстательной железы.)
Мы всегда проверяем наличие хориоидеи при низком давлении; если они есть, мы объясняем пациенту, что в 80% случаев это пройдет само по себе.Мы наблюдаем за пациентом каждую неделю или каждые две недели, если камера не слишком мелкая.
Примерно в 20 процентах случаев нам приходится вмешиваться и дренировать отслоение хориоидеи в операционной.
Это обычно побуждает цилиарное тело вырабатывать больше жидкости, восстанавливая глубину передней камеры и улучшая зрение. Кроме того, мы обычно увеличиваем дозу стероидов и следим за тем, чтобы не было утечки, вызывающей гипотонию. Затем мы всегда проинструктируем пациента не тереть глаза и пользоваться щитком на ночь.Все эти превентивные меры должны способствовать тому, чтобы глаз снова оказался под давлением. Поскольку это часто бывает длительным, мы хотим предотвратить весь этот цикл, поддерживая давление между 15 и 20 мм рт.ст. в начале послеоперационного периода.
|
С другой стороны, иногда неглубокая камера застает нас врасплох; когда мы проверяем пузырь, кажется, что потока не много, но в послеоперационном периоде давление ниже, чем мы ожидали. Фактически, иногда глаз полностью закрывается, когда давление становится очень высоким и падает после операции.Глаз может просто перестать выделять жидкость, что приведет к очень низкому падению давления, несмотря на все наши усилия.
К счастью, в большинстве случаев мы знаем, какие пациенты подвержены риску гипотонии, и прилагаем все усилия, чтобы избежать такого исхода во время операции. В целом, я бы сказал, что мы сталкиваемся с гипотонией примерно в 5% случаев.
Лечение кровотечений
Кровоизлияния – неотъемлемая часть жизни при выполнении трабекулэктомии.Отчасти это связано с тем, что большинство этих пациентов — пожилые люди, которые принимают препараты для разжижения крови, такие как плавикс, кумадин или просто аспирин — иногда их комбинацию — по различным системным причинам, большинство из которых довольно серьезные. В моей практике нет случаев, когда пациенты прекращали прием препаратов, разжижающих кровь. Но я также не использую перибульбарные блокады, так что здесь есть некоторый фактор безопасности, поскольку мы не вводим иглы в местах, где мы не можем видеть, что происходит. Вместо этого мы используем метод блиц-анестезии, сочетающий местное введение 2% лидокаина в желе, внутрикамерное введение 1% лидокаина без консервантов и субконъюнктивальный лидокаин. Эта стратегия позволяет нам остановить любое кровотечение, потому что мы можем его увидеть, если оно произойдет.
Эта стратегия позволяет нам остановить любое кровотечение, потому что мы можем его увидеть, если оно произойдет.
Иногда, когда ВГД падает с высокого на низкий, у пациента развивается супрахориоидальное кровоизлияние, а не просто отслоение хориоидеи, что очень серьезно. На самом деле супрахориоидальное кровоизлияние часто можно диагностировать по телефону. Пациентка будет сидеть на кухне, поглядывая на часы, и ровно в 10:02 она почувствует сильную боль в глазу. Пациентка часто может точно сказать вам, что она делала, когда это произошло.
|
 Мы видим пациента на следующее утро, и, конечно же, у глаза сильное кровотечение. Если повезет, то не настолько значительно, чтобы прорвало сетчатку в полость стекловидного тела, а содержится в супрахориоидальном пространстве.
Мы видим пациента на следующее утро, и, конечно же, у глаза сильное кровотечение. Если повезет, то не настолько значительно, чтобы прорвало сетчатку в полость стекловидного тела, а содержится в супрахориоидальном пространстве.Когда это происходит, я обычно поручаю коллеге по сетчатке проверить пациента, чтобы убедиться в отсутствии витреоретинальных спаек, если хориоидеи соприкасаются, что может привести к дальнейшим проблемам с сетчаткой. Часто эти кровоизлияния необходимо дренировать, но обычно мы ждем 10 дней, пока кровь разжижается. Если хориоидеи не целуются, то врач-глаукоматоз обычно осушает их и восстанавливает камеру. Если есть какие-либо вопросы о витреоретинальных спайках, наши коллеги по сетчатке берут на себя ответственность.
Управление утечкой пузырьков
В конечном счете, вам нужен низкий, диффузный пузырь с минимальной васкуляризацией без утечек. В действительности, конечно, подтекание пузырей может произойти как в раннем, так и в позднем послеоперационном периоде, и существует множество различных способов борьбы с ними. В последние годы наблюдается движение в сторону хирургии на основе свода, поскольку она обеспечивает более диффузный пузырь; в результате конъюнктивальные швы на лимбе теперь являются частью картины. Эти швы иногда негерметичны, что может привести к неглубокой передней камере, гипотонической ситуации и несостоятельности пузыря.
В последние годы наблюдается движение в сторону хирургии на основе свода, поскольку она обеспечивает более диффузный пузырь; в результате конъюнктивальные швы на лимбе теперь являются частью картины. Эти швы иногда негерметичны, что может привести к неглубокой передней камере, гипотонической ситуации и несостоятельности пузыря.
Любая утечка пузыря требует вмешательства; частота эндофтальмита составляет 1 процент в год при наличии подтекающего пузыря. По этой причине, один из шагов, который хирурги глаукомы должны пройти каждый раз, когда они осматривают пациентов после трабекулэктомии, — это проверка на утечку пузырей, обычно с использованием теста Зейделя.
|
Другое дело, если подтекание пузыря происходит позже в послеоперационном периоде. Серьезность этого типа утечки зависит от того, где находится утечка и насколько легко ее устранить.
Иногда аутологичная кровь, введенная в купол пузыря, может помочь закрыть отверстие.От 50 до 60 процентов времени отверстие может быть закрыто очень большой бандажной контактной линзой, такой как линза Контур (Геркулес, Калифорния). Время от времени мы применяем водные подавители, чтобы уменьшить поток и способствовать заживлению отверстия. Если пациента необходимо вернуть в операционную, часто помогает продвижение конъюнктивы; компрессионные швы также могут способствовать его заживлению.
Во время лечения пациенты используют капли с антибиотиками. Однако я не рекомендую использовать их в течение длительного времени, потому что со временем они сами отберут бактерии, устойчивые к антибиотику.
Борьба с инфекцией
Это подводит нас к осложнению, которого боятся все хирурги: инфекции. Инфекция всегда представляет собой серьезную проблему, независимо от того, инфицирована ли только пузырь (блебит) или поражена камера (эндофтальмит).
|
 )
)Гипопион говорит нам, что может быть эндофтальмит, возможно, из-за пузыря. Когда есть клетки в стекловидном теле, а также в передней камере, диагноз очень ясен.Это чрезвычайная ситуация, потому что эндофтальмит может привести к быстрому нисходящему движению к слепоте.
Когда мы наблюдаем эти знаки, срабатывает тревога. В этой ситуации больного лечат витаминизированными антибиотиками или фторхинолонами каждый час. Если возможно, водную среду культивируют. Специалист по сетчатке обычно осматривает пациента и может провести лечение методом постукивания и инъекции. Пациенту сделают УЗИ, чтобы определить уровень клеток в полости стекловидного тела.
Как только становится ясно, что инфекция находится под контролем, мы начинаем давать стероиды, чтобы успокоить глаз и спасти пузырь.
Послеоперационная консультация пациента
Наши рекомендации пациентам после трабекулэктомии стандартны: не тереть глаза и носить защитный экран в течение как минимум одной недели после операции. Если в глазу кровь, я не одобряю никаких наклонов; пациент должен спать с дополнительными подушками, чтобы кровь могла осесть ниже, а затем рассеяться. Мы не поощряем плавание в течение первой недели или около того, пока швы еще на месте, а также поднятие тяжестей или йогу в этот период, хотя аэробные упражнения допустимы.Пациенты могут возобновить прием душа, бритье и мытье головы почти сразу после операции.
Если в глазу кровь, я не одобряю никаких наклонов; пациент должен спать с дополнительными подушками, чтобы кровь могла осесть ниже, а затем рассеяться. Мы не поощряем плавание в течение первой недели или около того, пока швы еще на месте, а также поднятие тяжестей или йогу в этот период, хотя аэробные упражнения допустимы.Пациенты могут возобновить прием душа, бритье и мытье головы почти сразу после операции.
Возможно, самое главное, мы говорим пациентам, что если их зрение изменится, они должны немедленно позвонить нам. Поскольку нас беспокоит спонтанное кровотечение, нас беспокоит инфекция. К счастью, мы редко получаем такие звонки; чаще нам звонят, сообщая о дискомфорте, разрывах или царапинах. Но среди этих звонков иногда бывают очень серьезные, поэтому мы всегда призываем наших пациентов немедленно звонить нам, если они замечают какие-либо существенные изменения.
Когда пузырек не работает
К сожалению, неудача пузыря не редкость, независимо от того, насколько хорошо сделана операция. Обычно мы даем два-три месяца, прежде чем решить, был ли пузырек успешным или неудачным. Очевидно, что если давление повышается через три-четыре недели, мы должны следить за дальнейшим повышением давления, но часто это просто тенонова киста, которую необходимо размягчить, и в этом случае мы снова назначаем пациенту лекарства от глаукомы. и ждать.
Обычно мы даем два-три месяца, прежде чем решить, был ли пузырек успешным или неудачным. Очевидно, что если давление повышается через три-четыре недели, мы должны следить за дальнейшим повышением давления, но часто это просто тенонова киста, которую необходимо размягчить, и в этом случае мы снова назначаем пациенту лекарства от глаукомы. и ждать.
Несостоятельный пузырек часто можно реанимировать, прокалывая его митомицином С. Однако наилучший успех при прокалывании обычно наступает спустя много времени после того, как была установлена трабекулэктомия, обычно через год или более. На данный момент у нас есть 64-процентный показатель успеха возвращения трабекулэктомии к жизни. Если трабекулэктомия не увенчалась успехом на ранней стадии, прокалывание пузыря обычно не дает успешного результата. В то же время, если я замечаю, что глаз чрезмерно красный и в конъюнктиве есть кровеносные сосуды, и я боюсь, что пузырек не выдержит, я иногда делаю инъекцию Авастина в пузырек.(Конечно, это не по прямому назначению.)
Иногда трабекулэктомия не удается уже через шесть недель. Если это произойдет, в зависимости от состояния зрительного нерва и поля зрения нам, возможно, придется перейти к другому подходу к лечению. В такой ситуации мы обычно ждем, пока глаз полностью успокоится, примерно через два месяца. Затем мы переоцениваем ситуацию. Если трабекулэктомия определенно не удалась, я бы рассмотрел вариант шунтирования ExPress с любой стороны глаза, если это возможно, или при необходимости перешел бы к трубчатому шунтированию.
Полезные советы
Несколько моментов, о которых следует помнить при ведении пациентов после трабекулэктомии:
• Заранее информируйте пациентов о возможных осложнениях. Пациентов, которым предстоит операция, например, с очень высоким ВГД, следует предупредить о том, что у них повышен риск закрытия глаза, и им следует прекратить делать послеоперационную внутриглазную жидкость. (Вы также должны ясно дать понять, что собираетесь сделать все возможное, чтобы этого не произошло.)
• Убедитесь, что у пациента реалистичные ожидания относительно катаракты. Пациент должен понимать, что минимальная катаракта может прогрессировать после трабекулэктомии.
• Рассмотрите возможность удаления существующей катаракты во время трабекулэктомии. Мы часто делаем это для улучшения зрения в дополнение к контролю внутриглазного давления, поскольку операция по удалению катаракты в этой избранной подгруппе неизбежна и часто лучше всего лечится одним визитом в операционную.
• Если зрение пациента в первый день после операции идеальное, не думайте, что все хорошо. Как отмечалось ранее, это, вероятно, указывает на то, что ВГД выше, чем должно быть, и его необходимо устранить.
• Сосредоточьтесь на зрительной реабилитации. Очень важно как можно быстрее вернуть людей к нормальной деятельности, а не просто сосредоточиться на ВГД. Иногда рефракция пациента меняется после операции, поэтому следует заранее обсудить это с пациентом.
После операции мы удаляем разъемные и конъюнктивальные швы через три недели и при необходимости поощряем повторную рефракцию, пока все стабильно. Мне нравится следить за тем, чтобы пациенты быстро рефракционировали и возвращались к повседневной деятельности, а самое позднее к шести-восьми неделям приступали ко всем видам деятельности.
• Следите за едва заметными утечками пузырьков. Не каждая утечка очевидна, но последствия все равно могут быть серьезными. Поэтому всегда проверяйте на утечку, даже если все выглядит хорошо.
• Рассмотрите возможность предварительного наложения склеральных швов перед склеростомой. Трабекулэктомии иногда могут спровоцировать развитие нестандартного астигматизма. Одним из способов предотвращения этого в операционной является предварительное наложение склеральных швов перед снятием блока. Таким образом, когда глаз смягчается, швы остаются на месте, поэтому мы не вызываем никакого дополнительного астигматизма.
• Не используйте анестезию. Это позволит избежать возможности невидимых кровотечений, которые могут быть вызваны инъекцией.
Лучшие варианты: скоро?
Меня очень воодушевляют все исследования способов снижения ВГД за счет максимального оттока без образования пузырьков. Проблема в том, что до сих пор не существует ни одной процедуры, которая в достаточной степени снизила бы ВГД у пациентов, которым требуется очень низкое давление, выражающееся однозначной цифрой, — по крайней мере, ни одна из них не была достаточно надежной, чтобы стать новым золотым стандартом. Так что на данный момент трабекулэктомия по-прежнему остается операцией для этих пациентов. Это несовершенно, но по сравнению со слепотой риск определенно стоит того. ОБЗОР
Доктор Мостер — профессор офтальмологии в Медицинской школе Университета Томаса Джефферсона и лечащий хирург отделения глаукомы Института глаза Уиллса.

 Противовоспалительные средства восстанавливают слизистую роговицы, используются для профилактики осложнений электроофтальмии.
Противовоспалительные средства восстанавливают слизистую роговицы, используются для профилактики осложнений электроофтальмии. Ципролет восстанавливает ткани глаза при ожогах. Лекарство назначается и в том случае, если в глаз попадает инородное тело.
Ципролет восстанавливает ткани глаза при ожогах. Лекарство назначается и в том случае, если в глаз попадает инородное тело. Лекарство обеспечивает профилактику гнойных осложнений, используется при травмировании глаз.
Лекарство обеспечивает профилактику гнойных осложнений, используется при травмировании глаз. Если желаете, замените пипетку на шприц без иглы.
Если желаете, замените пипетку на шприц без иглы.
 Чем быстрее будет достигнут контроль над болью, тем быстрее Вы восстановитесь после перенесенной операции. Не надо терпеть боль! Если Вы почувствовали боль, сообщите об этом медицинской сестре.
Чем быстрее будет достигнут контроль над болью, тем быстрее Вы восстановитесь после перенесенной операции. Не надо терпеть боль! Если Вы почувствовали боль, сообщите об этом медицинской сестре.
 Это работает как кардиостимулятор в сердце.
Это работает как кардиостимулятор в сердце.


