Цвета побежалости металла
Экспериментальная мастерская Виктора Леонтьева. Разное из металловедения
Приветствую вас, коллеги и господа мастеровые. Я расскажу о старинном методе измерения температуры стальных предметов по внешним признакам. Приборов для точного измерения температуры различных объектов в наше время существует предостаточно. Для измерения температур контактным методом используются термометры. А для контроля нагрева на расстоянии, то есть, бесконтактно, используются пирометры с различными конструкциями и техническими характеристиками.
И все же, занимающимся металлообработкой надо обязательно уметь определять температуру стальных изделий. Пусть приблизительно, но оперативно и без приборов.
Цвета побежалости
При нагревании некоторых металлосплавов до определенных температур окисные пленки на их поверхностях могут приобретать различные цвета.
Такие цвета и их оттенки характерны для температур, вызвавших их появление, называют цветами побежалости.
Более выразительно цвета побежалости проявляются на сталях: углеродистых, легированных и нержавеющих. Мы понаблюдаем за возникновением цветов побежалости при нагреве газовым пламенем листа из низкоуглеродистой стали. Обозначенное место на поверхности листа, под которым находится источник нагрева, я буду называть точкой нагревания. Заметно, что естественный цвет стали в точке нагревания изменился на светло желтый.
Это означает, что температура материала в этом месте достигла примерно 205 С. По мере дальнейшего повышения температуры, светло желтая область от точки нагревания, как видно, отдалилась. А ее место приобрело темно желтый цвет, с присущей ему температурой 240 С. Пятно общего прогрева расширяется. Цвета побежалости выстраиваются вокруг точки нагревания в характерном порядке, указывая до какой температуры нагрелся материал, в занимаемой каждым из них области. При более плавном нагревании цветотемпературные области будут расширенными. Как на данном образце среднеуглеродистой стали, на котором их осмотр и продолжим. Если не принимать во внимание цветовые оттенки, наблюдаемые в очень узком расположении, насчитываются девять убедительно выраженных цветотемпературных областей, в число которых область с естественным цветом стали не входит. Далее, поочередно к каждой из девяти цветотемпературных областей будет подводиться шаблон, цвет и оттенок которого наиболее сходен с цветом этой области.
По мере дальнейшего повышения температуры, светло желтая область от точки нагревания, как видно, отдалилась. А ее место приобрело темно желтый цвет, с присущей ему температурой 240 С. Пятно общего прогрева расширяется. Цвета побежалости выстраиваются вокруг точки нагревания в характерном порядке, указывая до какой температуры нагрелся материал, в занимаемой каждым из них области. При более плавном нагревании цветотемпературные области будут расширенными. Как на данном образце среднеуглеродистой стали, на котором их осмотр и продолжим. Если не принимать во внимание цветовые оттенки, наблюдаемые в очень узком расположении, насчитываются девять убедительно выраженных цветотемпературных областей, в число которых область с естественным цветом стали не входит. Далее, поочередно к каждой из девяти цветотемпературных областей будет подводиться шаблон, цвет и оттенок которого наиболее сходен с цветом этой области.
На шаблоне указан диапазон температур и среднее значение, которое присуще данному цвету побежалости на поверхности углеродистой стали.
Однажды появившись, цвета побежалости после охлаждения не исчезают. По их наличию можно, например, определить что деталь или инструмент эксплуатировались с некими нарушениями, что и привело к их перегреву. Цвета побежалости на легированных, нержавеющих и жаропрочных сталей такие же. Однако, они проявляются при более высоких температурах, значения которых зависят от содержания легирующих элементов.
По их наличию можно, например, определить что деталь или инструмент эксплуатировались с некими нарушениями, что и привело к их перегреву. Цвета побежалости на легированных, нержавеющих и жаропрочных сталей такие же. Однако, они проявляются при более высоких температурах, значения которых зависят от содержания легирующих элементов.
Цвета каления
При продолжении нагревания на смену цветам побежалости приходят цвета каления.
Поскольку каление представляет из себя свечение материала, объективная оценка самых темных его цветов, возможна только в темноте. А более светлых, как минимум, при затемнении. Первый, различимый глазом цвет каления красновато-коричневый, означающий, что температура каления в области его проявления находится в диапазоне 530 – 580 градусов по Цельсию. В отличие от цветов побежалости, цвета каления при охлаждении не сохраняются, а изменяются в обратном порядке.
Если на поверхности образовалась окалина, ее цвет возвращается к светло серому оттенку. При нагревании магнитных, железоуглеродистых сплавов выше 768 С их магнитные свойства исчезают. И появляются вновь, после охлаждения ниже этой температуры.
Это явление можно использовать как дополнительное средство контроля температур. Цвета каления отражают температуру нагрева не только металлических тел, но и не металлических тоже. Например, изделий из керамики, графита и других.
Метод измерения температур по цветам побежалости и каления
Методом измерения температур по цветам побежалости и каления с давних времен успешно пользовались металлурги, кузнецы, термисты, а так же представители других профессий, включая станочников. Для измерения температуры этим методом, используются таблицы, в которых собраны шаблоны цветов побежалости и каления с описанием их оттенков и указанием значения температур, приводящих к появлению каждого из них.
Для измерения температуры этим методом, используются таблицы, в которых собраны шаблоны цветов побежалости и каления с описанием их оттенков и указанием значения температур, приводящих к появлению каждого из них.
Имеющие постоянную практику мастеровые и специалисты, таблицами, обычно не пользуются. Поскольку все цветовые оттенки и значения температур, связанные с их проявлениями, они знают на память. Когда же постоянной практики в этой области нет, полагаться на память, особенно на цветовую, пожалуй, не стоит. Путем визуального сравнения из той или иной таблицы, выбирается шаблон, цвет которого более похож на цвет контролируемой области объекта. Акцентирую ваше внимание на том, что при сравнении цветов шаблона и объекта, ожидать их полного, до идентичности совпадения, не следует.
Достаточно именно похожести их цветовых оттенков. И тогда можно считать, что температура равномерно прогретого объекта, находится в диапазоне значений, указанных на цветовом шаблоне.
Часто на поверхности объекта проявляются сразу два смежных цвета. Не сложно догадаться, что температура этого объекта находится между средними значениями температур, указанными на обоих шаблонах. В сравнении с приборными измерениями, точность этого метода, конечно, меньшая. И все же, во многих случаях применения, например, при выполнении не особо ответственной закалки или отпуска, точности цветового метода вполне хватает. Что же касается обработки резанием, когда по цветам побежалости на движущейся стружке контролируется расстояние режущей кромки, причем, в разных ее точках, замены этому старому методу, пожалуй, не найти. Таблиц с цветами побежалости и каления в литературе и интернете опубликовано достаточно. Их интерпретации отличаются по форме и по содержанию, к сожалению, тоже. В отличие от большинства из них цвета, используемые в этом видео уроке шаблонов, выверены с помощью компьютера по реальным цветам каления и по цветам побежалости углеродистых сталей. Указанные на шаблонах названия цветовых оттенков условные.
По этому коду, введенному в поиск, цвет любого их шаблонов легко найти в интернете. Готовые таблицы с цветовыми шаблонами для загрузки в мобильное устройство или для печати, можно скачать с сайта проекта. Возможные причины погрешностей при измерении температур Надо учитывать, что на цветовосприятие влияет общая освещенность помещения, а так же ее цвет, который может быть естественным, белым или желтоватым, исходящим от ламп накаливания. Это касается тех случаев, когда пытаются оценить цвета, полагаясь на память. При измерении температур по цветам побежалости, надо понимать, что ими отражается температура именно на контролируемой поверхности. А это не всегда соответствует температуре всей массы нагретого предмета. Если стоит задача нагреть предмет до определенной температуры, с контролем по цвету побежалости, его надо прогревать не через одну какую-то точку или поверхность, а равномерно, со всех сторон.
Цвета побежалости стали — Энциклопедия по машиностроению XXL
Нагрев деталей при отпуске производится в ваннах, заполненных расплавленным свинцом, оловом, солями или в воздушной среде. В подвижных мастерских нагрев деталей производят на. металлических плитах, контролируя температуру по цветам побежалости стали.Температуру нагрева деталей при термической обработке определяют специальными приборами, называемыми пирометрами. При отсутствии пирометров температуру нагрева металла можио определить грубо на глаз по цветам каления и по цветам побежалости стали. [c.83]
[c.83]
Температура нагрева и цвета побежалости стали [c.84]
Цвета побежалости стали [c.53]
Цементит окрашивается при выявлении методом цветов побежалости [4], пикратом натрия [60] при травлении при 90° С в течение 5—30 мин. Раствор Ka[Fe( N)e] при 20° С начинает окрашивать цементит в сталях после травления в течение 1 ч (наиболее интенсивное окрашивание наступает через 2 ч). [c.153]
Проба стали свободна от коррозии Допустимы легкие цвета побежалости [c.36]
Цвета побежалости углеродистых сталей [c.164]
Цвета побежалости нержавеющих сталей и жаропрочных сплавов [c.165]
Цвета каления сталей 164 Цвета побежалости углеродистых сталей 164 —-нержавеющих сталей и жаропрочных сплавов 165 Цекование — Подачи 376, — Скорости резания 382 Цементация — Обозначение — Характеристика 163 Центр тяжести плоской фигуры — Определение 65 Цианирование — Характеристика 163
[c. 766]
766]
При упрочнении деталей, изготовленных из быстрорежущей стали или ее заменителей, на смежной грани допускается наличие первого из цветов побежалости — светло-желтого при электроискровом упрочнении деталей, изготовленных из углеродистой стали, режимами и технологией упрочнения обеспечивают полное отсутствие цветов побежалости. [c.276]
Непосредственно с краем шва (один из очагов разрушения) металл имеет явно выраженные цвета побежалости, что хорошо видно под микроскопом (МБС-10) при увеличении в 10… 30 раз. Это позволяет предположить, что вблизи сварного шва существует зона провоцирующего нагрева, которая может быть причиной нарушения межкристаллитных связей в стали и привести к межкристаллитной коррозии (МКК), особенно у аустенитных хромоникелевых сталей не стабилизированных титаном или ниобием. По литературным данным [70, 81 и др.] для проявления склонности к МКК для сталей типа 18-10 (18-9) [c.91]
Во время нагрева стали для отпуска в пределах 220—320° С на ее чистой поверхности образуются характерные цвета побежалости, которые появляются из-за возникновения тончайших пленок окислов. Толщина пленок окислов зависит от температуры нагрева и продолжительности выдержки при температурах нагрева. Низкие температуры дают наиболее тонкую пленку вызывая интерференцию коротких синих лучей, пленка принимает желтый цвет.
[c.247]
Толщина пленок окислов зависит от температуры нагрева и продолжительности выдержки при температурах нагрева. Низкие температуры дают наиболее тонкую пленку вызывая интерференцию коротких синих лучей, пленка принимает желтый цвет.
[c.247]
Пользуются также приближенными методами определения температуры металла по цветам каления при нагреве под закалку или отжиг и при отпуске по цветам побежалости на светлой поверхности деталей. При этом цвет побежалости зависит от времени пребывания стали при данной температуре. В практике исследования состояния деталей при эксплуатации о их температуре также судят по цветам побежалости. [c.111]
При термической обработке необходимо соблюдать температурный режим, так как нарушение его может привести к браку. Для точного определения температурного режима используют различные приборы. Без приборов температуры устанавливают приблизительно.
 Обычно это делает опытный термист. Температуру определяют по цвету побежалости и излучению (цвету каления). Цвета побежалости — радужные цвета, возникающие в результате появления тонкого слоя окислов на чистой поверхности углеродистой стали при нагреве от 220 до 330 °С (табл. 9.1). Ими можно пользоваться при низком отпуске и закалке с самоотпуском.
[c.175]
Обычно это делает опытный термист. Температуру определяют по цвету побежалости и излучению (цвету каления). Цвета побежалости — радужные цвета, возникающие в результате появления тонкого слоя окислов на чистой поверхности углеродистой стали при нагреве от 220 до 330 °С (табл. 9.1). Ими можно пользоваться при низком отпуске и закалке с самоотпуском.
[c.175]Нержавеющие 13%-ные хромистые стали имеют более высокую стойкость против окисления до 750—800° С стали с 18— 20% Сг — до 900—1000° С, а стали с 25—28% Сг — до 1100— 1150° С. Повышение содержания хрома в железе сдвигает в сторону более высоких температур начало интенсивного окисления стали и появление цветов побежалости на металле (табл. 213 и рис. 348). [c.650]
Цвета побежалости t 13%-ная хромистая, сталь Углеродистая сталь [c.650]
СИНЕЛОМКОСТЬ СТАЛИ — понижение пластичности стали при статич. нагружении в районе темп-р, вызывающих синий цвет побежалости (ок. 300°). При динамическом нагружении темп-ра хрупкости перемещается в район темп-р 500— 550°.
[c.169]
300°). При динамическом нагружении темп-ра хрупкости перемещается в район темп-р 500— 550°.
[c.169]
На поверхности стали допускаются цвета побежалости, пятна загрязнения и налет шлама, а также вмятины и бугорки глубиной залегания, не превышающей /г суммы предельных отклонений по толщине шине. [c.290]
Закалка с самоотпуском. Закаливаемая часть нагретого изделия охлаждается в воде, а затем вынимается и отпускается до требуемого цвета побежалости. Применяется для закалки инструмента из углеродистой стали. [c.42]
Отпуск стали до цвета побежалости производится в интервале температур 220—330 °С. [c.45]
Если очистить поверхность закаленной без отпуска стали от окалины, накипи масла и прочего и начать ее подогревать, то при нагреве на поверхности стали появятся цвета побежалости (тонкие окислы металла). По цветам побежалости можно приближенно определить температуру нагрева стали. Температуры отпуска, соответствующие цветам побежалости, приведены в табл. 18.
[c.45]
18.
[c.45]
Отпуск стали по цветам побежалости. Температуру отпуска часто определяют по цветам побежалости. Этот метод основан на наблюдении, показывающем, что светлая, зачищенная поверхность стали при нагреве окисляется, покрываясь тончайшей окисной пленкой. С повышением температуры отпуска толщина окисной пленки увеличивается и цвет поверхности изменяется. Каждому цвету побежалости свойственна определенная температура (табл. 6). Цвета побежалости зависят не только от температуры нагрева, но и от продолжительности нагрева, т. е. времени выдержки. [c.39]
Цвета побежалости. Это радужные цвета, возникающие в результате появления тонкого слоя окислов на чистой поверхности углеродистой стали при нагреве ее в интервале температур 150—350°С и на легированной стали при более высоких температурах. [c.90]
Появление цветов побежалости при отпуске в интервале 200—300°С объясняется тем, что при этих температурах на чистой (полированрюй, шлифованной) металлической поверхности возникают тонкие слои окислов. Цвет слоя окисла зависит от его толщины уже за короткое время пребывания стали при 220°С она покрывается слоем толщиной 0,04 мкм. Этот слой придает поверхности стали светло-желтый цвет. Данные об изменении цвета поверхности в зависимости от толщины слоя и температуры следующие
[c.304]
Цвет слоя окисла зависит от его толщины уже за короткое время пребывания стали при 220°С она покрывается слоем толщиной 0,04 мкм. Этот слой придает поверхности стали светло-желтый цвет. Данные об изменении цвета поверхности в зависимости от толщины слоя и температуры следующие
[c.304]
Технические условия на поверхностную закалку индукционным способом должны гарантировать необходимую работоспособность детали и удобный контроль соответствия с ними фактических результатов термообработки. Они должны включать задание размеров и расположения закаленной зоны с допустимыми отклонениями, глубину закаленного слон, твердость поверхности. В технических условиях также могут быть особо оговорены максимальные пределы деформации, ограничения рихтовки, распространение цветов побежалости, допустимые дефекты в зоне закаленного слоя и др. Технические условия назначаюгся с учетом свойств выбранной марки стали и задают также предшествующую термическую обработку детали, твердость перед закалкой, допустимую глубину переходной зоны разупрочнения исходной структуры (после термического улучшения). При этом учитывается, что граница закаленного слоя и.ч цилиндрической поверхности ие может быть приближена к широкой выступающей торцовой части (к щеке коленчатого вала) менее чем на 6— 10 мм, что дополнительно уточняется после закалки опытной партии. Закалка ие может быть распростраиеиа на участок поверхности с близко расположенными друг к другу отверстиями или широкими одиночными окнами, вырезами, существенно суживаю-1ЦИМИ зону протекания индуктированного тока. Детали инструментального производства, тонкостенные и асимметричные, деформация и неравномерный нагрев которых делают индукционный нагрев неприемлемым, следует перевести на химикотермическую обработку.
[c.4]
При этом учитывается, что граница закаленного слоя и.ч цилиндрической поверхности ие может быть приближена к широкой выступающей торцовой части (к щеке коленчатого вала) менее чем на 6— 10 мм, что дополнительно уточняется после закалки опытной партии. Закалка ие может быть распростраиеиа на участок поверхности с близко расположенными друг к другу отверстиями или широкими одиночными окнами, вырезами, существенно суживаю-1ЦИМИ зону протекания индуктированного тока. Детали инструментального производства, тонкостенные и асимметричные, деформация и неравномерный нагрев которых делают индукционный нагрев неприемлемым, следует перевести на химикотермическую обработку.
[c.4]
На поверхности стальных шлифов при нагреве на воздухе образуются тонкие окисные слои, которые растут в зависимости от температуры и продолжительности травления. Наблюдаемые при этом цвета побежалости являются результатом интерференции.
 При микроскопическом наблюдении обнаруживают, что поверхность шлифа окрашивается на отдельных зернах одной и той же фазы в зависимости от ориентировки зерен относительно поверхности шлифа образуются слои разной толш,ины. Толщина окисных слоев также неодинакова на разных фазах в стали цементите и феррите. Это явление используют для получения цветных изображений структуры.
[c.96]
При микроскопическом наблюдении обнаруживают, что поверхность шлифа окрашивается на отдельных зернах одной и той же фазы в зависимости от ориентировки зерен относительно поверхности шлифа образуются слои разной толш,ины. Толщина окисных слоев также неодинакова на разных фазах в стали цементите и феррите. Это явление используют для получения цветных изображений структуры.
[c.96]Проведение травления довольно просто. Шлиф после полирования слегка подтравливают. Благодаря этому проявляются границы зерен и одновременно удаляется оказывающий вредное влияние на окончательные результаты деформированный слой. Некоторые авторы, например Скортези и Дюранд [56], рекомендовали неоднократное травление и полирование. Хорошо обезжиренный образец помещают полированной стороной вверх на медную плиту или песчаную баню и нагревают. За поверхностью образца следует непрерывно наблюдать. По достижении желаемой окраски шлифа образец охлаждают в ртутной ванне или, если не стремятся избежать слабого дополнительного развития цветов побежалости, на холодной металлической плите. Горячее травление на воздухе можно применять в первую очередь для незакаленных сталей при нагреве практически неизбежны изменения мартенсита. Несмотря на это, Ханке и Хенкель [57] травили этим методом мартенситные и аустенитные образцы при этом они смогли очень хорошо выявить обе фазы.
[c.96]
Горячее травление на воздухе можно применять в первую очередь для незакаленных сталей при нагреве практически неизбежны изменения мартенсита. Несмотря на это, Ханке и Хенкель [57] травили этим методом мартенситные и аустенитные образцы при этом они смогли очень хорошо выявить обе фазы.
[c.96]
При выявлении кубического двойного карбида хрома (Сг, Fe)4 методом цветов побежалости происходит очень медленное окрашивание только высокохромистой стали. Раствор KafFe( N)e] при 20° С окрашивает эту структурную составляющую, а также кубический двойной карбид вольфрама Tj-FeaWg [79] (сталь [c.154]
Если кусок стали очистить от окалины напильником, зач истить наждачной бумагой и начать подогревать, то на очищенной поверхности, начиная с температуры 220° С, начнут появляться разные цвета от светложелтого до серого. Эти цвета называются цветами побежалости. Каждый цвет соответствует определенной те1мпературе. Появление побежалых цветов объясняется образованием на поверхности стали тонкой плеики окислов железа, получающейся в ре-20
[c. 20]
20]
При температурах 200—300° С наблюдается снижение пластичности стали ( > и При этом уменьшение пластичности и вязкости стали в области тегчператур 200— 300° С носит название синеломкости, которое происходит от синего цвета побежалости при нагреве стали до 300° С. [c.41]
Нагревание титана в условиях ограниченного доступа воздуха сопровождается появ.пением на его поверхности цветов побежалости, подобно тому как это наблюдается при нагревании стали. Блестящая голубая поверхность, возникающая, по-видимому, в результате образования окиси титана, обладает большей коррозионной сто11костью против воздействия некоторых кислот, чем сам металл. Растворение кислорода, азота и углерода в титане, наблюдаемое прп нагревании металла в атмосфере содержащих эти элементы газов, служит практически способом упрнчнения поверхности титана. [c.769]
Каждому из указанных выше периодов присущи свои механизмы распространения трещины. В первом периоде распространение трещины контролируется двумя механизмами — продольным и поперечным сдвигом. Для стали 45 по отметкам фронта трещины нагревом образца до цветов побежалости установлено, что она имеет форму по-луэллипса. Для трещин, глубина которых не превышает 0,5, отношение полуосей составляет около /3. При дальнейшем увеличении их размеров это соотношение нарушается, происходит более интенсивное ее прорастание вглубь.
[c.49]
Для стали 45 по отметкам фронта трещины нагревом образца до цветов побежалости установлено, что она имеет форму по-луэллипса. Для трещин, глубина которых не превышает 0,5, отношение полуосей составляет около /3. При дальнейшем увеличении их размеров это соотношение нарушается, происходит более интенсивное ее прорастание вглубь.
[c.49]
Металл измельчают гребенчатыми резцами из стали Р6М5, схема которых показана на рис. 10, Режим измельчения практически целиком определяется ограничениями, связанными с качеством получаемой стружки. Частота вращения шпинделя токарно-винторезных станков составляет 12,5 — 31,5 мин» , так как при большей частоте вращения возможно появление на поверхности стружки цветов побежалости. Угол наклона плоскости резца к направлению подачи колеблется в пределах от 9 до 20° угол заточки резца подбирают опытным путем из расчета получения материала необходимой крупности. Продольную подачу резца варьируют в пределах 0,07 — 0,25 мм/об.
[c. 119]
119]
Изучение структуры и свойств сварных соединений после длительной выдержки (старения) при температурах 250-650°С позволило установить, что разрушение образцов во всех случаях происходит в з.т.в. Это связано с ростсяи зерна, которое увеличивается-до 3-4 балла по сравнению с 7-8 баллом в исходном состоянии. Вздержка при температуре 650°С приводит к собирательной рекристаллизации и направленной диффузии углерода из ферритной в аустенитную сталь при сварке разнородных материалов. На поверхности зачищенных сварных соединений и основного металла нет сколько-нибудь значительной окалины. Появляются лишь цвета побежалости. [c.45]
Полученные этим автором результаты по сухому сероводороду приведены на рис. 128. По данным привеса видно, что коррозия исключительно слаба. Все металлы делятся автором на три группы. К первой группе относятся металлы, не изменяющие даже внешнего вида (магний, алюминий и сплав авиаль), а также те, которые сохраняют естественный вид, но покрываются либо цветами побежалости (цинк), либо мелкими черными пятнышками (сталь 18-8). Ко второй группе относятся металлы, меняющие лишь свой цвет,— никель, железо и свинец. К третьей — металлы, изменяющие свой внешний вид,— серебро, латунь и медь.
[c.193]
Ко второй группе относятся металлы, меняющие лишь свой цвет,— никель, железо и свинец. К третьей — металлы, изменяющие свой внешний вид,— серебро, латунь и медь.
[c.193]
Лента электротехничеекой стали имеет поверхность. На поверхно сти лент в состоянии поставки не допускаются ржавчина,, надавы и изгибы, дающие излом. Цвета побежалости и легкий налет после травления не являются браковочными признаками. На кромках лент не до-. пускаются расслоения, а также де йты, выводящие леету за пределы номинальных разм )ов. На поверхности лент допускаются вмятины, надавы от валков, мелкие риски и царапины и легкая ря зна в пределах половины допускаемых отклонений по толщине. [c.300]
Считают, что при наличии некоторого опыта по цветам побежалости стружки нелегированной стали можно определить температуру с точностью 5°, т. е. около 2%. Однако в действительности этот метод дает значительно большую погрешность, доходящую иногда, как показали опыты Б.
 Т. Прушкова, даже до 20—30% в зависимости от толщины среза, времени работы и др. Столь большие отклонения вызваны тем, что цвета побежалости выражают лишь температуру поверхности стружки, определяющую толщину пленки окисла, а тем самым и ее цвет. Цвет побежалости меняется в зависимости не только от температуры, но и от продолжительности действия тепла. При охлаждений стружки смазочно-охлаждающими жидкостями цвета побежалости могут совсем- исчезнуть, между тем как стружка сохраняет на поверхности контакта с резцом высокую температуру. ……
[c.137]
Т. Прушкова, даже до 20—30% в зависимости от толщины среза, времени работы и др. Столь большие отклонения вызваны тем, что цвета побежалости выражают лишь температуру поверхности стружки, определяющую толщину пленки окисла, а тем самым и ее цвет. Цвет побежалости меняется в зависимости не только от температуры, но и от продолжительности действия тепла. При охлаждений стружки смазочно-охлаждающими жидкостями цвета побежалости могут совсем- исчезнуть, между тем как стружка сохраняет на поверхности контакта с резцом высокую температуру. ……
[c.137]Инструмент из углеродистой стали (зубила, крейцмей-сели, молотки и др.), нагретый по всей длине, при необходимости закалки только рабочей части калят в перекидку . Например, закалку зубила можно произвести следующим образом после опиловки, зачистки и предварительной заточки зубило нагревают до температуры 780—800 °С (светло-вишневый цвет), затем погружают рабочую часть в воду на глубину 30—35 мм. После потемнения рабочей части зубила его вынимают и погружают в воду боек на глубину 20—25 мм. При охлаждении бойка рабочая часть зубила эа счет передачи тепла от неохлаждаемой части металла нагревается и отпускается. Чтобы судить о температуре отпуска по цвету побежалости, необходимо закаливаемую часть зубила зачистить наждачным полотном или на обычном камне. Отпуск рабочей части зубила производится при температуре 270—300°С (фиолетовый цвет побежалости), отпуск бойка зубила — при температуре 450—500 °С, т. е. при сером цвете побежалости.
[c.48]
При охлаждении бойка рабочая часть зубила эа счет передачи тепла от неохлаждаемой части металла нагревается и отпускается. Чтобы судить о температуре отпуска по цвету побежалости, необходимо закаливаемую часть зубила зачистить наждачным полотном или на обычном камне. Отпуск рабочей части зубила производится при температуре 270—300°С (фиолетовый цвет побежалости), отпуск бойка зубила — при температуре 450—500 °С, т. е. при сером цвете побежалости.
[c.48]
Толщина пленки окислов зависит от температуры нагрева стали, а пленки разной толщины по-разному отражают лучи света. Например, соломенный цвет побежалости характерен для углеродистых сталей при температуре 220—245°С, буровато-желтый—при 260° С, пурпуроватый — при 275—280° С, темно-синий— при 310° С. По цветам побежалости можно определять температуру нагрева стальных деталей при отпуске. [c.90]
Приведем некоторые данные, полученные методом эллиптической поляризации отраженного света. На мягкой стали (0,04% С) в азотной кислоте образуется пленка толщиной б = 25-г 30 А [26]. На нержавеющей стали (—0,1% С, —18% Сг, 8% N1) в этих же условиях б я 10 А. Такую же толщину имеет пленка, образованная на железе в сухом воздухе. Железо и никель испытывались соответственно в 0,5 н. NaOH -1- 1 н. N82804 и в 0,1 н. КаОН 0,3 н. На2304. Образцы подвергались анодной поляризации, благоприятствующей образованию окисла, и катодной, восстанавливающей его. После первой анодной поляризации б = 20 40 А. При повторных анодных и катодных поляризациях, приводящих к разрыхлению поверхности, на электродах наблюдались цвета побежалости, т. е. б сильно увеличивалась.
[c.89]
На мягкой стали (0,04% С) в азотной кислоте образуется пленка толщиной б = 25-г 30 А [26]. На нержавеющей стали (—0,1% С, —18% Сг, 8% N1) в этих же условиях б я 10 А. Такую же толщину имеет пленка, образованная на железе в сухом воздухе. Железо и никель испытывались соответственно в 0,5 н. NaOH -1- 1 н. N82804 и в 0,1 н. КаОН 0,3 н. На2304. Образцы подвергались анодной поляризации, благоприятствующей образованию окисла, и катодной, восстанавливающей его. После первой анодной поляризации б = 20 40 А. При повторных анодных и катодных поляризациях, приводящих к разрыхлению поверхности, на электродах наблюдались цвета побежалости, т. е. б сильно увеличивалась.
[c.89]
У. Р. Эванс [17] нагревал железную пластинку на воздухе так, чтобы на одном ее конце стали видны цвета побежалости, а другой конец оставался бы холодным и без видимых изменений. После охлаждения в разных местах поверхнйсти пластинки наносились капли раствора нитрата меди. На конце пластинки, остававшемся холодным, немедленно происходило окисление железа ионом Си
[c. 209]
209]
Я сварщик — Цвета побежалости — дефект сварки?
Бытует мнение, что цвета побежалости при сварке углеродистых сталей являются дефектом. Мне лично пару раз приходилось такое слышать и однажды, увидев комментарии к фотографии шва с яркими цветами побежалости, что это явный дефект, решил разобраться в вопросе более подробно. Этакий MYTHBUSTERS предлагаю посмотреть под катом.
Начнем с определения.
Цвета побежалости — радужные цвета, образующиеся на гладкой поверхности металла или минерала в результате формирования тонкой прозрачной поверхностной оксидной плёнки (которую называют побежалостью) и интерференции света в ней. [1]
Эти цвета ранее использовали для определения температуры при
термообработке стали. Но это не очень точный
индикатор. На окрас влияет скорость подъёма температуры, состав газовой среды,
время выдержки стали при данной температуре, а также характер освещения и др. факторы. [1]
факторы. [1]
Между толщиной плёнки и длиной волны отраженного ею света существует прямая зависимость: чем больше толщина пленки, тем более коротковолновый отраженный свет мы получаем. Например, синий цвет образуется, когда из белого «вычитаются» более длинные волны, например, красный и оранжевый, а жёлтый образуется при «вычитании» из спектра коротковолнового излучения, например, фиолетового и синего (закройте правую часть радуги, что показана выше). Получается, что синий цвет соответствует более высокой температуре нагрева, а жёлтый — более низкой. [2]
Интересно про цвета побежалости написано здесь.
Рассмотрим схему участков сварного соединения и их термический цикл. [3]
Нам интересен участок №7. Он также
называется участком синеломкости и охватывает
температурный диапазон от 200 до 400 °С. На этом участке наблюдаются синие
цвета побежалости на поверхности металла (откуда и название). При сварке
низкоуглеродистых сталей основной металл в этой зоне не имеет видимых
структурных изменений, но наблюдается резкое падение ударной вязкости из-за
снижения пластичности. Это происходит в тех случаях, когда в сталях содержится
кислород, азот и водород в несколько избыточном количестве. Размеры отдельных
участков ЗТВ и общая ширина ее зависят от условий нагрева, охлаждения и
способов сварки. [4, 5]
При сварке
низкоуглеродистых сталей основной металл в этой зоне не имеет видимых
структурных изменений, но наблюдается резкое падение ударной вязкости из-за
снижения пластичности. Это происходит в тех случаях, когда в сталях содержится
кислород, азот и водород в несколько избыточном количестве. Размеры отдельных
участков ЗТВ и общая ширина ее зависят от условий нагрева, охлаждения и
способов сварки. [4, 5]
При сварке нержавеющих сталей цвета побежалости также проявляют себя, но в других диапазонах температур. Для нержавеющих сталей изменение цвета при нагреве на воздухе наблюдается: светло-соломенный (300°C), соломенный (400°C), красно-коричневый (500°C), фиолетово-синий (600°C), синий (700°C). [1]
Побежалость для
коррозионностойких сталей является более критичной, т.к. является показателем
того, что пассивный (защитный) слой поврежден, и в этом месте могут возникнуть
очаги точечной (питтинговой) коррозии. [6] Поэтому
поврежденный слой необходимо зачищать либо лепестковыми кругами, либо щеткой с
ворсом из нержавейки (не допускается зачистка стальной щеткой), либо травление.
[6] Поэтому
поврежденный слой необходимо зачищать либо лепестковыми кругами, либо щеткой с
ворсом из нержавейки (не допускается зачистка стальной щеткой), либо травление.
Итак, получается, что цвета побежалости — неизбежное явление при сварке сталей. Кроме того, в Инструкции по визуальному и измерительному контролю (РД 03-606-03) такой дефект не определен. Они указаны там лишь только как загрязнение, препятствующее контролю и которое должно быть зачищено.
Вероятно, это считают дефектом по ошибке — путают со сваркой титана. Здесь должна обеспечиваться надежная газовая защита поверхности металла нагретой свыше 400°C. О хорошей газовой защите свидетельствует блестящая серебристая поверхность. Появление на шве желто-голубых цветов побежалости указывает на нарушение защиты, а серый налет свидетельствует о плохой защите. [7]
Интересен тот факт, что цвет
побежалости считается дефектом сварного соединения, появляется и в нормативных документах. Например, в СТО-ГК «Трансстрой» 005-2007 Стальные конструкции мостов. Технология монтажной сварки.
Например, в СТО-ГК «Трансстрой» 005-2007 Стальные конструкции мостов. Технология монтажной сварки.
Также мне попалась интересная статья по разработке метода определения сварочных напряжений по цветам побежалости. [8] Нюанс в том, что исследована модель однопроходного шва. Будет ли этот метод работать на многопроходных швах?
В следующей статье мы попытаемся выяснить, можно ли определить был или не был перегрет металл, исходя из ширины участка синеломкости. Что касается вопроса в заголовке статьи, то, я думаю, ответ очевиден — наличие цветов побежалости не является дефектом для углеродистых сталей.
Список использованных материалов:
1. https://ru.wikipedia.org
2. http://metallovedeniye.ru
3. В.А. Лосев, Н.А. Юхин. Иллюстрированное пособие сварщика. Москва: Соуэло, 2004. 59 с.
4. Костенко Е.М. Сварочные работы: Практическое пособие для электрогазосварщика.
5. В.А.
Чебан. Сварочные работы: учеб. пособие. Изд. 3-е. Ростов-на-дону: Феникс, 2006.
412 с.
пособие. Изд. 3-е. Ростов-на-дону: Феникс, 2006.
412 с.
6. Ю. П. Солнцев, Е.И. Пряхин. Материаловедение: учебник для вузов. Изд. 4-е, перераб. и доп. Спб.: Химиздат. 2007. 784 с.
7. С.М. Гуревич. Сварка химически активных и тугоплавких металлов и сплавов. Москва: Машиностроение. 1982. 95 с.
8. Р.В. Гольдштейн, В.М. Козинцев, Д.А. Куров, А.Л. Попов, Д.А. Челюбеев. Разработка метода определения сварочных напряжений по цветам побежалости. УДК 539.3+53.082.56 http://vestnik.pstu.ru
Источник фото: @kinetiktrucks
Материал подготовил Антон Чураков
При использовании данного материала ссылка на ресурс ЯСВАРЩИК обязательна.
Железо цвета побежалости — Справочник химика 21
Отполированную сталь и железо можно подвергнуть воронению, благодаря чему их поверхность покрывается красивым слоем окисла, стойким по отношению к влаге из воздуха. Для воронения поверхность протирают маслом (минеральным) и, положив на железный лист, нагревают на листе в пламени примуса до выгорания масла и почернения поверхности. Стальную деталь, не прибегая к смазыванию маслом, можно нагреть до появления того или иного цвета побежалости и затем для закрепления его опустить в расплавленный парафин или льняное масло (гл. 2, 2). Нагревая стальную пластинку с одной из ее сторон, можно получить и закрепить целую гамму цветов побежалости. [c.155]
Стальную деталь, не прибегая к смазыванию маслом, можно нагреть до появления того или иного цвета побежалости и затем для закрепления его опустить в расплавленный парафин или льняное масло (гл. 2, 2). Нагревая стальную пластинку с одной из ее сторон, можно получить и закрепить целую гамму цветов побежалости. [c.155]
Этому опыту было дано такое объяснение. В местах, подвергнутых слабому нагреву, где нет видимых изменений, образовалась тонкая и сплошная пленка окисла. Она защищала металл от соприкосновения с ионами Си , и реакция (У1,6) была невозможна. В зоне цветов побежалости образовавшаяся пленка окисла настолько толста, что не может остаться сплошной, растрескивается и обнажает железо. В местах дефектов пленки происходит реакция ( 1,6). На поверхности, оставшейся холодной, пленки либо нет вообще, либо она настолько пориста, что реакция (VI,6) протекает беспрепятственно, [c.209]
Термический способ (воронение и синение) применяют для обработки мелких проволочных, а также полированных изделий (часовых стрелок и волосков, винтов, лент, пружин и т. п.). Прр воронении изделия смазывают тонким слоем асфальтового или масляного лака, растворимого в бензине, подсушивают на воздухе и загружают (на железных сетках) на 12— 20 мин. в печь при температуре 350—450° С после того как изделия приобрели черную окраску, их выгружают из печи и охлаждают в минеральном масле. В результате такой обработки на металле образуется защитная пленка из окислов железа, на которой имеется тонкий слой сплавленного асфальта или осмоленного масла. Для синения изделия помещают в печь при температуре 310—350° С и выгружают из нее в момент появления на поверхности металла цветов побежалости. Печи снабжены слюдяным или кварцевым стеклом для наблюден ия за ходом процесса. [c.211]
п.). Прр воронении изделия смазывают тонким слоем асфальтового или масляного лака, растворимого в бензине, подсушивают на воздухе и загружают (на железных сетках) на 12— 20 мин. в печь при температуре 350—450° С после того как изделия приобрели черную окраску, их выгружают из печи и охлаждают в минеральном масле. В результате такой обработки на металле образуется защитная пленка из окислов железа, на которой имеется тонкий слой сплавленного асфальта или осмоленного масла. Для синения изделия помещают в печь при температуре 310—350° С и выгружают из нее в момент появления на поверхности металла цветов побежалости. Печи снабжены слюдяным или кварцевым стеклом для наблюден ия за ходом процесса. [c.211]
Удельный вес никеля, наносимого гальваническим пз тем, равен 8,9 точка плавления 1455° С. Электрическая проводимость никеля составляет лишь 15% электрической проводимости меди. При высокой температуре на никеле появляются цвета побежалости, однако в окисляющей атмосфере при температуре до 800° С никель не изменяет своих свойств. Обычные загрязнения-железо, марганец, кобальт, кислород (в виде окиси) и сера (в виде сульфида). В щелочах и органических кислотах никель не растворяется, в серной и со- тяной кислотах он растворяется медленно, в азотной кислоте хорошо. [c.149]
Обычные загрязнения-железо, марганец, кобальт, кислород (в виде окиси) и сера (в виде сульфида). В щелочах и органических кислотах никель не растворяется, в серной и со- тяной кислотах он растворяется медленно, в азотной кислоте хорошо. [c.149]
Особенности хромового покрытия. Хромовое покрытие стойко против действия большинства газов, щелочей, растворов кислот и солей хром растворяется в горячей серной и азотной кислотах. Блеск и цвет хромового покрытия не изменяются от воздействия атмосферы. При нагревании твердость хро.мового покрытия уменьшается. При температуре нагрева от 200 до 600° С уменьшение твердости происходит медленно, а при температуре свыше 600° С — очень быстро. Для появления цветов побежалости критической температурой является 450° С. При нагреве до температуры, близкой к 450° С, хромовое покрытие начинает менять цвет. С точки зрения противокоррозийной защиты хром как электроотрицательный металл в принципе защищает железо от ржавления. Но поскольку на воздухе хром пассивируется (на покрытии образуется тонкая пленка окиси хрома), то его электроотрицательные и защитные свойства снижаются. Это относится только к тонким пористым хромовым покрытиям. [c.164]
Это относится только к тонким пористым хромовым покрытиям. [c.164]
Физические свойства. Уран — блестящий металл, напоминающий по виду в свежем срезе или окисленном состоянии железо. Поверхность свежеполированного металла имеет сильный блеск, но после нескольких часов пребывания на воздухе покрывается цветами побежалости. Уран имеет плотность 19,07 г/сж . Он на 80% тяжелее свинца, пластичен и ковок. [c.9]
Непосредственно вслед за шлифовкой поверхности железа производилось ее окисление. Для получения клиновидных пленок один конец железной полоски нагревался до появления окалины, в то время как другой находился в хорошем контакте с медным зажимом, иногда охлаждаемым проточной водой. Благодаря этому холодный конец образца сохранял свой металлический блеск. Между холодным и горячим концами всегда можно было наблюдать цвета побежалости различных оттенков. [c.25]
Относительно толстые окисные пленки, снятые с железа, имеющего последние цвета побежалости, в проходящем свете дают коричневатую окраску, а в отраженном имеют блестящий, почти металлический вид На более тонких пленках коричневый цвет и металлический блеск становятся менее четкими. [c.80]
[c.80]
Следует заметить, что легкость отделения пленок, возникших при обычных температурах, сильно меняется в зависимости от физического и химического характера железа. Снятие таких пленок со стали обычно невозможно, хотя пленки со стали, нагретой до цветов побежалости, снимаются легко. Применение йодного метода для отделения пленок от железа, обработанного в растворе хромовокислого калия, упомянуто на стр. 379 эти пленки снимаются более легко, чем пленки, возникшие на воздухе. [c.81]
Несколько опытов, произведенных в Кембридже с желе-. 50М, покрытым видимой пленкой, иллюстрируют этот факт. Железо было очищено абразивом, нагрето до полу Гения цвета побежалости первого порядка и испытано в 0,1 Л серной кислоте. Цвета быстро изменились и скоро исчезли. Даже 0,002 М кислота вызывает утонение пленки в течение минуты. Из этого можно было бы сделать тот вывод, что кислота разрушает пленки окиси железа. Тогда опыт был повторен с железом, нагретым до появления более толстых пленок (цвета [c. 89]
89]
Если это объяснение правильно, то становится возможным воспрепятствовать. восстановлению пленки (замедляя таким образом ее разрушение) при помощи окислительных агентов. Опыты подтвердили это предположение. Было установлено, что 0,01 М серная кислота, содержащая хромовую кисло Уу (0,1 /П), ие изменяет железо с цветами побежалости, хотя 0,01 М серная кислота (без хромовой кислоты) дает заметное изменение в 5 сек. и полное разрушение более ранних окрасок в 1 йин. [c.90]
Описанные опыты делают очевидным то, что видимые окисные пленки на железной поверхности совершенно у с т о й ч и в ы в кислоте в анодных условиях. Были затем проведены опыты с анодом из железа без цветов побежалости, пассивированного в разбавленной серной кислоте применением тока высокой плотности. В этом случае также было обнаружено, что некоторые короткие перерывы тока могут быть допущены без потери пассивности однако более долгие перерывы возвращают металлу его способность растворяться при низких плотностях тока. Трудно не притти к заключению, что оба случая анодного иммунитета являются следствием наличия окисных пленок, хотя на ненагретом железе пленка еще слишком тонка, чтобы дать интерференционные цвета. [c.91]
Трудно не притти к заключению, что оба случая анодного иммунитета являются следствием наличия окисных пленок, хотя на ненагретом железе пленка еще слишком тонка, чтобы дать интерференционные цвета. [c.91]
Опыты, проведенные в лаборатории в Кембридже также показали, что существуют окислы железа, стойкие к азотной кислоте. Полоски электролитического железа нагревались с одного конца, так же как и при получении обычных интерференционных цветов, обязанных возникновению окисным пленкам другой конец полоски при этом остается без изменения. Когда эти полосы были помешены в азотную кислоту уд, веса 1,4, никаких изменений цветов не было замечено даже спустя ЗУа часа при 23° если бы кислота была способна быстро растворять окислы, дающие цвета побежалости, то последние быстро исчезли бы. При повторении этого опыта с более разбавленной кислотой (уд. вес 1,2), железо подверглось сильной коррозии у конца, свободного от цветов побежалости у противоположного конца железо около пленок было подъедено, а сами пленки отстали в виде шероховатых микроскопической величины чешуек, похожих на чешуйки. [c.394]
[c.394]
Видимые пленки, образующиеся иа металлах при действии азотной кислоты. Имеется много указаний, что при действии азотной кислоты на металле может образоваться пленка. Во многих произведенных в Кембриджской лаборатории опытах по исследованию действия разбавленной азотной кислоты на железо было замечено, что в тех случаях, когда красные пары, получающиеся в ходе реакции, проходят над поверхностью железа, поднимаясь к уровню кислоты, получается последовательный ряд интерференционных цветов (желтоватый, красновато-лиловый, синий и т. д.), указывающих на наличие пленки. Достижение видимой толщины доказывало, что вещество пленки не имело здесь защитного характера и, во всяком случае, было установлено, что площадь, покрытая цветами побежалости, в этом случае является активной по отношению к пробе с азотнокислой медью. Однако возможно, что некоторое изменение условий может дать пленки гораздо более ровные и менее пористые и такие пленки, не достигая толщины, необходимой для появления цветов побежалости, могут вместе с тем сделать металл пассивным. Очевидно такие условия осуществляются в концентрированной азотной кислоте. [c.395]
Очевидно такие условия осуществляются в концентрированной азотной кислоте. [c.395]
Одно время высказывались сомнения в том, что цвет побежалости на железе действительно зависит от толщины пленки. Указывали, что если это так, то должно быть возможным изменение цветов в обратном порядке при уменьшении толщины пленки ранние опыты сошлифовывания пленки на железе, окрашенном в голубой цвет первого порядка, не дали пурпурного и желтого цветов, характерных для более тонких пленок, хотя последующие опыты были более успешны Но сошлифовывание не подходящий метод для получения столь тонких пленок. Катодная обработка железа с цветами побежалости в разбавленной соляной кислоте дает более однородное уменьшение толщины и ожидаемое изменение цветов было в действительности получено в данном случае уменьшение толщины зависит от катодного восстановления окиси железа до закиси, которая очень быстро растворяется в кислоте скорость реакции зависит только от силы тока и таким образом легко получить необходимую однородность уменьшения толщины пленки.
 Следовательно, указанное выше возражение по отношению к интерференционному объяснению цветов тонких пленок устранено. [c.841]
Следовательно, указанное выше возражение по отношению к интерференционному объяснению цветов тонких пленок устранено. [c.841]В чистом воздухе пассивирующая пленка и лежащий под ней металл будут химически устойчивы. В загрязненном промышленном воздухе агрессивные газы химически разрушают пассивирующую окисную пленку. При этом изменяется цвет поверхности деталей, на ней появляются цвета побежалости, темные и цветные пятна и т. д. Повышение температуры увеличивает скорость разрушения пассивирующей окисной пленки, а солнечный свет, наоборот, препятствует ее разрушению. Доказано, например, что детали из железа и цинка на солнечном свету химически более устойчивы, чем в темноте. Скорость коррозии резко возрастает также при наличии на поверхностях деталей пыли. В пыльном воздухе коррозия идет значительно интенсивнее. [c.94]
Подобный процесс называется диффузией, причём, благодаря диффузии атомов А, исчезает разность концентраций и устанавливается стехиометриЧеское равновесие. Примером может служить известное явление цветов побежалости, наблюдаемое, например, при образовании тонких слоёв окислов на железе. При этом атом А на рис. 134 соответствует железу, а атом В—кислороду, т. е. слева мы имеем чистое железо, а справа — окислительную атмосферу кислорода. [c.298]
Примером может служить известное явление цветов побежалости, наблюдаемое, например, при образовании тонких слоёв окислов на железе. При этом атом А на рис. 134 соответствует железу, а атом В—кислороду, т. е. слева мы имеем чистое железо, а справа — окислительную атмосферу кислорода. [c.298]
На более сильно нагретом конце полосы цвета побежалости, обусловленные интерференцией, исчезают, и внешний вид определяется специфическим цветом окисла. Обычно пленка имеет синевато-серый или черный цвет но на медной полосе, когда резким изгибом удается отделить пленку в виде тонких чешуек, видно, что, хотя наружный ее слой почти черный и состоит обычно из окиси меди (СиО), внутренний слой — красный и состоит из закиси меди (СигО). Никель образует только один слой (N 0), а железо иногда образует три слоя (см. ниже). [c.30]
Наблюдение за цветами побежалости само собой не позволяет измерить количество окисла на или непосредственно под поверхностью металла. Вернон и его сотрудники нашли, что выше 200° (когда шлифованное железо окисляется однородно по параболическому закону) количество окисла, находящегося в пленке, эквивалентно всему поглощенному кислороду. При нагревании ниже 200° С, когда окислы проникают в металл и окисление подчиняется логарифмическому закону, этого явления не наблюдается. В области более низких температур в снятой пленке кислорода было значительно меньше, чем общее количество поглощенного кислорода. Цвета побежалости отсутствовали (или ограничивались слабым соломенным цветом), даже тогда, когда общее количество поглощенного кислорода, как можно судить по увеличению веса, было достаточно, чтобы образовалась окраска (если допустить, что пленка однородная) [c.58]
Вернон и его сотрудники нашли, что выше 200° (когда шлифованное железо окисляется однородно по параболическому закону) количество окисла, находящегося в пленке, эквивалентно всему поглощенному кислороду. При нагревании ниже 200° С, когда окислы проникают в металл и окисление подчиняется логарифмическому закону, этого явления не наблюдается. В области более низких температур в снятой пленке кислорода было значительно меньше, чем общее количество поглощенного кислорода. Цвета побежалости отсутствовали (или ограничивались слабым соломенным цветом), даже тогда, когда общее количество поглощенного кислорода, как можно судить по увеличению веса, было достаточно, чтобы образовалась окраска (если допустить, что пленка однородная) [c.58]
Потемнение, замеченное на кухонной посуде, объясняется различным образом. Одни авторы рассматривают его как начало образования пленок, дающих благодаря явлениям интерференции цвета побежалости, другие же связывают этот эффект с действием железа. Третьи снова постулируют образование мелких частичек металлического алюминия, вкрапленных в окись или гидроокись. Если, например, коррозия происходит по границам зерен, которые превращаются в окись, а внутренние участки зерна сохраняют металлическое состояние, то любой световой луч, падающий на поверхность, теряется в результате многократного отражения от металлических частиц. Это обусловливает потемнение поверхности по тем же оптическим эффектам, которые объясняют темный цвет мелкодисперсной платины. Возможно, что все эти факторы играют роль при различных обстоятельствах. [c.101]
Третьи снова постулируют образование мелких частичек металлического алюминия, вкрапленных в окись или гидроокись. Если, например, коррозия происходит по границам зерен, которые превращаются в окись, а внутренние участки зерна сохраняют металлическое состояние, то любой световой луч, падающий на поверхность, теряется в результате многократного отражения от металлических частиц. Это обусловливает потемнение поверхности по тем же оптическим эффектам, которые объясняют темный цвет мелкодисперсной платины. Возможно, что все эти факторы играют роль при различных обстоятельствах. [c.101]
На одинаково нагретых полосках меди или железа цвета побежалости ПОЯВЛЯЮТСЯ практически в той же последовательности, но на железе окраска в толстых пленках может быть слабее или вовсе отсутствовать. Окисел железа менее прозрачен, чем окисел меди, поэтому отражение от внутренней поверхности при толстой пленке становится слабее. Тот факт, что последовательность цветов для всех металлов приблизительно одинакова, показывает, что окраска зависит от толщины пленки и не является специфическим свойством окисла. Повторение одного и того же цвета последовательно несколько раз легко объясняется. Если толщина пленки такова, что пути лучей света, отраженных от внутренней и наружной поверхностей пленки, соответственно отличаются на величину, равную половине длины волны зеленого цвета, то произойдет частичное затухание зеленых лучей и образец, рассматриваемый при дневном свете, будет казаться красно-фиолетовым, так как этот цвет является дополнительным к зеленому. Однако до некоторой степени такой же цвет получится, когда пленка утолщилась настолько, что разница в пути лучей стала Р/а, 2V2 или З /а длины зеленой волны. Таким образом, красноватое окрашивание последовательно повторяется несколько раз, хотя его оттенки при повторных появлениях различны. Не только оттенки окраски, но и последовательность цветов второго порядка немного отличается от таковых первого порядка по причинам, которые объяснены на стр. 719. Таблицы толщин пленок различных цветов приведены на стр. 55, 56. [c.30]
Повторение одного и того же цвета последовательно несколько раз легко объясняется. Если толщина пленки такова, что пути лучей света, отраженных от внутренней и наружной поверхностей пленки, соответственно отличаются на величину, равную половине длины волны зеленого цвета, то произойдет частичное затухание зеленых лучей и образец, рассматриваемый при дневном свете, будет казаться красно-фиолетовым, так как этот цвет является дополнительным к зеленому. Однако до некоторой степени такой же цвет получится, когда пленка утолщилась настолько, что разница в пути лучей стала Р/а, 2V2 или З /а длины зеленой волны. Таким образом, красноватое окрашивание последовательно повторяется несколько раз, хотя его оттенки при повторных появлениях различны. Не только оттенки окраски, но и последовательность цветов второго порядка немного отличается от таковых первого порядка по причинам, которые объяснены на стр. 719. Таблицы толщин пленок различных цветов приведены на стр. 55, 56. [c.30]
Полученные этим автором результаты по сухому сероводороду приведены на рис. 128. По данным привеса видно, что коррозия исключительно слаба. Все металлы делятся автором на три группы. К первой группе относятся металлы, не изменяющие даже внешнего вида (магний, алюминий и сплав авиаль), а также те, которые сохраняют естественный вид, но покрываются либо цветами побежалости (цинк), либо мелкими черными пятнышками (сталь 18-8). Ко второй группе относятся металлы, меняющие лишь свой цвет,— никель, железо и свинец. К третьей — металлы, изменяющие свой внешний вид,— серебро, латунь и медь. [c.193]
128. По данным привеса видно, что коррозия исключительно слаба. Все металлы делятся автором на три группы. К первой группе относятся металлы, не изменяющие даже внешнего вида (магний, алюминий и сплав авиаль), а также те, которые сохраняют естественный вид, но покрываются либо цветами побежалости (цинк), либо мелкими черными пятнышками (сталь 18-8). Ко второй группе относятся металлы, меняющие лишь свой цвет,— никель, железо и свинец. К третьей — металлы, изменяющие свой внешний вид,— серебро, латунь и медь. [c.193]
ЦВЕТА ПОБЕЖАЛОСТИ — радужные цвета поверхности материала. Появляются при образовании тонких пленок в результате изменения (напр., окисления) поверхностного слоя. Так, при низком или среднем отпуске стали в окислительной среде (напр., на воздухе) на поверхности образуются п.ченки окислов, толщина к-рых увеличивается с повышением т-ры нагрева и продолжительности выдержки. Появление Д. п. связано с интерференцией белого цвета в этих пленках, вследствие чего погашаются лучи той или иной длины волны. По Ц. п. можно судить о т-ре нагрева и продолжительности выдержки изделия нри этой т-ре, поскольку длина волны погашенного луча зависит от толщины пленки. При нагреве в те-.чение нескольких минут на поверхности железа и нелегированной углеродистой стали появляется Д. п. слабо-желтый — при т-ре 215 С, светло-соломенный — 220° С, светло-желтый — 230 С, тускло-желто-соломенный — 235 С, соломенный — 240 С, густо-соломенный — 250° С, желтовато-коричневый — 255° С, коричневый — 265 С, коричневопурпурный — 270° С, пурпурный — [c.712]
По Ц. п. можно судить о т-ре нагрева и продолжительности выдержки изделия нри этой т-ре, поскольку длина волны погашенного луча зависит от толщины пленки. При нагреве в те-.чение нескольких минут на поверхности железа и нелегированной углеродистой стали появляется Д. п. слабо-желтый — при т-ре 215 С, светло-соломенный — 220° С, светло-желтый — 230 С, тускло-желто-соломенный — 235 С, соломенный — 240 С, густо-соломенный — 250° С, желтовато-коричневый — 255° С, коричневый — 265 С, коричневопурпурный — 270° С, пурпурный — [c.712]
Приведем некоторые данные, полученные методом эллиптической поляризации отраженного света. На мягкой стали (0,04% С) в азотной кислоте образуется пленка толщиной б = 25-г 30 А [26]. На нержавеющей стали (—0,1% С, —18% Сг, 8% N1) в этих же условиях б я 10 А. Такую же толщину имеет пленка, образованная на железе в сухом воздухе. Железо и никель испытывались соответственно в 0,5 н. NaOH 1 н. N82804 и в 0,1 н. КаОН 0,3 н. На2304. Образцы подвергались анодной поляризации, благоприятствующей образованию окисла, и катодной, восстанавливающей его. После первой анодной поляризации б = 20 40 А. При повторных анодных и катодных поляризациях, приводящих к разрыхлению поверхности, на электродах наблюдались цвета побежалости, т. е. б сильно увеличивалась. [c.89]
После первой анодной поляризации б = 20 40 А. При повторных анодных и катодных поляризациях, приводящих к разрыхлению поверхности, на электродах наблюдались цвета побежалости, т. е. б сильно увеличивалась. [c.89]
У. Р. Эванс [17] нагревал железную пластинку на воздухе так, чтобы на одном ее конце стали видны цвета побежалости, а другой конец оставался бы холодным и без видимых изменений. После охлаждения в разных местах поверхнйсти пластинки наносились капли раствора нитрата меди. На конце пластинки, остававшемся холодным, немедленно происходило окисление железа ионом Си [c.209]
ВОН кислоты в слое улучшает его стойкость. На рис. 1.93 показано влияние содержания кремния в сплаве на состав слоя и на коррозионные потери сплава в 10% растворе хлорного железа. На сплавах, содержащих молибден, последний выделяется в форме окисла. Повышенная стойкость этих сплавов основана на совместном действии кремневой кислоты и молибдена [281, 282]. В толстых слоях (300—500 А), которые образуются под действием воЗ духа при нагревании, хром содержится в повышенном, а никель — в уменьшенном количествах. Эти слои являются кристалличс скими, показывают цвета побежалости и построены по типу шпинели [283]. Скорость их роста лимитируется скоростью движения ионов металла и кислорода в слое. [c.103]
Эти слои являются кристалличс скими, показывают цвета побежалости и построены по типу шпинели [283]. Скорость их роста лимитируется скоростью движения ионов металла и кислорода в слое. [c.103]
Опыт V.10. Стальную пластину бОх 10×2 мм зачистить наждачной бумагой, протереть органическим растворителем (ацетоном) для обезжиривания и нагреть с одного конца в пламени газовой горелки в течение 2—3 мин до появления цветов побежалости. Дать пластинке остыть и затем пипеткой нанести на пластинку по ее длине равномерно на некотором расстоянии друг от друга 3—4 капли 2%-ного раствора нитрата меди. Заметить время появления пятен меди в зависимости от того, в какой степени была нагрета пластинка. На том конце пластинки, который совсем не нагревался, медь не выделяется, потому что тонкая окисная пленка на железе защищает металл и не пропускает раствора Си(МОз)а. На противоположном конце пластинки почти мгновенно появляется большое желтое пятно меди. Этот конец нагревался больше всего и здесь образовалась наиболее толстая, но и менее эластичная пленка оксида она растрескивается при высоких температурах и потому не обладает защитными свойствами и пропускает к железу раствор Си(МОз)2- [c. 322]
322]
Практически толщина оксидного слоя может колебаться от сотых долей микрона до 10 л и более. Защитные свойства оксидной тленки, а также механическая прочность ее в значительной степени зависят от применяемого способа оксидирования. Так, тонкие слои, дающие цвета побежалости, получаемые на железе термическим способом, обладают малой механической прочностью вследствие их крайне незначительной толщины, но более высокими защитными свойствами, чем пленки, получаемые химическим способом. В последнем случае защитные окисные пленки отличаются большей пористостью. На скорость образования оксидной пленки влияет состав и структура металла изделия. Малоуглеродистая легированная сталь труднее оксидируется. Для нее требуется повышенная температура оксидирования и большая продолжительность процесса. Как правило, оксидированию подвергаются изделия, предназначенные для использования в закрытых помещениях, а также для временной защиты готовых обработанных изделий. В сухом воздухе окисные пленки достаточно стойки. Во влажной атмосфере и осо- [c.334]
Во влажной атмосфере и осо- [c.334]
Углерод. Влияние углерода на реакции взаимодействия железа с кислородсодержащими газами определяется в большой мере обезуглероживанием при температурах выше приблизительно 700° С. Как известно и как это неоднократно подтверждалось (см., например, работу Остина [745]), обезуглероживание стали водородом сильно ускоряется в присутствии водяного пара или при использовании листовой стали с цветами побежалости. Если углеродсодержащее железо соприкасается с газом, содержащим кислород даже в малой примеси, то образующаяся окись углерода создает значительное давление. зависяп1ее от температуры, концентрации углерода в стали и концентрации кислорода с. газовой среде. Ясно, что выделение окиси углерода (наряду с углекислым газом) должно отразиться на окислении сталей. Этот выделяющийся газ препятствует н какой-то мере созданию [c.320]
Ванадий. В сплавах железа с ванадием последним обогащены внутренние слои, прилегающие к металлу, тогда, как в наружных слоях его обнаруживается мало [116, 446, 729] вследствие сравнительно больщой свободной энергии образования окислов ванадия и малой скорости диффузии его ионов. Ванадий не способен улучшать сопротивление сталей окислению [446, 773]. Наоборот, как наблюдал Бандель [747], добавка ванадия в количестве 4,4% вызывала при 1100° С образование на поверхности сталей цветов побежалости. Фактически легкоплавкая пятиокись ванадия, как это показано несколько дальше, принадлежит к числу самых худших соединений, вызывающих катастрофическое окисление. [c.332]
Ванадий не способен улучшать сопротивление сталей окислению [446, 773]. Наоборот, как наблюдал Бандель [747], добавка ванадия в количестве 4,4% вызывала при 1100° С образование на поверхности сталей цветов побежалости. Фактически легкоплавкая пятиокись ванадия, как это показано несколько дальше, принадлежит к числу самых худших соединений, вызывающих катастрофическое окисление. [c.332]
Другим рациональным методом задержки катодного восстановления пленок является анодная обработка образца с цветами побежалости. Для этого нужно соединить образец с электрической батареей до введения его в кислоту в противном случае пленки будут разрушены до того, как начнется анодная обработка. Когда железо, имеющее цвет первого порядка, становится с момента его погружения в кислоту анодом, не наблюдается никакой коррозии и никаких изменений цвета образец ведет себя как пассивный анод и выделяется кислород. Оказалось возможным также прервать ток на доли секунды (иногда даже на несколько секунд) без на-пу1 1ения пассивности или исчезновения цвета. В таких случаях [c.90]
В таких случаях [c.90]
Толщина пленок, образовавшихся при взаимодействии металла с сухим воздухом или окислителями, различна и зависит от рода металла, характера среды, температуры и других факторов. Толщина пленок на меди и железе в обычных aт ю фepныx условиях составляет 10—30 А (А= ЫО мм). Такие пленки невидимы и настолько тонки, что метал.л сохраняет свой блеск. Наличие пленки можно установить по изменению отражательной способности поверхности металла. Так. называемые цвета побежалости на металлах обусловлены образованием пленок толщиной 400—5000 А. [c.128]
Закись железа, магнетит, а также Y-oк i6ь железа имеют кубическую кристаллическую структуру можно считать, что Рвз04 образуется из РеО удалением четверти железа (некоторые двухвалентные ионы должны стать трехвалентными, чтобы сохранить электронейтральность). Возможно дальнейшее удаление железа и получение серии твердых растворов с кубической структурой, в которых последним является -Ре Оз. Обычно полагают, что «у-окисел не стоек при высоких температурах устойчивая форма а-РеаОз, которая является главной составляющей пленки и обусловливает цвета побежалости. Эта форма окисла имеет ромбоэдрическую структуру. В результате новых электронно-дифракционных исследований, проведенных в лаборатории Коэна в Оттаве на железе, нагретом при 320° С в течение 1740 мин. в кислороде при давлении 20 мм, найдено присутствие малых количеств у-РеаОз между слоями магнетита и а-РеаОз, что позволяет пред- [c.32]
Обычно полагают, что «у-окисел не стоек при высоких температурах устойчивая форма а-РеаОз, которая является главной составляющей пленки и обусловливает цвета побежалости. Эта форма окисла имеет ромбоэдрическую структуру. В результате новых электронно-дифракционных исследований, проведенных в лаборатории Коэна в Оттаве на железе, нагретом при 320° С в течение 1740 мин. в кислороде при давлении 20 мм, найдено присутствие малых количеств у-РеаОз между слоями магнетита и а-РеаОз, что позволяет пред- [c.32]
Магнетит —фаза устойчивая даже при низких температурах и можно предполагать, что в области цветов побежалости пленки окиси железа (которые способствуют окраске, будучи совершенно прозрачными) отделяются от металла относительно непрозрачным магнетитом. Для пленок с цветами второго и более высокого порядка это имеет место, но, по-видимому, также верно и для пленок первого порядка в течение некоторого времени. Определенная окраска может быть получена длительной выдержкой при низкой температуре или меньшей выдержкой при более высокой температуре. При втором способе окрашенная пленка окиси железа обыч1 о находится непосредственно на поверхности металла [c.34]
При втором способе окрашенная пленка окиси железа обыч1 о находится непосредственно на поверхности металла [c.34]
Сцепление окисла и металла на шлифованной поверхности. Ранее проведенная работа по снятию пленки в Кембридже и более подробное исследование в Теддингтоне показали, что через тонкие пленки на железе и меди (включая те, которые дают цвета побежалости первого порядка) происходит значительное окисление металла. Под гомогенной окисной пленкой появляется смешанная зона металла и окисла. Современная работа по изучению электронной эмиссии, проведенная в Глазго, подтверждает это и указывает на удивительно глубокое проникновение смешанной зоны. Нестойкий деформированный окисел, образовавшийся под поверхностью шлифованного металла, может испускать электроны при освещении определенными длинами волн в условиях, когда относительно устойчивая пленка окисла на поверхности не способна к этому. Алюминий, шлифованный на воздухе карборундовой бумагой средней зернистости, после выдержки на воздухе в течение [c. 55]
55]
В 0,001 н. растворе, проводимость которого низка, защитное действие краев может распространяться лишь на ограниченное расстояние от них (фиг. 29, б). В 0,0001 н. растворе защищенная область становится очень узкой основная часть центральной области претерпевает изменения, но на ранней стадии коррозия, начавшись в различных точках поверхности, защищает от поражения область, непосредственно к ней примыкающую, так что каждая темная точка коррозии окружена светлым не изменившимся участком. Внеэтих участков основная часть поверхности покрыта пленками цветов побежалости, что указывает на то, что в этих местах защита недостаточна для того, чтобы помешать движению катионов железа наружу через пленку. Однако катионы движутся наружу медленно и осаждаются щелочью и кислородом, как только они выходят из поверхности металла таким образом, на поверхности металла образуется пленка, толщина которой достаточна для того, чтобы давать интерференционные окраски и защищать металл от коррозии в течение некоторого времени. [c.109]
[c.109]
Для того чтобы удостовериться в том, действительно ли жидкость, образующаяся на начальных точках коррозии, может разрушать окисную пленку, были проведены специальные опыты с образцами железа, нагретого до появления окрашивания, на котором была нанесена царапина, до частичного погружения его (царапина вертикальна) в раствор хлористого натрия. Вскоре около царапины начинался процесс коррозии и коррозионные продукты, опускаясь вниз, разрушали окисные плецки на дугообразной области. Для того чтобы это не вызывало сомнений, опыт был поставлен так, что коррозионные продукты из царапины на полупогруженном образце попадали на второй образец, помещенный под первым без электрического контакта с ним (так что сложность, обусловленная дифференциальной аэрацией, была устранена) в этом случае пленки с цветами побежалости опять исчезали в области, на которую попадали продукты коррозии, но не везде. Если продукты коррозии могут разрушить относительно толстые пленки, образующиеся при нагревании, то они определенно разрушат невидимые пленки, имеющиеся на не подвергнутых нагреву образцах. [c.112]
[c.112]
Постоянное залечивание слабых мест в пленке происходит на железе и стали в областях, где образующаяся на катоде щелочь является доминирующей одним из примеров может служить область ватерлинии частично погруженного образца, на котором возникают пленки с характерными окрасками типа цветов побежалости, но нет активной коррозии (стр. 87). Эти положения, однако, лучше показать на примере поведения капель раствора хлористого натрия или калия, помещенных на горизонтальную стальную поверхность. Распределение анодных и катодных участков удобно демонстрировать с помощью добавок к электролиту так называемого ферроксил — [c.112]
Изменения начинаются, как и на других металлах, в изолированных точках, которые более многочисленны около краев однако вместо образования свободных, плохо сцепленных с поверхностью продуктов, как это наблюдается на железе и цинке, на меди появляются овальные области ярких цветов побежалости на хорошо отшлифованных образцах и грязнокоричневые пятна на грубо отшлифованных образцах. Твердая хлористая медь, образующаяся при анодной реакции, будучи трудно растворимой, превращается тут же на месте в окись меди благодаря взаимодействию со щелочью, возникающей за счет катодной реакции и растекающейся по поверхности. Таким образом, образующаяся пленка дает характерное окрашивание. Тем временем на остальной поверхности возникают более слабые цвета, которые вызваны пленками, образованными при взаимодействии ионов одновалентной меди, двигающихся через начальную пленку в жидкость со щелочью, образующейся на катоде если это так, то это окрашивание можно рассматривать аналогично тому, которое наблюдается в районе ватерлинии на цинке или железе. [c.118]
Твердая хлористая медь, образующаяся при анодной реакции, будучи трудно растворимой, превращается тут же на месте в окись меди благодаря взаимодействию со щелочью, возникающей за счет катодной реакции и растекающейся по поверхности. Таким образом, образующаяся пленка дает характерное окрашивание. Тем временем на остальной поверхности возникают более слабые цвета, которые вызваны пленками, образованными при взаимодействии ионов одновалентной меди, двигающихся через начальную пленку в жидкость со щелочью, образующейся на катоде если это так, то это окрашивание можно рассматривать аналогично тому, которое наблюдается в районе ватерлинии на цинке или железе. [c.118]
Коррозия имеет место, если максимальная скорость доставки ингибитора меньше, чем скорость образования ионов металла в результате анодной реакции в отсутствие ингибитора. Сокращение фронта диффузии к чувствительному участку у конца менисковой щели будет, несомненно, снижать скорость доставки ингибитора, однако в такой же степени будет уменьшаться скорость миграции ионов, так как любое сокращение сечения, независимо от его геометрической формы, будет увеличивать сопротивление диффузии и электрическое сопротивление по той же причине. Таким образом, вероятность разрушений в точке, расположенной в мениске, будет точно такой, как в любой другой. Пиирс, однако, обнаружил, что особая чувствительность точек в менисковой области имеет место только в том случае, если на металле есть пленка (например, железо, нагретое до температуры, вызывающей цвета побежалости) или если электролит содержит соединения, образующие пленку (например, ингибитор). Если [c.143]
Таким образом, вероятность разрушений в точке, расположенной в мениске, будет точно такой, как в любой другой. Пиирс, однако, обнаружил, что особая чувствительность точек в менисковой области имеет место только в том случае, если на металле есть пленка (например, железо, нагретое до температуры, вызывающей цвета побежалости) или если электролит содержит соединения, образующие пленку (например, ингибитор). Если [c.143]
Как сделать цвета побежалости более яркими? — Термообработка
Если как на картинке, то точно так-же, как и на ней, при помощи фотошопа. А если вживую — тщательно подготовить поверхность. Желательно отполировать. Затем обезжирить. И уже потом греть. Получившуюся оксидную плёнку нужно защитить, иначе долго не протянет. Если получать её на предмете с картинки, тем более долго не протянет. Поскольку глюкофон имеет постоянный контакт с руками, без какого-либо защитного покрытия, оксидная плёнка на нём выдержит пару часов эксплуатации максимум. Кароче, лаком дунуть надо поверх обязательно. По идее, на издаваемых звуках тонкий слой лака сильно не отразится. По крайней мере, видел и слышал просто окрашенные эмалью — вполне себе звучат. Так-же цвета побежалости вполне можно получить химическим путём. Рецептов масса. В интернете есть целые кучи, начиная от классических патин и заканчивая японскими. Рецепты наших патин более понятны и ингредиенты для их приготовления вполне доступны. Но мне почему-то понравилось несколько именно японских рецептов. К сожалению, этим вопросом занимался очень давно, конкретных рецептур по памяти не вспомню. Но было дело, доводилось получать на полированной стали фиолетовые оттенки, так по какому-то японскому рецепту поверхность получалась не просто фиолетовой, а очень насыщенно фиолетовой, аж бархатистой. Выглядело весьма эпично, результат меня тогда сильно впечатлил. В америкосии это даже целое направление хобби у людей. Кто-то марки собирает, кто-то модельки корабликов клеит, а кто-то целыми днями всякие металлы во всякую химию макает и результатам радуется.
Кароче, лаком дунуть надо поверх обязательно. По идее, на издаваемых звуках тонкий слой лака сильно не отразится. По крайней мере, видел и слышал просто окрашенные эмалью — вполне себе звучат. Так-же цвета побежалости вполне можно получить химическим путём. Рецептов масса. В интернете есть целые кучи, начиная от классических патин и заканчивая японскими. Рецепты наших патин более понятны и ингредиенты для их приготовления вполне доступны. Но мне почему-то понравилось несколько именно японских рецептов. К сожалению, этим вопросом занимался очень давно, конкретных рецептур по памяти не вспомню. Но было дело, доводилось получать на полированной стали фиолетовые оттенки, так по какому-то японскому рецепту поверхность получалась не просто фиолетовой, а очень насыщенно фиолетовой, аж бархатистой. Выглядело весьма эпично, результат меня тогда сильно впечатлил. В америкосии это даже целое направление хобби у людей. Кто-то марки собирает, кто-то модельки корабликов клеит, а кто-то целыми днями всякие металлы во всякую химию макает и результатам радуется. Погуглите, мне когда-то пара форумов попадалась буржуйских, где они там своими результатами по этой теме делятся и рецептуру выкладывают. В основном конечно народ забавляется с цветными металлами, ну, или например оксидирование титана (как и его анодирование) шибко развиты, но если хорошо порыться, то и для стали рецептов хватает. Или скачайте книжку какую-нибудь. Например:
Погуглите, мне когда-то пара форумов попадалась буржуйских, где они там своими результатами по этой теме делятся и рецептуру выкладывают. В основном конечно народ забавляется с цветными металлами, ну, или например оксидирование титана (как и его анодирование) шибко развиты, но если хорошо порыться, то и для стали рецептов хватает. Или скачайте книжку какую-нибудь. Например:
|
Для закаливания детали она нагревается до высокой температуры, затем идет процесс охлаждения в специализированных для обрабатываемых изделий средах. Результат зависит от заданного режима закалки, разные режимы позволяют получить различные свойства обрабатываемого металла. Данный процесс должен обеспечить повышение высокопрочных и твердых свойств металла. Следует заметить, что при закаливании сталь обретает твердость, но при этом она становится более хрупкой. Для эффективных результатов, деталь равномерно нагревают до температуры 740-850°С, после этого быстро охлаждают до 400-450°С. Охлаждает со скоростью не менее 150°С в секунду, период времени охлаждения приблизительно 2-3 с. Следующий шаг охлаждения идет с пониженной температурой 300°С, протекает при разной скорости. В качестве охлаждающих сред применяют воду и трансформаторное масло. Жидкости имеют различия между собой по скорости охлаждения и температуре, в воде скорость охлаждения больше — до 600°С в секунду, а в масле она оказывается до 150°С в секунду. Высокая критическая точка нагрева детали придает стали крупнозернистую структуру, что в результате приводит к неожиданным последствиям: возникновению трещин, коробление и деформации. Аналогично к тем же действиям приводит чрезмерно быстрое охлаждение. При закаливание агрегатов и инструментов, используются печи для закалки, их можно подразделить на: камерные или пламенные, где данное изделие накаляется при помощи пламени. А так же на электрические муфельные это печи-ванны, которые представляют собой тигли, заполненные сплавами солей, (например хлористым барием). Есть разница между жидкими и воздушными средами, так как накаливание в жидких средах идет в два раза быстрее, чем в воздушной среде, а у сплава металла в четыре раза быстрее. К примеру для закаливание стальных деталей малого размера, используют сплав свинца. Изделия опускают в ванны и затем накладывают древесный уголь, при процессе плавления свинца на поверхности вспыхивает восстанавливающее пламя в результате свинец не окисляется. В современной промышленности, применяют электрические токи с высокой частотой. Обрабатываемую током заготовку вставляют в специальный индуктор, по которой идет ток с высокой частотой, далее изделие моментально нагревается до заданной температуры. Определенно, побежалые цвета, появляются одинаково на двух видах стали, как на сырой, так и на закаленной. Для закаливания инструментов при отпуске, используют два метода: 1) После закалки поверхность инструмента, начинают шлифовать мелкой наждачной бумагой, после этого инструмент нагревают, затем на чистой и гладкой поверхности, появляются цвета побежалости. Если появляется необходимый цвет, то изделие накаляют до заданной температуры, далее идет процесс охлаждения в воде. Что бы следить за переменой цветов необходимо внимание и зрительная память, так как при перемене некоторых оттенков цветов идет быстрое изменение. 2) В процессе закаливания некоторых инструментов (чеканов, штихелей, резцов, молотков) для закаливания необходима, только рабочая площадь, а инструмент не закаливается, остается в сыром виде. Данный метод применяют в процессе отпуска тонких стальных инструментов(кос, пил и т. д). При нагревательном процессе стальных деталей идет реакция окисления и обезуглероживание. Получение на поверхности окалины идет за счет образования оксидов железа. |
Самый простой способ воронения стали в разные оттенки
Воронение стали позволяет создать защитное покрытие, препятствующее коррозии, которое к тому же обладает хорошими декоративными качествами. Если оно сделано правильно, то имеет большую стойкость, чем краски, поэтому может применяться на трущихся поверхностях. Рассмотрим, как можно сделать воронение в домашних условиях различных оттенков: золотистого, с синевой и классического черного.
Что потребуется:
- газовая горелка;
- растворитель;
- емкость с водой;
- емкость с отработкой.
Процесс воронения
Заготовку для воронения нужно хорошо отшлифовать, чтобы она была гладкой, и обезжирить ее растворителем. Затем деталь цепляется крючком из проволоки и равномерно прогревается газовой горелкой. В местах утолщения металла, ее стоит греть дольше.

Если в момент появления на стали золотистого цвета побежалости окунуть ее в воду, то такой благородный налет сохраниться.
Это тончайший достаточно легко снимаемый слой воронения с отличными декоративными качествами. Если покрыть такую заготовку прозрачным лаком, то она будет выглядеть красиво и точно не поржавеет.
Если прогреть заготовку дольше, пока под факелом паяльника не начнет проявляться синева, и также ее остудить в воду, то получим более стойкое и очень красивое воронение. Однако оно также нуждается в дополнительном лакировании.
Наиболее стойкого воронения можно добиться нагрев деталь до равномерного серого цвета побежалости, чтобы он проявился по всей поверхности.
Такая заготовка окунается в переработку.
Затем ее нужно вытащить и погреть горелкой, чтобы масло окончательно запеклось и среагировало со сталью. В результате заготовка станет черной матовой. Если повторно ее окунуть в отработку и подсушить горелкой, то цвет станет глубже.
 Этот слой воронения не нуждается в лакировании. Сквозь него металл не поржавеет.
Этот слой воронения не нуждается в лакировании. Сквозь него металл не поржавеет.При воронении важно не перегревать деталь больше, чем до серой побежалости. В противном случае металл отпустится, станет мягче и потеряет свои изначальные свойства.
Смотрите видео
7+ умных способов очистить потускневший металл
Ювелирные изделия из серебра, латуни, нержавеющей стали и других металлов ошеломляют, когда они новые и сияют своим первоначальным цветом и блеском. Со временем эти металлические предметы тускнеют и становятся неприглядными. Узнайте, как очистить потускневшие металлические поверхности, чтобы вернуть вашим любимым предметам их первоначальный вид.
Металлы подвержены воздействию условий окружающей среды по мере старения, что приводит к обесцвечиванию поверхности. Этот темный цвет на ваших любимых металлических предметах является результатом потускнения.
Этот темный цвет на ваших любимых металлических предметах является результатом потускнения.
К счастью, потускнение влияет только на внешний слой металла, и его легко очистить с помощью простых ингредиентов. Патину, коричневую или зеленую пленку, которая образуется на поверхности металла в результате окисления, легко удалить.
Однако полировка металла неподходящими чистящими средствами или слишком частая полировка повреждает поверхность металла. Важно знать, какие чистящие средства безопасны, а какие наиболее эффективны.
(дгемма/123рф.ком)В то время как для различных типов металлов требуются специальные чистящие средства, многие основные чистящие средства удаляют потускнение с большинства типов металлов. Мы покажем вам, как чистить эти поверхности, используя как основные, так и расширенные методы очистки.
Основные способы очистки потускневшего металла
Перед удалением стойких потускнений, независимо от того, пытаетесь ли вы удалить потускнение с алюминия или серебра, обязательно очистите металлическое изделие с помощью основного чистящего средства.
Одним из самых простых способов очистки потускневшего металла является мыльная вода, которая также является лучшим способом очистки поддельных украшений. Если ваши металлические предметы слегка почернели и загрязнились, начните с этого простого чистящего средства.
TB1234
Базовая металлическая уборка
- теплые воды
- мыло для блюда
- Большой пластиковый контейнер
- мягкой губки
- ткань микрофибры
TB1234
Наполните большую пластиковую корзину или контейнер теплой или горячей водой и добавьте пару капель средства для мытья посуды.Перемешайте воду ложкой или руками, чтобы получился мыльный раствор.
Поместите металлические предметы в мыльную воду, чтобы погрузить их на 15 минут. Не погружайте их слишком надолго, чтобы не повредить металлическую поверхность.
№ Используйте мягкую губку, чтобы протереть каждый элемент и тщательно промыть их чистой водой. Протрите каждую часть мягкой тканью.
Протрите каждую часть мягкой тканью.
Очистка потускневшего металла с помощью белого уксуса
Хотя белый уксус является лучшим средством для потускнения латуни, он также является отличным решением для очистки потускневших металлических поверхностей, таких как нержавеющая сталь, олово, медь и бронза.
TB1234
Уксус Tarnish Remover
- 1 чашка белого уксуса
- 1 стакан теплой воды
- пластиковая чаша
- зубная щетка
- мягкая ткань
TB1234
Налейте теплую воду и уксус в большое пластиковое ведро или ванну и перемешайте. Окуните зубную щетку в жидкость и нанесите раствор на потускневшие участки металла. Таким же образом можно почистить украшения уксусом.
Мягкая, гибкая щетина щетки, смешанная с кислотой уксуса, разрыхляет и удаляет грязь и тусклость. Продолжайте очищать зубной щеткой поверхность круговыми движениями и наносите больше жидкости по мере необходимости.
№ Промойте теплой водой и тщательно высушите мягкой сухой тканью. Осмотрите деталь на предмет оставшегося потускнения и при необходимости повторите процесс очистки.
Как очистить потускневший металл самодельной пастой
Эта смесь белого уксуса, соли и муки представляет собой идеальную пасту для чистки сильно потускневших вещей.Уксус также является хорошим решением для создания домашнего средства для удаления потускнения нержавеющей стали.
TB1234
DIY Tarnish Remover Paste
- 1/2 чашки белый уксус
- 1/4 чашки муки
- 1 чайной ложки соли
- пластиковая шара
- вода
- полотенце
TB1234
Сделайте густую пасту, добавив уксус, муку и соль в маленькую пластиковую миску. Нанесите пасту на потускневший предмет или на чистые кольца из нержавеющей стали и оставьте на десять минут.
Смойте засохшую уксусную пасту и удалите с предмета потускнения, подержав его под чистой проточной водой, и высушите мягким полотенцем из микрофибры.
Очистка потускневшего металла лимоном и солью
Если у вас дома нет дистиллированного уксуса, попробуйте использовать средство для удаления потускнения с лимоном и солью. Лимонный сок с высоким содержанием лимонной кислоты действует как кислое средство, безопасно устраняя потускнение, в то время как соль является мягким абразивом для мягкого удаления грязи.
tb1234
Лимонная соль
- Лимон
- 1 чайная ложка соли
- Вода
- Мягкая ткань
2
Покатайте целый лимон по прилавку примерно 30 секунд, а затем разрежьте его пополам.Растирание разрушает мембраны лимона, делая его более сочным.
Поместите вторую половинку лимона в полиэтиленовый пакет и храните его в холодильнике для последующего использования. Посыпьте солью срез лимона и протрите им потускневший металл так же, как вы пользуетесь губкой для мытья посуды.
Периодически сжимайте лимон, чтобы выпустить больше сока. Промойте металлический предмет под чистой водой и высушите его мягкой чистой тканью.
Промойте металлический предмет под чистой водой и высушите его мягкой чистой тканью.
Удаление налета с металла с помощью пищевой соды
Пищевая сода и лимонный сок — это натуральные ингредиенты, которые прекрасно удаляют потускнение с металлических поверхностей, таких как серебро, оставляя полированную поверхность, а также являются ингредиентами для удаления ржавчины.
tb1234
Натуральное средство для удаления потускнения
- 2 чайные ложки пищевой соды
- Лимон
- Вода
- Бумажное полотенце
Прокатите рукой лимон по твердой поверхности, чтобы выпустить сок, и разрежьте его пополам. Насыпьте пищевую соду на одну половину лимона, а вторую половину положите в пластиковый пакет в холодильник, чтобы использовать позже.
Используйте половинку лимона так же, как и губку для мытья посуды, и протрите ею потускневший участок металла.Пройдитесь по поверхности несколько раз, чтобы убедиться, что потускнение исчезло.
Держите деталь под проточной водой и пальцами удалите всю пищевую соду из металлических щелей и промокните ее насухо бумажными полотенцами.
Как удалить тусклость с столового серебра
Все мы ежедневно пользуемся столовым серебром, и потускневшая вилка или ложка не очень привлекательны, когда мы пытаемся насладиться едой. Вот как очистить посеребренные изделия из серебра и стерлингового серебра, чтобы удалить потускнение за считанные минуты.
TB1234
серебро Tarnish Remover
- алюминиевая фольга
- проперотки
- 2 кварта воды
- 1 чашка пищевой сода
- Saucepan
TB1234
Выстелите дно противня, достаточно большого, чтобы вместить все ваше потускневшее серебро. Поместите столовое серебро на фольгу и равномерно посыпьте пищевую соду сверху кусочков. Налейте в кастрюлю около двух литров воды и доведите до кипения.
Залейте столовое серебро кипятком, чтобы оно было покрыто. Потускнение исчезает по мере остывания воды. Удалите кусочки серебра и высушите их мягкой тканью.
Потускнение исчезает по мере остывания воды. Удалите кусочки серебра и высушите их мягкой тканью.
Использование обычных предметов домашнего обихода для очистки потускневшего металла
Белый уксус, алюминиевая фольга и пищевая сода являются одними из наиболее очевидных средств для очистки металла от потускнения, но что, если у вас нет этих предметов дома? Вот пара предметов повседневного обихода, которые отлично заменят средство для удаления тусклости.
TB1234
Краткое удаление Tarnish Remover
- кетчуп
- Зубная паста
- Зубная щетка
- Вода
- Мягкая ткань
- Мягкая ткань
TB1234
Нанесите каплю зубной пасты на потускневший участок металла. Попробуйте использовать зубную пасту, содержащую пищевую соду, для достижения наилучших результатов. Используйте старую зубную щетку, чтобы потереть металл круговыми движениями и обязательно проникнуть в закоулки.
Тщательно промойте предмет чистой водой и осмотрите его на наличие следов потускнения. При необходимости повторите и высушите металл мягкой тканью.
При необходимости повторите и высушите металл мягкой тканью.
Если вы предпочитаете использовать кетчуп для очистки металла, нанесите слой соуса на металлическую поверхность и оставьте минимум на 30 минут. Уксусная кислота в кетчупе разрушает тусклость, чтобы ее было легко удалить.
№ Используйте зубную щетку с мягкой щетиной, чтобы почистить металлическую поверхность легкими круговыми движениями. Держите металлическую деталь под проточной водой, пока она не станет чистой, и вытрите ее мягкой тканью.
Использование коммерческих чистящих средств для металлов для удаления потускнения
Если у вас нет терпения или времени на очистку металлических изделий самодельным раствором или полиролью для металла, приобретаемые в магазине чистящие средства для металла — это безопасная и простая альтернатива для восстановления металлических поверхностей.
TB1234
коммерческий металлический очиститель
- Water
- блюдо мыла
- коммерческий металлический очиститель и полировщик
- мягкая ткань
- ткань микрофибры
TB1234
Выберите чистящее средство, предназначенное для очистки латуни, меди или других металлов, и следуйте инструкциям на этикетке. Начните с очистки предмета теплой водой и моющим средством для посудомоечной машины, чтобы удалить пыль и мусор. Если предмет не слишком грязный, протрите его влажной тряпкой.
Начните с очистки предмета теплой водой и моющим средством для посудомоечной машины, чтобы удалить пыль и мусор. Если предмет не слишком грязный, протрите его влажной тряпкой.
Используйте мягкую ткань, чтобы нанести очиститель и протереть металл зерном, чтобы удалить потускнение. Промойте деталь под проточной водой и насухо протрите тканью из микрофибры.
Время имеет свойство обесцвечивать металлические поверхности, а коричнево-зеленая патина оставляет желать лучшего. В то время как эти металлические детали легко очистить с помощью коммерческого чистящего средства, некоторые домашние средства легко удаляют потускнение, и многие из них удивительны.
(dgemma/rigsby8131/123rf.com) Теперь, когда вы знаете, как почистить потускневший металл, чтобы вернуть вашим любимым металлическим предметам их первоначальный блеск и сияние, почему бы не поделиться нашими решениями по очистке потускневшего металла со своей семьей и друзьями на Facebook и Pinterest?
Почему на моей коже тускнеют украшения? (Reasons & Solutions 2022)
Если вы носите украшения и обнаруживаете, что ваша кожа обесцвечивается, это может сильно беспокоить новичка. Реальность такова, что вам нечего бояться. Однако, если это ваше повседневное явление, может быть довольно неприятно очищать кожу, чтобы удалить цвет с вашей кожи. Два цвета, которые появляются на коже, — зеленый или черный, оба неприглядны.
Реальность такова, что вам нечего бояться. Однако, если это ваше повседневное явление, может быть довольно неприятно очищать кожу, чтобы удалить цвет с вашей кожи. Два цвета, которые появляются на коже, — зеленый или черный, оба неприглядны.
В этой статье мы рассмотрим, что вызывает это почернение или обесцвечивание.
Почему моя кожа тускнеет на украшениях? ( 4 основные причины) Ниже приведены некоторые из причин, по которым ваша кожа может потускнеть на украшениях, которые вы носите.
1. Коррозия Коррозия металла является одной из причин, и, возможно, основной, почему на коже есть цветопередача. Берите пример с золота. Чистое золото не подвергается коррозии, но оно слишком мягкое для изготовления украшений; это исходное состояние. Подходит только для торговли. По этой причине вы обнаружите, что золото сплавляется с другими металлами, которые имеют тенденцию к эрозии. Золото не подвергается коррозии, но корродировать будут сплавы, и это при более темном цвете.
Золото не подвергается коррозии, но корродировать будут сплавы, и это при более темном цвете.
Основной причиной коррозии является ношение украшений во влажных условиях. Существует также оставлять его влажным на коже в течение длительного времени. Если вымоете руки и не будете сушить место, где украшения соприкасаются с кожей, через некоторое время вы обнаружите, что коррозия произойдет.
Поэтому вам не рекомендуется принимать душ или плавать в бассейне или океане с украшениями. Очень немногие металлы могут противостоять соленой воде. Вот почему вы обнаружите, что серебряные сплавы и медь будут подвергаться коррозии в присутствии соли, даже из продуктов, которые мы едим, таких как попкорн и картофельные чипсы.
Еще одна проблема возникает, если вы потеете естественным образом, как и все мы. Наша кожа имеет потовые железы, которые химически выделяют жиры и жирные кислоты. Их достаточно, чтобы вызвать реакцию с металлом и облегчить коррозию. Чтобы предотвратить это, вы можете использовать абсорбирующую пудру без оксида цинка на участках, которые соприкасаются с кожей.
2. Металлическое истирание Черная как смоль пыль, появляющаяся на руке, возникает из-за так называемого металлического истирания.Это заслуга макияжа, который мы носим. Вы обнаружите, что соединения, содержащиеся в косметике, тверже, чем украшения.
При их соприкосновении происходит трение, в результате чего металл стирается. Если вам интересно, почему не меняется цвет используемого металла, например, золота или серебра, то это потому, что мелкодисперсный металл становится черным, а не металлическим. Затем пятно появляется, когда металл вступает в контакт с кожей или даже одеждой.
Если вы хотите полностью избежать этого, убедитесь, что кожа, с которой соприкасаются ваши украшения, очищена водой с мылом и очищена от макияжа.Если вы не можете избежать этого, убедитесь, что макияж, лосьоны и духи, которые вы наносите, высохли на руках, прежде чем надевать украшения. Вы хотите предотвратить истирание любой ценой.
3. Химические реакции Такой металл, как стерлинговое серебро, имеет тенденцию тускнеть по целому ряду причин. Одним из них является воздействие соединений серы. В целом, воздействие атмосферы, где он вступает в реакцию с сероводородом в воздухе, также является еще одной причиной коррозии стерлингового серебра.
Вы обнаружите, что этот комплекс представляет собой загрязненный воздух, в котором мы все в основном живем в настоящее время. Другие острые продукты, такие как лук, рыба и яйца, могут привести к воздействию сероводорода.
Когда вы смотрите на потускневшее стерлинговое серебро, оно обычно черного или тускло-серого цвета. Вы обнаружите, что цвет будет переходить на вашу кожу или одежду, когда вы носите украшения.
Те, у кого влажная кожа, обнаружат, что их кожа окрашивается в зеленый цвет, когда они носят стерлинговое серебро. Это благодаря меди, используемой для сплава стерлингового серебра.
4. Химия тела Как уже упоминалось, организм выделяет химические вещества, которые в конечном итоге вступают в реакцию с металлом. До сих пор мы упоминали жиры и жирные кислоты. Что-то еще, что присутствует на нашей коже, когда мы потеем, — это сера или сульфиды и аминокислоты.
Пот также является кислотой, которая при взаимодействии с телом вызывает обесцвечивание кожи и украшений. Если вы много потеете, то обнаружите, что сохранить ваши украшения в этом новом состоянии будет сложнее, чем вам хотелось бы.
Если в последнее время вы стали замечать, что ваша кожа тускнеет на украшениях, чего раньше не было, то, вероятно, в вашем организме происходят какие-то изменения. Гормональные изменения и некоторые лекарства могут изменить химический состав организма и привести к потускнению кожи.
Это связано с избыточным образованием кислоты, которая затем вступает в реакцию с металлом. Когда жарко или влажно, вы можете отказаться от ношения украшений. В качестве альтернативы вы можете носить абсорбирующие средства, не содержащие оксида цинка, чтобы ваша кожа оставалась сухой.
В качестве альтернативы вы можете носить абсорбирующие средства, не содержащие оксида цинка, чтобы ваша кожа оставалась сухой.
Как решить проблему ? Помимо упомянутого абсорбирующего порошка, вы можете сделать еще многое другое. Лучший способ решить эту проблему с самого начала — приобрести украшения с родиевым покрытием, устойчивым к коррозии.
Можно также использовать лак или лак для ногтей для покрытия внутренней части украшения. Вам придется делать это регулярно, потому что он исчезает, но это того стоит. Он защищает как украшения, так и вашу кожу.
Другие методы, такие как снятие украшений при работе с химическими веществами (лосьонами, моющими средствами, хлором и т. д.), помогут сохранить украшения дольше.
Кроме того, когда вы наденете их, вы можете очистить их водой с мягким мылом. Тщательно высушите, а затем храните в герметичном пакете с силиконовым гелем, чтобы впитать влагу. Если вы носите изделие ежедневно, регулярно чистите его, чтобы оно оставалось новым и не содержало химикатов.
Если вы носите изделие ежедневно, регулярно чистите его, чтобы оно оставалось новым и не содержало химикатов.
Ребята, больше полезных советов смотрите здесь и здесь.
Увидимся в следующем посте!
Тайгер любит моду и украшения. Он также является производителем модных ювелирных изделий, который помогает тысячам малых предприятий расти, а также ведет дела с некоторыми крупными брендами модных ювелирных изделий. Он настоящий эксперт по металлу, и он поделится некоторой информацией, которую вы ищете.
Эй! Наконец-то я нахожу ответ!
Руководство по ювелирным металлам | Zales
Не может быть изысканных украшений без металлов, а разнообразие доступных металлов позволяет сделать украшения доступными практически для всех.
Zales предлагает украшения, изготовленные из традиционных металлов, таких как золото , серебро и платина , а также современные металлы, такие как вольфрам , нержавеющая сталь, титан и другие. Вот взгляд на металлы, используемые в ювелирных изделиях сегодня.
Вот взгляд на металлы, используемые в ювелирных изделиях сегодня.
Золотые украшения
Хорош как золото — почти ничего. Вечный выбор для всех видов ювелирных изделий. Золото легче всего поддается обработке из всех металлов, потому что оно очень пластично. Чтобы создать прочные и долговечные украшения, чистое золото сплавляют с другими металлами, такими как медь или цинк, для придания прочности и цвета.
Zales обычно использует в своих украшениях желтое, розовое и белое золото. Вот что отличает каждый тип:
Желтое золото
Золото имеет естественный желтый цвет, но при добавлении серебра или меди его естественная теплота усиливается .
Количество чистого золота в украшениях зависит от его пробы. Чем выше карат, тем выше чистота, но и ниже долговечность. Вот почему большинство украшений из желтого золота — это 14-каратное или 18-каратное золото.
Желтое золото также является самым гипоаллергенным из всех видов золота.
Розовое золото
A блестящий розовый металл , розовое золото может иметь оттенки от красной розы до розового золота. Для создания розового цвета розового золота чистое золото сочетается с медью и серебром . Чем больше меди добавлено в сплав, тем розовее будет золото.
Розовое золото не нужно окунать или покрывать, так как цвет чистый .Он не считается гипоаллергенным и требует большей полировки, чем другие виды золота, чтобы сохранить свой блеск.
Белое золото
Для создания бело-серебряного цвета золото смешивают с палладием и серебром или с никелем, медью и цинком. Белое золото также необходимо покрыть платиной или родием для улучшения белизны и придания прочности и блеска .
Ювелирные изделия из белого золота иногда необходимо повторно окунать после того, как покрытие стирается.
Золотой карат
Чтобы определить пробу золота, используемого в ювелирном изделии, проверьте его маркировку, также называемую его клеймом . Обычно это находится на внутренней стороне стержня или обратной стороне кулона, серьги или браслета. Вот что нужно искать:
Обычно это находится на внутренней стороне стержня или обратной стороне кулона, серьги или браслета. Вот что нужно искать:
-каратное золото Проба
Мера в каратах Клейма Твердость Чистота золота 24 карата — Самый мягкий 100% 22 карата 916/22К Мягче 91.6% 18 карат 750/18К Средний 75,0% 14 карат 585/14К Сильнее 58,8% 10 карат 417/10К Самый сложный 41,7%
Ювелирные изделия из платины
Редкая и драгоценная платина — ярко-белый металл , в тридцать раз более редкий, чем золото.Он очень прочный, не тускнеет и гипоаллергенен. Он блестящий, красивый и прослужит не одно поколение — отличный выбор для ювелирных украшений.
Из-за своей прочности и твердости сложные гравюры могут выглядеть четче и точнее из платины, а белый вид металла делает его идеальным для демонстрации бриллиантов и драгоценных камней.
При использовании в ювелирных изделиях его обычно смешивают с аналогичными металлами — иридием, палладием, рутением, родием или осмием.Чтобы ювелирное изделие было помечено как платиновое, оно должно иметь чистоту не менее 90% платины . Ищите клеймо «PLAT» , отштампованное на внутренней стороне хвостовика (кольца) или на задней части изделия.
Ювелирные изделия из стерлингового серебра
Когда-то считавшееся даже более ценным, чем золото, сегодня серебро является самым доступным из всех драгоценных металлов. Поскольку чистое серебро слишком мягкое для изготовления ювелирных изделий, его смешивают с медью или другим металлом, чтобы получить стерлинговое серебро, которое более прочно.
Стерлинговое серебро должно содержать серебро чистоты не менее 92,5% , поэтому оно имеет штамп .925 . Вы можете найти этот отличительный знак на внутренней стороне стержня кольца из стерлингового серебра или на задней части ювелирных изделий.
Серебро пробы может варьироваться от ярко-белого до серовато-белого и может иметь матовую или блестящую поверхность. Серебро легко тускнеет и царапается, поэтому всегда храните украшения из стерлингового серебра в пакетах для предотвращения потускнения и в прохладном, сухом месте.
Ювелирные изделия из альтернативных металлов
В дополнение к трем большим металлам — платине, золоту и серебру — современный вариант пробивается на ювелирную сцену. Они особенно популярны среди мужчин, которым нравится легкий вес и дополнительная прочность . Вот некоторые из наших любимых:
Кобальт
Украшения из кобальта сделаны из того же материала, который используется для изготовления двигателей реактивных самолетов и хирургических инструментов. Это тверже, чем нержавеющая сталь , и поэтому ее труднее поцарапать.
Это тверже, чем нержавеющая сталь , и поэтому ее труднее поцарапать.
Хотя кобальт не на 100% устойчив к царапинам, он намного тверже титана и всех других драгоценных металлов, включая платину, золото и серебро. Он также гипоаллергенен.
Нержавеющая сталь
Нержавеющая сталь вышла за пределы кухни и стала желанным металлом в часах и ювелирных изделиях. Нержавеющая сталь серебристо-белого цвета с зеркальной поверхностью и слоем хрома, очень хорошо сохраняет свой блеск и цвет и устойчива к потускнению.
Нержавеющая сталь, один из самых прочных металлов, хорошо противостоит износу и разрыву, что делает ее отличным выбором, когда образ жизни или работа требуют повышенной прочности.
Титан
Титан так же прочен, как сталь, но на 45% легче по весу . Фактически, он имеет самое высокое отношение прочности к весу среди всех металлов.
Он похож на платину по своей устойчивости к потускнению — вот что делает его разумным выбором для космических кораблей, а также для украшений, особенно для предметов, которые носят каждый день.
Титан универсальный , легкий , гипоаллергенный и устойчивый к коррозии , с металлическим цветом, который может меняться от белого до темного и цветного в зависимости от способа обработки.
Вольфрам
Вольфрам очень тяжелый, серо-белого цвета с блестящей поверхностью. Этот гипоаллергенный металл имеет самую высокую температуру плавления и самую высокую прочность из всех металлов — по-шведски это означает «тяжелый камень».» Из-за своей твердости блеск сохраняется долго.
Выбор подходящего металла
Несколько факторов, которые следует учитывать при выборе металла для ваших украшений:
Внутренняя ценность
Базовая стоимость. Цены на металлы колеблются ежедневно в зависимости от спроса и предложения. Чем более редкий и драгоценный металл, тем меньше его доступность. Редкость может стимулировать спрос , благодаря чему редкий металл, такой как платина или золото , с большей вероятностью сохранит свою ценность с течением времени.
Срок службы
Учитывайте способность металла выдерживать ежедневный износ, а также долговечность его модного вида. Например, хотя вольфрам и очень прочный, он не считается драгоценным металлом.
Гипоаллергенность
Гипоаллергенные металлы сводят к минимуму возможность раздражающей аллергической реакции. Более чистые металлы, такие как платина и титан , как правило, гипоаллергенны, что создает небольшой риск потенциального раздражения.
Прочность
Все металлы царапаются и даже иногда вмятины. Однако некоторые металлы, такие как титан и вольфрам , устойчивы к царапинам.
Коэффициент восстановления
Можно ли восстановить металл, чтобы ваши украшения выглядели как новые? Некоторые металлы можно легко восстановить. Другие, хотя и долговечные и прочные, могут не справиться с процессом восстановления или изменения размеров.
Редкость
Чем реже металл, тем дороже он будет.Поэтому изделия из платины и золота , как правило, будут дороже, чем из других металлов.
Подъем
Некоторым нравится ощущение веса украшений, в то время как другие предпочитают чувствовать, что на них вообще ничего нет. Платина — самый плотный и тяжелый металл — на 40% тяжелее золота . Титан и нержавеющая сталь являются одними из самых легких.
Заботиться Полировать, мыть или полировать? Вот все, что вам нужно знать об уходе за металлическими украшениями.
Один цвет, очень разные металлы
Выстройте кучу украшений издалека, и самое простое различие, которое вы сможете провести, это между серебром и золотом.
В то время как выбор между этими двумя оттенками в основном зависит от стиля и предпочтений, выбор конкретного типа металлических украшений требует немного больше усилий.
Допустим, вы решили приобрести украшения серебристого цвета. Вы действительно хотите серебро? Или, может быть, платина? Читайте дальше, чтобы узнать о различиях между серебряными и платиновыми украшениями.
Платина против серебра Давайте сначала рассмотрим различия во внешнем виде.
Хотя на первый взгляд и серебро, и платина кажутся серебристыми, на самом деле эти два металла легко различимы невооруженным глазом. Оба имеют серый подтон, в отличие от белого золота, которое имеет более теплый желтый оттенок, но платина намного ярче и блестит, а серебро имеет более тусклый серый цвет .
Долговечность
 Протрите каждую часть мягкой тканью.
Протрите каждую часть мягкой тканью.

 Промойте металлический предмет под чистой водой и высушите его мягкой чистой тканью.
Промойте металлический предмет под чистой водой и высушите его мягкой чистой тканью.
- алюминиевая фольга
- проперотки
- 2 кварта воды
- 1 чашка пищевой сода
- Saucepan
TB1234
Выстелите дно противня, достаточно большого, чтобы вместить все ваше потускневшее серебро. Поместите столовое серебро на фольгу и равномерно посыпьте пищевую соду сверху кусочков. Налейте в кастрюлю около двух литров воды и доведите до кипения.
Залейте столовое серебро кипятком, чтобы оно было покрыто. Потускнение исчезает по мере остывания воды. Удалите кусочки серебра и высушите их мягкой тканью.
Потускнение исчезает по мере остывания воды. Удалите кусочки серебра и высушите их мягкой тканью.
Использование обычных предметов домашнего обихода для очистки потускневшего металла
Белый уксус, алюминиевая фольга и пищевая сода являются одними из наиболее очевидных средств для очистки металла от потускнения, но что, если у вас нет этих предметов дома? Вот пара предметов повседневного обихода, которые отлично заменят средство для удаления тусклости.
TB1234
Краткое удаление Tarnish Remover
- кетчуп
- Зубная паста
- Зубная щетка
- Вода
- Мягкая ткань
- Мягкая ткань
TB1234
Нанесите каплю зубной пасты на потускневший участок металла. Попробуйте использовать зубную пасту, содержащую пищевую соду, для достижения наилучших результатов. Используйте старую зубную щетку, чтобы потереть металл круговыми движениями и обязательно проникнуть в закоулки.
Тщательно промойте предмет чистой водой и осмотрите его на наличие следов потускнения. При необходимости повторите и высушите металл мягкой тканью.
При необходимости повторите и высушите металл мягкой тканью.
Если вы предпочитаете использовать кетчуп для очистки металла, нанесите слой соуса на металлическую поверхность и оставьте минимум на 30 минут. Уксусная кислота в кетчупе разрушает тусклость, чтобы ее было легко удалить.
№Используйте зубную щетку с мягкой щетиной, чтобы почистить металлическую поверхность легкими круговыми движениями. Держите металлическую деталь под проточной водой, пока она не станет чистой, и вытрите ее мягкой тканью.
Использование коммерческих чистящих средств для металлов для удаления потускнения
Если у вас нет терпения или времени на очистку металлических изделий самодельным раствором или полиролью для металла, приобретаемые в магазине чистящие средства для металла — это безопасная и простая альтернатива для восстановления металлических поверхностей.
TB1234
коммерческий металлический очиститель
- Water
- блюдо мыла
- коммерческий металлический очиститель и полировщик
- мягкая ткань
- ткань микрофибры
TB1234
Выберите чистящее средство, предназначенное для очистки латуни, меди или других металлов, и следуйте инструкциям на этикетке. Начните с очистки предмета теплой водой и моющим средством для посудомоечной машины, чтобы удалить пыль и мусор. Если предмет не слишком грязный, протрите его влажной тряпкой.
Начните с очистки предмета теплой водой и моющим средством для посудомоечной машины, чтобы удалить пыль и мусор. Если предмет не слишком грязный, протрите его влажной тряпкой.
Используйте мягкую ткань, чтобы нанести очиститель и протереть металл зерном, чтобы удалить потускнение. Промойте деталь под проточной водой и насухо протрите тканью из микрофибры.
Время имеет свойство обесцвечивать металлические поверхности, а коричнево-зеленая патина оставляет желать лучшего. В то время как эти металлические детали легко очистить с помощью коммерческого чистящего средства, некоторые домашние средства легко удаляют потускнение, и многие из них удивительны.
(dgemma/rigsby8131/123rf.com)Теперь, когда вы знаете, как почистить потускневший металл, чтобы вернуть вашим любимым металлическим предметам их первоначальный блеск и сияние, почему бы не поделиться нашими решениями по очистке потускневшего металла со своей семьей и друзьями на Facebook и Pinterest?
Почему на моей коже тускнеют украшения? (Reasons & Solutions 2022)
Если вы носите украшения и обнаруживаете, что ваша кожа обесцвечивается, это может сильно беспокоить новичка. Реальность такова, что вам нечего бояться. Однако, если это ваше повседневное явление, может быть довольно неприятно очищать кожу, чтобы удалить цвет с вашей кожи. Два цвета, которые появляются на коже, — зеленый или черный, оба неприглядны.
Реальность такова, что вам нечего бояться. Однако, если это ваше повседневное явление, может быть довольно неприятно очищать кожу, чтобы удалить цвет с вашей кожи. Два цвета, которые появляются на коже, — зеленый или черный, оба неприглядны.
В этой статье мы рассмотрим, что вызывает это почернение или обесцвечивание.
Почему моя кожа тускнеет на украшениях? ( 4 основные причины)
Ниже приведены некоторые из причин, по которым ваша кожа может потускнеть на украшениях, которые вы носите.
1. Коррозия Коррозия металла является одной из причин, и, возможно, основной, почему на коже есть цветопередача. Берите пример с золота. Чистое золото не подвергается коррозии, но оно слишком мягкое для изготовления украшений; это исходное состояние. Подходит только для торговли. По этой причине вы обнаружите, что золото сплавляется с другими металлами, которые имеют тенденцию к эрозии. Золото не подвергается коррозии, но корродировать будут сплавы, и это при более темном цвете.
Золото не подвергается коррозии, но корродировать будут сплавы, и это при более темном цвете.
Основной причиной коррозии является ношение украшений во влажных условиях. Существует также оставлять его влажным на коже в течение длительного времени. Если вымоете руки и не будете сушить место, где украшения соприкасаются с кожей, через некоторое время вы обнаружите, что коррозия произойдет.
Поэтому вам не рекомендуется принимать душ или плавать в бассейне или океане с украшениями. Очень немногие металлы могут противостоять соленой воде. Вот почему вы обнаружите, что серебряные сплавы и медь будут подвергаться коррозии в присутствии соли, даже из продуктов, которые мы едим, таких как попкорн и картофельные чипсы.
Еще одна проблема возникает, если вы потеете естественным образом, как и все мы. Наша кожа имеет потовые железы, которые химически выделяют жиры и жирные кислоты. Их достаточно, чтобы вызвать реакцию с металлом и облегчить коррозию. Чтобы предотвратить это, вы можете использовать абсорбирующую пудру без оксида цинка на участках, которые соприкасаются с кожей.
2. Металлическое истирание
Черная как смоль пыль, появляющаяся на руке, возникает из-за так называемого металлического истирания.Это заслуга макияжа, который мы носим. Вы обнаружите, что соединения, содержащиеся в косметике, тверже, чем украшения.
При их соприкосновении происходит трение, в результате чего металл стирается. Если вам интересно, почему не меняется цвет используемого металла, например, золота или серебра, то это потому, что мелкодисперсный металл становится черным, а не металлическим. Затем пятно появляется, когда металл вступает в контакт с кожей или даже одеждой.
Если вы хотите полностью избежать этого, убедитесь, что кожа, с которой соприкасаются ваши украшения, очищена водой с мылом и очищена от макияжа.Если вы не можете избежать этого, убедитесь, что макияж, лосьоны и духи, которые вы наносите, высохли на руках, прежде чем надевать украшения. Вы хотите предотвратить истирание любой ценой.
3. Химические реакции
Такой металл, как стерлинговое серебро, имеет тенденцию тускнеть по целому ряду причин. Одним из них является воздействие соединений серы. В целом, воздействие атмосферы, где он вступает в реакцию с сероводородом в воздухе, также является еще одной причиной коррозии стерлингового серебра.
Вы обнаружите, что этот комплекс представляет собой загрязненный воздух, в котором мы все в основном живем в настоящее время. Другие острые продукты, такие как лук, рыба и яйца, могут привести к воздействию сероводорода.
Когда вы смотрите на потускневшее стерлинговое серебро, оно обычно черного или тускло-серого цвета. Вы обнаружите, что цвет будет переходить на вашу кожу или одежду, когда вы носите украшения.
Те, у кого влажная кожа, обнаружат, что их кожа окрашивается в зеленый цвет, когда они носят стерлинговое серебро. Это благодаря меди, используемой для сплава стерлингового серебра.
4. Химия тела
Как уже упоминалось, организм выделяет химические вещества, которые в конечном итоге вступают в реакцию с металлом. До сих пор мы упоминали жиры и жирные кислоты. Что-то еще, что присутствует на нашей коже, когда мы потеем, — это сера или сульфиды и аминокислоты.
Пот также является кислотой, которая при взаимодействии с телом вызывает обесцвечивание кожи и украшений. Если вы много потеете, то обнаружите, что сохранить ваши украшения в этом новом состоянии будет сложнее, чем вам хотелось бы.
Если в последнее время вы стали замечать, что ваша кожа тускнеет на украшениях, чего раньше не было, то, вероятно, в вашем организме происходят какие-то изменения. Гормональные изменения и некоторые лекарства могут изменить химический состав организма и привести к потускнению кожи.
Это связано с избыточным образованием кислоты, которая затем вступает в реакцию с металлом. Когда жарко или влажно, вы можете отказаться от ношения украшений. В качестве альтернативы вы можете носить абсорбирующие средства, не содержащие оксида цинка, чтобы ваша кожа оставалась сухой.
В качестве альтернативы вы можете носить абсорбирующие средства, не содержащие оксида цинка, чтобы ваша кожа оставалась сухой.
Как решить проблему ?
Помимо упомянутого абсорбирующего порошка, вы можете сделать еще многое другое. Лучший способ решить эту проблему с самого начала — приобрести украшения с родиевым покрытием, устойчивым к коррозии.
Можно также использовать лак или лак для ногтей для покрытия внутренней части украшения. Вам придется делать это регулярно, потому что он исчезает, но это того стоит. Он защищает как украшения, так и вашу кожу.
Другие методы, такие как снятие украшений при работе с химическими веществами (лосьонами, моющими средствами, хлором и т. д.), помогут сохранить украшения дольше.
Кроме того, когда вы наденете их, вы можете очистить их водой с мягким мылом. Тщательно высушите, а затем храните в герметичном пакете с силиконовым гелем, чтобы впитать влагу. Если вы носите изделие ежедневно, регулярно чистите его, чтобы оно оставалось новым и не содержало химикатов.
Если вы носите изделие ежедневно, регулярно чистите его, чтобы оно оставалось новым и не содержало химикатов.
Ребята, больше полезных советов смотрите здесь и здесь.
Увидимся в следующем посте!
Тайгер любит моду и украшения. Он также является производителем модных ювелирных изделий, который помогает тысячам малых предприятий расти, а также ведет дела с некоторыми крупными брендами модных ювелирных изделий. Он настоящий эксперт по металлу, и он поделится некоторой информацией, которую вы ищете.
Эй! Наконец-то я нахожу ответ!
Руководство по ювелирным металлам | Zales
Не может быть изысканных украшений без металлов, а разнообразие доступных металлов позволяет сделать украшения доступными практически для всех.
Zales предлагает украшения, изготовленные из традиционных металлов, таких как золото , серебро и платина , а также современные металлы, такие как вольфрам , нержавеющая сталь, титан и другие. Вот взгляд на металлы, используемые в ювелирных изделиях сегодня.
Вот взгляд на металлы, используемые в ювелирных изделиях сегодня.
Золотые украшения
Хорош как золото — почти ничего. Вечный выбор для всех видов ювелирных изделий. Золото легче всего поддается обработке из всех металлов, потому что оно очень пластично. Чтобы создать прочные и долговечные украшения, чистое золото сплавляют с другими металлами, такими как медь или цинк, для придания прочности и цвета.
Zales обычно использует в своих украшениях желтое, розовое и белое золото. Вот что отличает каждый тип:
Желтое золото
Золото имеет естественный желтый цвет, но при добавлении серебра или меди его естественная теплота усиливается .
Количество чистого золота в украшениях зависит от его пробы. Чем выше карат, тем выше чистота, но и ниже долговечность. Вот почему большинство украшений из желтого золота — это 14-каратное или 18-каратное золото.
Желтое золото также является самым гипоаллергенным из всех видов золота.
Розовое золото
A блестящий розовый металл , розовое золото может иметь оттенки от красной розы до розового золота. Для создания розового цвета розового золота чистое золото сочетается с медью и серебром . Чем больше меди добавлено в сплав, тем розовее будет золото.
Розовое золотоне нужно окунать или покрывать, так как цвет чистый .Он не считается гипоаллергенным и требует большей полировки, чем другие виды золота, чтобы сохранить свой блеск.
Белое золото
Для создания бело-серебряного цвета золото смешивают с палладием и серебром или с никелем, медью и цинком. Белое золото также необходимо покрыть платиной или родием для улучшения белизны и придания прочности и блеска .
Ювелирные изделия из белого золотаиногда необходимо повторно окунать после того, как покрытие стирается.
Золотой карат
Чтобы определить пробу золота, используемого в ювелирном изделии, проверьте его маркировку, также называемую его клеймом . Обычно это находится на внутренней стороне стержня или обратной стороне кулона, серьги или браслета. Вот что нужно искать:
Обычно это находится на внутренней стороне стержня или обратной стороне кулона, серьги или браслета. Вот что нужно искать:
-каратное золото Проба
| Мера в каратах | Клейма | Твердость | Чистота золота |
|---|---|---|---|
| 24 карата | — | Самый мягкий | 100% |
| 22 карата | 916/22К | Мягче | 91.6% |
| 18 карат | 750/18К | Средний | 75,0% |
| 14 карат | 585/14К | Сильнее | 58,8% |
| 10 карат | 417/10К | Самый сложный | 41,7% |
Ювелирные изделия из платины
Редкая и драгоценная платина — ярко-белый металл , в тридцать раз более редкий, чем золото.Он очень прочный, не тускнеет и гипоаллергенен. Он блестящий, красивый и прослужит не одно поколение — отличный выбор для ювелирных украшений.
Из-за своей прочности и твердости сложные гравюры могут выглядеть четче и точнее из платины, а белый вид металла делает его идеальным для демонстрации бриллиантов и драгоценных камней.
При использовании в ювелирных изделиях его обычно смешивают с аналогичными металлами — иридием, палладием, рутением, родием или осмием.Чтобы ювелирное изделие было помечено как платиновое, оно должно иметь чистоту не менее 90% платины . Ищите клеймо «PLAT» , отштампованное на внутренней стороне хвостовика (кольца) или на задней части изделия.
Ювелирные изделия из стерлингового серебра
Когда-то считавшееся даже более ценным, чем золото, сегодня серебро является самым доступным из всех драгоценных металлов. Поскольку чистое серебро слишком мягкое для изготовления ювелирных изделий, его смешивают с медью или другим металлом, чтобы получить стерлинговое серебро, которое более прочно.
должно содержать серебро чистоты не менее 92,5% , поэтому оно имеет штамп .925 . Вы можете найти этот отличительный знак на внутренней стороне стержня кольца из стерлингового серебра или на задней части ювелирных изделий.
Серебропробы может варьироваться от ярко-белого до серовато-белого и может иметь матовую или блестящую поверхность. Серебро легко тускнеет и царапается, поэтому всегда храните украшения из стерлингового серебра в пакетах для предотвращения потускнения и в прохладном, сухом месте.
Ювелирные изделия из альтернативных металлов
В дополнение к трем большим металлам — платине, золоту и серебру — современный вариант пробивается на ювелирную сцену. Они особенно популярны среди мужчин, которым нравится легкий вес и дополнительная прочность . Вот некоторые из наших любимых:
Кобальт
Украшения из кобальта сделаны из того же материала, который используется для изготовления двигателей реактивных самолетов и хирургических инструментов. Это тверже, чем нержавеющая сталь , и поэтому ее труднее поцарапать.
Это тверже, чем нержавеющая сталь , и поэтому ее труднее поцарапать.
Хотя кобальт не на 100% устойчив к царапинам, он намного тверже титана и всех других драгоценных металлов, включая платину, золото и серебро. Он также гипоаллергенен.
Нержавеющая сталь
Нержавеющая сталь вышла за пределы кухни и стала желанным металлом в часах и ювелирных изделиях. Нержавеющая сталь серебристо-белого цвета с зеркальной поверхностью и слоем хрома, очень хорошо сохраняет свой блеск и цвет и устойчива к потускнению.
Нержавеющая сталь, один из самых прочных металлов, хорошо противостоит износу и разрыву, что делает ее отличным выбором, когда образ жизни или работа требуют повышенной прочности.
Титан
Титан так же прочен, как сталь, но на 45% легче по весу . Фактически, он имеет самое высокое отношение прочности к весу среди всех металлов.
Он похож на платину по своей устойчивости к потускнению — вот что делает его разумным выбором для космических кораблей, а также для украшений, особенно для предметов, которые носят каждый день.
Титан универсальный , легкий , гипоаллергенный и устойчивый к коррозии , с металлическим цветом, который может меняться от белого до темного и цветного в зависимости от способа обработки.
Вольфрам
Вольфрам очень тяжелый, серо-белого цвета с блестящей поверхностью. Этот гипоаллергенный металл имеет самую высокую температуру плавления и самую высокую прочность из всех металлов — по-шведски это означает «тяжелый камень».» Из-за своей твердости блеск сохраняется долго.
Выбор подходящего металла
Несколько факторов, которые следует учитывать при выборе металла для ваших украшений:
Внутренняя ценность
Базовая стоимость. Цены на металлы колеблются ежедневно в зависимости от спроса и предложения. Чем более редкий и драгоценный металл, тем меньше его доступность. Редкость может стимулировать спрос , благодаря чему редкий металл, такой как платина или золото , с большей вероятностью сохранит свою ценность с течением времени.
Срок службы
Учитывайте способность металла выдерживать ежедневный износ, а также долговечность его модного вида. Например, хотя вольфрам и очень прочный, он не считается драгоценным металлом.
Гипоаллергенность
Гипоаллергенные металлы сводят к минимуму возможность раздражающей аллергической реакции. Более чистые металлы, такие как платина и титан , как правило, гипоаллергенны, что создает небольшой риск потенциального раздражения.
Прочность
Все металлы царапаются и даже иногда вмятины. Однако некоторые металлы, такие как титан и вольфрам , устойчивы к царапинам.
Коэффициент восстановления
Можно ли восстановить металл, чтобы ваши украшения выглядели как новые? Некоторые металлы можно легко восстановить. Другие, хотя и долговечные и прочные, могут не справиться с процессом восстановления или изменения размеров.
Редкость
Чем реже металл, тем дороже он будет.Поэтому изделия из платины и золота , как правило, будут дороже, чем из других металлов.
Подъем
Некоторым нравится ощущение веса украшений, в то время как другие предпочитают чувствовать, что на них вообще ничего нет. Платина — самый плотный и тяжелый металл — на 40% тяжелее золота . Титан и нержавеющая сталь являются одними из самых легких.
ЗаботитьсяПолировать, мыть или полировать? Вот все, что вам нужно знать об уходе за металлическими украшениями.
Один цвет, очень разные металлы
Выстройте кучу украшений издалека, и самое простое различие, которое вы сможете провести, это между серебром и золотом.
В то время как выбор между этими двумя оттенками в основном зависит от стиля и предпочтений, выбор конкретного типа металлических украшений требует немного больше усилий.
Допустим, вы решили приобрести украшения серебристого цвета. Вы действительно хотите серебро? Или, может быть, платина? Читайте дальше, чтобы узнать о различиях между серебряными и платиновыми украшениями.
Платина против серебраДавайте сначала рассмотрим различия во внешнем виде.
Хотя на первый взгляд и серебро, и платина кажутся серебристыми, на самом деле эти два металла легко различимы невооруженным глазом. Оба имеют серый подтон, в отличие от белого золота, которое имеет более теплый желтый оттенок, но платина намного ярче и блестит, а серебро имеет более тусклый серый цвет .
ДолговечностьРазница в долговечности действительно несопоставима между платиной и серебром.
Серебро — мягкий металл, который быстро изнашивается и легко тускнеет. Одним из самых больших преимуществ платины является ее высокая температура плавления, что делает ее достаточно твердой, чтобы не требовать никаких сплавов.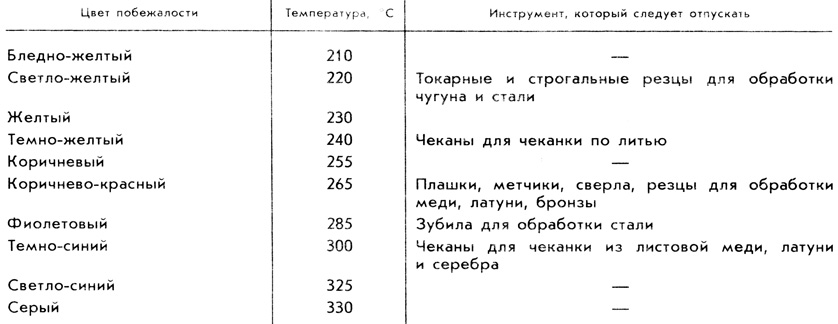
часто состоят из чистой платины на 90-95%, что идеально подходит для ежедневного ношения помолвочного кольца.
ЦенаСеребро – один из самых доступных ювелирных металлов. Прекрасно подходит для бижутерии, которая входит в моду и выходит из нее.
Однако, когда интерес представляет собой изысканное ювелирное изделие, которое вы будете носить довольно часто, если не каждый день, платина стоит вложений. Это один из самых дорогих металлов для изготовления ювелирных изделий, второй после родия, который обычно используется только в качестве покрытия поверх золота для увеличения его долговечности.
Износ и уходПлатина — предпочтительный металл для обладательниц ювелирных изделий с чувствительной кожей. Натуральный гипоаллергенный продукт, не вызывающий раздражения кожи.
Хотя у большинства людей нет прямой аллергии на серебро или золото, многие металлы, которые могут быть сплавлены с ними, являются обычными аллергенами.
Нужны низкие эксплуатационные расходы? Еще одно очко за платину.
Несмотря на то, что все ювелирные украшения должны проходить профессиональную чистку у ювелира пару раз в год, вам не нужно делать ничего больше, чтобы сохранить характерный блеск платины. С другой стороны, серебро требует частой полировки, чтобы избежать потускнения.
Если вы ищете обручальное кольцо или другие изысканные украшения, выбор между платиной и серебром довольно очевиден.Мы также знаем отличное место, где можно начать поиск ювелирных изделий из платины — Platinum Guild International. Удачных покупок ювелирных украшений!
Хотите быть уверенным в своем обручальном кольце, как только найдете идеальное? Получите расчет стоимости ювелирных изделий за минуту, не предоставляя никакой личной информации. Просто нажмите кнопку ниже.
6 основных типов металла для изготовления ювелирных изделий
Getty Images/Westend61
Самое приятное в ювелирных изделиях из металла — это разнообразие материалов, с которыми приходится работать. Если вы хотите обрабатывать серебро, золото, розовое золото, недрагоценные металлы или более специализированные металлы, оставайтесь с нами, чтобы получить краткое изложение наиболее распространенных типов металлов для изготовления ювелирных изделий.
Если вы хотите обрабатывать серебро, золото, розовое золото, недрагоценные металлы или более специализированные металлы, оставайтесь с нами, чтобы получить краткое изложение наиболее распространенных типов металлов для изготовления ювелирных изделий.
1. Серебро
Когда вы говорите о ювелирных изделиях, вы говорите о стерлинговом серебре. Это просто означает, что это 92,5% серебра и 7,5% меди. Стерлинговое серебро — отличный вариант, потому что оно прочное и долговечное, поэтому оно хорошо подходит для колец, ожерелий, браслетов, запонок, пряжек для ремней, украшений для тела… ну вы поняли.Но имейте в виду, что серебряные украшения мягче, чем золото, платина и титан, и они могут потускнеть без надлежащего ухода.
2. С серебряным наполнителем
Металлы с серебряным наполнителем (также известные как «серебряная накладка») — еще один популярный выбор. Разница в том, что проволока с серебряным наполнителем изготавливается с использованием тепла и давления для нанесения слоя серебра на основу из более дешевого металла.
Этот слой серебра в сотни раз толще стандартного покрытия.Поскольку он такой толстый, он позволяет вам работать глубже, больше полировать и даже делать легкую гравировку, не обнажая основной металл под ним.
С серебряным наполнителем подходит для ювелирных изделий, таких как проволочные серьги и цепочки. Это делает их доступными, плюс они будут служить вечно и будут отлично смотреться в сочетании с подвесками из стерлингового серебра.
3. Золото
Вестенд61/Getty Images
Золотые украшения представляют собой смесь золота и других металлов, таких как серебро, медь, никель и цинк.Когда вы говорите о фактическом содержании золота, оно измеряется в каратах (K) или каратах (ct). Это просто описывает пропорцию чистого золота к другим металлам в материале. Разумеется, чем выше доля золота в конечном металле, тем больше долларов вам придется за него выложить.
Максимальное содержание золота 24К, что делает ювелирные изделия ужасными, потому что золото 24К мягкое и податливое. Посмотрите на 14-каратное золото для ювелирных изделий — оно прочное и с ним легко работать. Или, если вы чувствуете себя более расточительным, попробуйте 18-каратное золото (75-процентное чистое золото).
Посмотрите на 14-каратное золото для ювелирных изделий — оно прочное и с ним легко работать. Или, если вы чувствуете себя более расточительным, попробуйте 18-каратное золото (75-процентное чистое золото).
Чистое золото желтого цвета, и, поскольку вы не будете его покупать, в конечном итоге цвет этого металла определяют не содержащие золота металлы, используемые в сплаве.
- Желтое золото представляет собой сплав чистого золота, серебра и меди или цинка.
- Белое золото представляет собой сплав чистого золота и белых металлов, таких как никель, серебро и палладий. На самом деле он более сероватого цвета и покрыт родием, чтобы придать ему более белый вид.Сегодня обычно избегают никеля, так как у многих людей на него аллергия.
- Розовое золото представляет собой сплав чистого золота с высоким содержанием меди.
- Зеленое золото точно такое же, как желтое золото, за исключением того, что в сплаве отсутствует медь.

Во всех своих вариациях золото является популярным выбором для таких вещей, как обручальные кольца, кольца, серьги и ожерелья.
4. Основной металл
Вестенд61/Getty Images
Неблагородные металлы включают, среди прочих, железо, никель, медь, латунь и титан.Этих металлов много, и они могут довольно легко окисляться или подвергаться коррозии, но из них получаются красивые подвески из чеканных дисков.
5. Платина
Платина — самый редкий и самый дорогой из металлов. Но цена оправдана, так как он очень прочный и никогда не тускнеет. Чистая платина плавится при температуре 3216,2 градусов по Фаренгейту, поэтому, если вы, знаете, буквально не проводите время на солнце, она отлично подойдет для таких вещей, как обручальные кольца и манжеты.
Внешний вид решает все, поэтому платину часто сплавляют с медью и кобальтом, чтобы придать ей другой вид.Кроме того, сочетание его с другими металлами делает его еще более прочным. Если вы ищете другие металлы «платиновой группы», обратите внимание на рутений, родий, палладий, осмий и иридий.
Если вы ищете другие металлы «платиновой группы», обратите внимание на рутений, родий, палладий, осмий и иридий.
6. Титан
Прочнее титана не бывает. Это самый твердый природный металл, известный человеку, по сравнению со сталью, золотом, серебром и платиной. Кроме того, он устойчив к царапинам, легок и легко окрашивается.
Титандаже полностью гипоаллергенен, что делает его популярным для изготовления украшений для пирсинга и даже хирургических имплантатов.Только не используйте этот чудо-металл для изготовления колец — ваши пальцы со временем меняют размер (странно, правда?), а титан нельзя паять или изменять размер.
Metal Guide — Hannon Gemologist and Master Jewelers
С тех пор, как семья Hannon Jewellers начала создавать украшения в Никарагуа в 1940 году, мы использовали лучшие сплавы драгоценных металлов для наших творений. Мы подбираем нашего клиента к цвету драгоценных камней, цвету и свойствам сплавов к предполагаемому использованию ювелирного творения.
Типы металлов
В Hannon Jewellers мы предлагаем широкий выбор металлов и чистоты металла. Каждый драгоценный металл нуждается в сплавах, чтобы сделать его прочным и долговечным, и мы производим наши металлы в соответствии с самыми высокими стандартами. Ниже перечислены некоторые из основных вариантов металла, которые мы предлагаем.
Золото
Определения для белого золота, желтого золота, никелевой пластины и желтой пластины:
Чистое золото: (чистое золото) мягче чистого серебра, но тверже олова.Его красота и блеск не имеют себе равных среди сплавов золота. Чрезвычайная ковкость, пластичность и мягкость чистого золота делают его практически бесполезным для ювелирных изделий.
Сплавы, добавленные для повышения прочности: Добавки легирующих элементов (других металлов) к золоту используются для увеличения ударной вязкости и твердости металла. Хотя почти любой металл можно сплавить (расплавить) с золотом, только некоторые металлы не будут резко менять цвет или делать металл хрупким.
Например, традиционное 14-каратное золото содержит четырнадцать частей чистого золота и десять частей других металлов, таких как серебро, медь и никель.Изменением этих комбинаций достигаются различные степени работоспособности. При изготовлении золотого сплава каждый компонент металла тщательно взвешивают и помещают в тигель. Затем металлы вместе нагревают до температуры более 1900 градусов по Фаренгейту, перемешивают до однородности и заливают в форму.
Наиболее распространенными золотыми сплавами для изготовления ювелирных изделий являются:
18-каратное золото или 750 означает содержание чистого золота 75%
14-каратное золото или 585 означает содержание чистого золота 58%
10-каратное золото или 416 означает содержание чистого золота 41%.
Чем выше процент чистого золота, тем дороже украшение.
Варианты золотого цвета:
Чистое золото, или 24 карата, не имеет изменений в цвете. Это всегда насыщенный теплый желтый цвет. Однако он может быть изготовлен в самых разных цветах, включая розовый, белый, зеленый, синий или серый, путем смешивания с различными металлами. Например, когда к чистому золоту добавляют серебро и медь, оно становится желтым. При добавлении никеля или палладия (или цинка и меди) золото становится белым.Чистое золото в сочетании с серебром, медью и цинком дает зеленое золото. А розовое золото получается, когда медь смешивается с чистым золотом. Более высокая доля меди дает красноватый оттенок . Если основной добавкой является никель (или иридий), сплав золота становится белым . Добавление индия, например, окрашивает золото в фиолетовый цвет и придает золоту обрабатываемость стекла.
Однако он может быть изготовлен в самых разных цветах, включая розовый, белый, зеленый, синий или серый, путем смешивания с различными металлами. Например, когда к чистому золоту добавляют серебро и медь, оно становится желтым. При добавлении никеля или палладия (или цинка и меди) золото становится белым.Чистое золото в сочетании с серебром, медью и цинком дает зеленое золото. А розовое золото получается, когда медь смешивается с чистым золотом. Более высокая доля меди дает красноватый оттенок . Если основной добавкой является никель (или иридий), сплав золота становится белым . Добавление индия, например, окрашивает золото в фиолетовый цвет и придает золоту обрабатываемость стекла.
По мере того, как отрасль продвигается вперед в исследованиях, на рынок выходит все больше и больше новых цветных сплавов. Новые оттенки коричневого, янтарного, серого, черного и темно-зеленого создаются традиционным методом легирования, а также гальванизацией.
Термин , наполненный золотом , относится к производственному процессу, в котором слиток недрагоценного металла, обычно меди, соединяется с более тонкими слитками золота. «Сэндвич» образуется путем механического соединения слоя золота с обеих сторон медного слитка. Затем этот «сэндвич» подвергают холодной обработке путем прокатки или волочения до тех пор, пока не будет получен металл гораздо более тонкой толщины. Затем из этого слоистого материала формуют или штампуют изделия. Затем объект покрывают золотом, чтобы скрыть края, поскольку в противном случае они обнажили бы зажатую конструкцию.Хотя сегодня продукт с золотым наполнителем легко доступен, этот процесс был наиболее популярен в начале 1900-х годов. Клеймо будет отображаться как 1/20 часть 14-каратного золота, что указывает на то, что по весу 1/20 часть металла, содержащегося в изделии, составляет 14-каратное золото.
Прокатное золото: Пластина относится к тому же процессу; однако содержание золота ниже; например, 1/30 12к. В вашем вопросе ссылка на белый и желтый — это просто указание на цвет используемого золота. Преимущества этого продукта в том, что слой золота намного толще и дольше носится, чем покрытие золотом.Это также намного дешевле, чем аналогичный продукт, полностью изготовленный из 14-каратного материала.
В вашем вопросе ссылка на белый и желтый — это просто указание на цвет используемого золота. Преимущества этого продукта в том, что слой золота намного толще и дольше носится, чем покрытие золотом.Это также намного дешевле, чем аналогичный продукт, полностью изготовленный из 14-каратного материала.
Заполненная золотом проволока: Проволока изготавливается с использованием аналогичного процесса, за исключением того, что сердечник из основного металла вставляется в золотую трубку. Склеенные трубка и сердечник затем вытягиваются через редукционные штампы, диаметры которых постепенно уменьшаются, до тех пор, пока не будет достигнут желаемый диаметр.
Золотое гальванопокрытие: Когда изделие упоминается как золотое, родиевое или никелированное , это указывает на то, что оно было покрыто тонким слоем этого конкретного металла.Термины «золотое гальванопокрытие» или «золотое покрытие» указывают на то, что оно создается в процессе гальванического покрытия, при котором наносится очень тонкая «окраска» золота — редко более 10 микродюймов. Даже тяжелое гальванопокрытие из золота имеет толщину всего 100 микродюймов. Изделия с гальваническим покрытием выглядят хорошо, когда они новые. Тем не менее, золотая пленка обычно очень мягкая, быстро стирается. Это означает, что основной металл обнажается, придавая ювелирному изделию изношенный и потускневший вид.
Даже тяжелое гальванопокрытие из золота имеет толщину всего 100 микродюймов. Изделия с гальваническим покрытием выглядят хорошо, когда они новые. Тем не менее, золотая пленка обычно очень мягкая, быстро стирается. Это означает, что основной металл обнажается, придавая ювелирному изделию изношенный и потускневший вид.
Позолота или позолота: Любое более тонкое покрытие должно быть помечено как позолота или позолота.Когда основным металлом является стерлинговое серебро, этот процесс известен как Vermeil .
Белое золото
Любой выбор сплава для создания Белого Золота — это компромисс между цветом или внешним видом, свойствами сплава при изготовлении ювелирных изделий и стоимостью.
Никель и палладий являются наиболее распространенными отбеливающими агентами, используемыми для придания золоту белого цвета. От того, какие сплавы используются, будут зависеть свойства и белизна полученного белого золота.
- Высокое содержание никеля: Обеспечивает яркий металлический цвет белого золота, но не такой ковкий, как сплавы с низким содержанием никеля.
 Также полученная смесь более подвержена растрескиванию. Это особенно важно для штырей, которые могут быть хрупкими и трескаться легче, чем другие сплавы.
Также полученная смесь более подвержена растрескиванию. Это особенно важно для штырей, которые могут быть хрупкими и трескаться легче, чем другие сплавы. - Низкое содержание никеля: Ювелиры могут предпочесть эту смесь, потому что она лучше подходит для изготовления. Он подвержен коррозии под напряжением. Может иметь желтоватое олово и может потребовать покрытия родием.
- Высокое содержание палладия: Этот сплав имеет мягкий белый цвет; он дороже, но не содержит никеля и менее гипоаллергенен.Он также устойчив к коррозии под напряжением и растрескиванию.
- Низкое содержание палладия: Не совсем белый цвет, может потребоваться покрытие родием. Он устойчив к коррозии под напряжением и растрескиванию.
Платина
Платина — один из самых редких металлов. Он чище, реже и долговечнее для использования в ювелирных изделиях. Это дороже золота, так как ежегодно в ювелирные изделия перерабатывается всего 88 тонн платины по сравнению с 2700 тоннами золота.
Platinum гипоаллергенен для людей с повышенной чувствительностью к некоторым металлам.При носке он остается белым с приобретенной легкой патиной, что делает его уникальным.
Когда требуется постоянная белизна, предпочтительным белым металлом является платина, поскольку она по своей природе белая и практически невосприимчива к химическим воздействиям.
Белое золото
против платины
Платина и золото являются драгоценными металлами. Однако каждый из них имеет совершенно разный химический состав и свойства.
Платина Платина — один из самых редких металлов.Он чище, реже и долговечнее для использования в ювелирных изделиях. Это дороже золота, так как ежегодно в ювелирные изделия перерабатывается всего 88 тонн платины по сравнению с 2700 тоннами золота. Platinum гипоаллергенен для людей с повышенной чувствительностью к некоторым металлам. Когда требуется постоянная белизна, предпочтительным белым металлом является платина, поскольку она по своей природе белая и практически невосприимчива к химическим воздействиям. | Белое золото Белое золотобыло создано как альтернатива платине более века назад. Он стал более популярным в 1940-х годах, когда платина была недоступна. Поскольку чистое золото по своей природе всегда желтое, его смешивание с позволяет «отбелить» его добела. Этот распространенный сплав изначально был никелем. Но поскольку у некоторых людей никель может вызывать аллергическую реакцию, сейчас используются новые сплавы, такие как палладий. |
Цвет:
Многие знатоки считают платину высшим драгоценным ювелирным металлом. также примерно в 60 раз более редкая, чем золото. Новая полированная платина имеет ярко-белый металлический цвет. Однако со временем платиновая деталь приобретет серовато-белый цвет или налет из-за царапин на поверхности. Некоторые люди будут чувствовать необходимость полировать это украшение чаще, чтобы сохранить «чистый или новый» вид, который обычно желателен. | Чистое золото желтого цвета. Белое золото — это желтое золото, в которое были добавлены другие сплавы, чтобы оно выглядело белым. Новое полированное белое золото имеет яркий цвет белого металла. В зависимости от типа сплава, используемого при изготовлении белого золота, украшения из белого золота со временем приобретают слабый желтоватый оттенок. В таких случаях белое золото может быть покрыто родием, чтобы восстановить ярко-белый вид ваших украшений. Вы хотели бы знать, что доступны новые инновационные альтернативы легированию золота для придания ему белого цвета. В этих новых золотых сплавах не использовался никель, а вместо него смешивался палладий для получения металла с превосходной белизной, который не требует покрытия родием. |
Сравнение металлов:
| Справочник для сравнения | Платина | Палладий | Белое золото | Чистое серебро |
Большинство изделий Hannon Jewellers доступны из всех драгоценных металлов.Вы можете выбрать золото всех цветов или металлы белого цвета, чтобы улучшить цвет и блеск ваших бриллиантовых украшений. Однако выбор типа металла является личным выбором. Однако выбор типа металла является личным выбором. | ||||
Цвет/Белизна | 9 | 9 | 8 | 10 |
Масса | 10 | 6 | 6 | 4 |
Твердость/ царапание | 8 | 8 | 10 | 2 |
Пластичность/мягкость | 7 | 7 | 9 | 5 |
Долговечность / повседневный износ | 10 | 8 | 8 | 8 |
Срок службы | 10 | 8 | 8 | 2 |
Гипоаллергенный | 10 | 10 | 8 | 5 |
Реставрация / можно ли сделать так, чтобы он снова выглядел как новый? | 10 | 10 | 10 | 10 |
Относительная стоимость | $$$$ | $$$ | $$ | $ |
Ключ
Различия в каратах
Золотые украшения можно идентифицировать по следующим клеймам:
24-каратное золото и всегда 100% чистое золото
18-каратное золото или 750 означает содержание чистого золота 75%
14-каратное золото или 585 означает 58%-е содержание чистого золота % чистого золота с содержанием
Чем выше процент чистого золота, тем дороже украшение.
Общие вопросы
Царапается ли платина?
Как и все драгоценные металлы, платина и белое золото царапаются.
Если изделие из платины или золота отполировано до блеска, царапины на самом деле легче обнаружить из-за высокого контраста между полировкой и царапиной.
| Платина — более мягкий и гибкий металл, чем белое золото. Со временем, так как ее легче поцарапать, на платине образуется естественная патина (серовато-белый тусклый цвет), которую многие люди предпочитают полированной поверхности. Платина— более плотный металл. Его химический состав имеет более компактную концентрацию материала на единицу, чем золото. Это означает, что ваши платиновые украшения тяжелее и будут носиться дольше, чем белое золото. Девяносто процентов платины весят на шестьдесят процентов больше, чем 14-каратное золото. Эти два свойства — быть плотнее и мягче золота — означают, что при царапании платины металл не теряется. | Белое золото – более твердый металл, чем платина. Это означает, что его поверхность более устойчива к царапинам, чем платина. Кроме того, белое золото менее ковкое. Белому золоту требуется большее давление, чтобы согнуться, чем платине. Это означает, что зубцы из белого золота с бриллиантами более устойчивы к изгибу, чем платина. Большинство ювелирных изделий с бриллиантами в настоящее время имеют оправы и зубцы из белого золота. Важно понимать, что при сравнении этих двух металлов мы говорим об относительных предельных различиях в ударной вязкости и твердости. Оба металла достаточно прочны, чтобы выдержать нормальный износ ваших украшений. |
Я слышал, что с платиной труднее работать, чем с золотом.
Платина и белое золото, как и другие металлы, могут обрабатываться или модифицироваться квалифицированным ювелиром.
| Платина обрабатывается иначе, чем золото, но не сложнее для квалифицированного и опытного мастера. (В некоторых ювелирных магазинах нет мастеров, умеющих работать с платиной). Платина имеет гораздо более высокую температуру плавления, чем другие драгоценные металлы, и ее можно легко загрязнить при неправильном обращении. Поэтому платина требует специальных процедур, химикатов и оборудования, которые удорожают процесс создания платиновых украшений. | Большинство ювелиров хорошо подготовлены для работы с золотом и всеми его сплавами. |
Почему платина стоит дороже?
Да, платиновые украшения стоят дороже. Платина – более чистый металл.Чаще всего он производится с чистотой 95 процентов. (в большинстве случаев чистота 90 или 95 процентов). Платина встречается реже, в настоящее время необработанная платина вдвое дороже золота за унцию, и поскольку она почти на две трети плотнее золота, то же самое кольцо из платины весит намного больше, чем золото. Кроме того, мы уже обращали внимание на то, что стоимость труда и специального оборудования, необходимых для изготовления ювелирных изделий из платины, выше. Эти четыре фактора умножают тот факт, что ювелирные изделия из платины могут стоить в пять раз дороже, чем такие же изделия, изготовленные из золота. В основном платина (и палладий) используется в промышленности. Цена на оба металла в большей степени определяется спросом на автомобили (каталитические нейтрализаторы, которые очищают автомобильные выбросы) и электронику (используется для покрытия драйверов жестких дисков компьютеров и изготовления жидкокристаллических дисплеев для телевизоров и компьютеров. Палладий также используется в качестве полупроводника). Поэтому цены на эти металлы имеют тенденцию двигаться синхронно с мировой экономикой. | Рыночная цена на золото ниже, чем на платину.Чистое золото встречается в большем количестве мест и в большем количестве в мире, и на рынке доступно больше запасов. Эти комбинации золота и сплавов также делают готовые украшения более доступными, чем платина. На цену золота также влияют экономические колебания. Хотя золото широко используется в ювелирных изделиях, его использование в промышленности ограничено. Основным драйвером спроса являются инвесторы, которые ищут некоторую защиту от инфляции и валютных рисков. Большинство золотых сплавов, используемых в производстве ювелирных украшений, имеет чистоту 75% (18К) или 58,33% (14К). Поэтому мы не можем реально сравнивать стоимость белого золота с ценой платины 95% чистоты. |
Как узнать, какой металл я покупаю?
Если вы покупаете ювелирные изделия у уважаемого ювелира, относительно легко проверить, являются ли они платиновыми или золотыми. Все украшения продаются в США.должен быть проштампован общим знаком качества, показывающим процентное содержание платины или золота, использованного в металле.
Чаще всего это следующие марки: Platinum, Plat или Pt. за которым следует процентное содержание платины, например: Pt. 1000 (чистая платина), Pt999 (999 частей на тысячу платины и одна часть другого металла). Другие распространенные платиновые сплавы: 950Pt (или 950Plat или Pt950), что составляет 950 частей на тысячу платины и 50 частей других металлов; 900Pt (или 900PIat или Pt900), что составляет 900 частей на тысячу платины и 100 частей других металлов; и 850Pt (или 850PIat или Pt850), что составляет 850 частей на тысячу платины и 150 частей других металлов. | Золотые украшения можно идентифицировать по следующим клеймам: Pure Gold имеет 24-каратную пробу и всегда на 100% чист. 18-каратное золото или 750 относится к содержанию чистого золота 75% 14-каратное золото или 585 относится к содержанию чистого золота 58% 10-каратное золото или 416 относится к содержанию чистого золота 41%. Чем выше процент чистого золота, тем дороже украшение. |
Белое золото дешевле платины. Он почти такого же цвета. Должен ли я купить Белое золото вместо этого?
Если вы внимательно посмотрите на белое золото и платину, вы увидите, что цвет и внешний вид не совсем одинаковы, хотя оба они имеют вид белого металла. В новом состоянии очень трудно, а иногда и невозможно отличить два металла друг от друга.
В новом состоянии очень трудно, а иногда и невозможно отличить два металла друг от друга.
Мы не рекомендуем располагать два кольца, одно из золота, а другое из платины, рядом друг с другом, поскольку в этом случае цветовые различия будут усиливаться. Ваш личный стиль жизни, семейные традиции, ожидания и бюджет являются важными факторами в ваших личных исследованиях и выборе ваших украшений. Поделитесь своими идеями со своим личным ювелиром, который поможет вам проанализировать, какой металл лучше всего подходит вам сейчас и в будущем.
Для получения дополнительной информации о платиновых украшениях: www.драгоценная платина.com
Или позвоните нам по телефону 225-766-8242 или напишите нам по электронной почте [email protected]
Почему золото окрашивает кожу?
Вы можете подумать, что неисправность в изготовлении или недоработка могут быть проблемой, когда кольцо «переворачивается», чернея или обесцвечивая кожу и одежду или само украшение. Ювелиры Hannon могут протестировать металл в ваших украшениях, чтобы проверить его содержание. Однако, если это не так, это краткое обсуждение причин и способов их предотвращения.
Ювелиры Hannon могут протестировать металл в ваших украшениях, чтобы проверить его содержание. Однако, если это не так, это краткое обсуждение причин и способов их предотвращения.
Наиболее распространенной причиной является металлическое истирание , вызванное нанесением макияжа на кожу или одежду. Косметика часто содержит соединения, более твердые, чем сами украшения, которые изнашивают или стирают очень мелкие частицы. Очень мелкодисперсный металл всегда кажется черным, а не металлическим, поэтому он выглядит как угольно-черная пыль. Когда эта пыль вступает в контакт с впитывающими поверхностями, такими как кожа или одежда, она прилипает, образуя черное пятно.
Чтобы этого не произошло, попробуйте сменить косметику.Если это невозможно, рекомендуем снимать кольца и другие украшения при их надевании, а участки кожи, контактирующие с украшениями, очищать водой с мылом.
Другой причиной является фактическая коррозия металлов . Золото само по себе не подвергается коррозии, но его первичные сплавы серебра или меди подвержены коррозии, образуя очень темные химические соединения во влажных или влажных условиях.
Золото само по себе не подвергается коррозии, но его первичные сплавы серебра или меди подвержены коррозии, образуя очень темные химические соединения во влажных или влажных условиях.
Когда вы потеете, выделяемые жиры и жирные кислоты могут вызвать коррозию 14-каратного золота, особенно при воздействии тепла и воздуха.Эта проблема может усугубляться на морском побережье и в субтропических районах, где хлориды в сочетании с потом образуют коррозионный элемент, обесцвечивающий кожу. Испарения смога постепенно воздействуют на украшения и проявляются в виде потускнения, которое стирается с кожи.
Мы рекомендуем часто снимать украшения и использовать абсорбирующую пудру, не содержащую абразивов, на коже, которая соприкасается с украшениями.
То же самое можно сказать и об аллергических реакциях на сплавы, используемые в золотых украшениях. Мы знаем об аллергических реакциях на серебро, медь и никель.В этом случае мы часто предлагаем использовать более чистый золотой сплав, такой как 18-каратное, или белое золото без содержания никеля. Мы не знаем об аллергических реакциях на платину, так как этот металл в своей традиционной форме является чистым металлом.
Мы не знаем об аллергических реакциях на платину, так как этот металл в своей традиционной форме является чистым металлом.
Даже дизайн украшений может оказывать влияние. Широкие хвостовики имеют большую площадь поверхности для контакта с абразивами или коррозионными веществами. Вогнутые поверхности внутри стержня образуют точки сбора, которые задерживают влагу и загрязняющие вещества, что также вызывает своего рода дерматит.
Может быть хорошей идеей снять все кольца перед использованием мыла, чистящих составов или моющих средств и часто чистить их кольца.
В дополнение к этим корректирующим действиям мы рекомендуем клиентам с этой проблемой перейти на 18-каратное золото или платину. Более низкое содержание сплава 18-каратного золота — 25% против почти 42% — значительно уменьшает проблему, а использование платины — благодаря ее чистоте — должно устранить ее полностью.
Что такое розовое золото? Вот что вам нужно знать об этом драгоценном металле
Каждый из предлагаемых нами драгоценных металлов обладает своими уникальными свойствами, которые делают его особенно подходящим для ювелирных изделий. Вот лишь несколько популярных металлов, которые используются в современных ювелирных изделиях.
Вот лишь несколько популярных металлов, которые используются в современных ювелирных изделиях.
Платина
Платина — самый редкий металл, поэтому она значительно дороже, чем даже чистое золото. Ежегодно добывается 85 тонн платины по сравнению с 1500 тоннами золота. Для производства одной унции платины необходимо добыть десять тонн руды. Платина — самый чистый металл. Платина — единственный драгоценный металл, используемый в ювелирных украшениях, чистота которого может составлять 95%. К платине обычно добавляют небольшие количества иридия и рутения (металл из семейства платиновых).На марке будет написано PLAT, PT или 950. Чистота платины делает ее единственным по-настоящему гипоаллергенным металлом.
Платина также является самым прочным металлом. Он весит на 60% больше, чем золото, и обладает высокой термостойкостью. Он очень плотный и чрезвычайно устойчивый к износу. Хотя платина по-прежнему будет царапаться, как и любой драгоценный металл, царапины не означают материальных потерь.
Золото
Хотя золото не так редко встречается, как платина, оно столь же желательно. Золото имеет естественный желтый цвет и может быть найдено во множестве различных степеней чистоты.Самая чистая форма золота — 24-каратное, но его редко можно увидеть в кольцах, потому что оно слишком мягкое для закрепки бриллианта. Чаще всего используется 14-каратное и 18-каратное золото. Когда мы говорим о различных «каратах» золота, мы имеем в виду степень, в которой золото смешивается с другими металлами. Например, сплав (смесь металлов) из 14 частей золота и 10 частей другого металла будет 14-каратным золотом. Чем больше «другого металла» используется в процессе, тем прочнее золото. Различные «цвета» золота являются результатом специальных сплавов, которые были разработаны для изменения естественного цвета золота.Различные цвета достигаются путем добавления различных сплавов. Например, белое золото производится путем добавления никеля и цинка, а розовое золото — путем добавления меди.
Что такое розовое золото?
Вы почти наверняка видели украшения из розового золота и даже можете предпочесть его другим оттенкам золота. Но чего вы, возможно, не знаете, так это того, из чего сделано розовое золото и что отличает его от золота других стилей.
Розовое золото — это сплав, состоящий из комбинации чистого золота и меди.Смесь двух металлов изменяет цвет конечного продукта и его карат. Например, наиболее распространенный сплав розового золота состоит из 75 процентов чистого золота и 25 процентов меди, что составляет 18-каратное розовое золото. Изменение процентного содержания одного металла в сплаве изменит карат.
Обычно прямое сочетание меди и золота дает насыщенный красноватый цвет. Но также можно добавить небольшое количество серебра, чтобы создать более мягкую розу — с небольшим количеством серебра, добавленным для создания варианта розового золота, называемого «розовым золотом».”
Некогда считавшееся прерогативой русских аристократов 19 века, красота и органичная грация розового золота теперь доступны каждому, а в 21 веке оно вновь обрело превосходство как один из самых популярных оттенков золота для свадеб и моды Ювелирные изделия.
По сравнению с желтым и белым золотом у розового золота есть несколько плюсов и минусов. Первым «за», конечно же, является красивый цвет, который может быть достаточной причиной для вас, чтобы выбрать украшения из розового золота. Кроме того, чистое золото — очень мягкий материал, который можно поцарапать, а в сплаве оно приобретает прочность, чтобы противостоять повреждениям.Розовое золото, благодаря высокому содержанию меди, намного прочнее желтого золота.
Однако при покупке оправы из розового золота следует помнить о нескольких вещах. Розовое золото не гипоаллергенно, поэтому, если вы чувствительны к меди, розовое золото может вам не подойти. Кроме того, медь более склонна к расслаиванию и окислению, чем другие сплавы металлов, поэтому, если ваше кольцо неправильно нагрето, золото и медь могут немного отделиться в ваших украшениях. Кроме того, вариант из розового золота мягче, чем желтое или белое золото, поэтому, если ваши украшения склонны к ударам, нежное розовое золото может быть не идеальным выбором.
Тем не менее, если вы знаете свой образ жизни и имеете квалифицированного ювелира, который должен поддерживать ваши изделия в надлежащем состоянии, существует несколько вариантов более современных и красивых украшений, чем сияющая красота розового золота, и мы призываем наших клиентов относиться к драгоценному металлу поближе. Посмотрите.
Серебро
Серебро, давно ценившееся как драгоценный металл, использовалось в качестве валюты, украшений и украшений на протяжении сотен лет. Мягкий, ковкий металл, серебро немного тверже золота и обладает самой высокой электропроводностью и теплопроводностью среди всех металлов.Одной из самых популярных форм серебра для ювелирных изделий является стерлинговое серебро. Это сплав серебра, содержащий 92,5% чистого серебра и 7,5% других металлов, обычно меди. Серебряные украшения часто покрывают тонким слоем серебра 999 пробы, чтобы придать им яркую, блестящую поверхность. Покрытие родием также обычно используется для придания яркости внешнему виду серебряных украшений. Серебро имеет тенденцию тускнеть и требует регулярного ухода для поддержания оптимального внешнего вида.
Серебро имеет тенденцию тускнеть и требует регулярного ухода для поддержания оптимального внешнего вида.
Почему стоит делать покупки в BENARI JEWELERS?
Вот уже более 50 лет BENARI JEWELERS предлагает своим клиентам высококачественные свадебные и модные украшения из розового золота.Если вы заинтересованы в том, что мы можем предложить, не стесняйтесь обращаться к нам по телефону 866-363-0808 или зайдите сегодня в наши демонстрационные залы Exton и Newtown Square, Pennsylvania, чтобы спросить о том, как найти подходящее для вас украшение из розового золота!
.



 Чтобы свинец не осел на стали полностью, используют поваренную соль с мучным клейстером для смазывания поверхностей заготовки.
Чтобы свинец не осел на стали полностью, используют поваренную соль с мучным клейстером для смазывания поверхностей заготовки. С высокой температурой или долгим периодом времени нагревания детали, оксидная пленка начинает менять толщину и меняется ее цвет.
С высокой температурой или долгим периодом времени нагревания детали, оксидная пленка начинает менять толщину и меняется ее цвет. В некотором случае инструмент накаливают на несколько мм выше резака до заданной температуры, далее после нагрева инструмента идет процесс охлаждения в воде, а рабочая часть остается горячей. Затем идет быстрое вынимание инструмента из воды, после чего рабочую часть защищают (наждачной бумагой или процессом трения о землю).После чего,теплота, остается в нейтральной части, затем повышает нагрев до охлажденного конца, в результате возникает необходимый цвет побежалости идет завершающий этап охлаждения.
В некотором случае инструмент накаливают на несколько мм выше резака до заданной температуры, далее после нагрева инструмента идет процесс охлаждения в воде, а рабочая часть остается горячей. Затем идет быстрое вынимание инструмента из воды, после чего рабочую часть защищают (наждачной бумагой или процессом трения о землю).После чего,теплота, остается в нейтральной части, затем повышает нагрев до охлажденного конца, в результате возникает необходимый цвет побежалости идет завершающий этап охлаждения. После,чего окалина извлекается из деталей либо механической обработкой или травлением.
После,чего окалина извлекается из деталей либо механической обработкой или травлением.
 Также полученная смесь более подвержена растрескиванию. Это особенно важно для штырей, которые могут быть хрупкими и трескаться легче, чем другие сплавы.
Также полученная смесь более подвержена растрескиванию. Это особенно важно для штырей, которые могут быть хрупкими и трескаться легче, чем другие сплавы. При носке он остается белым с приобретенной легкой патиной, что делает его уникальным.
При носке он остается белым с приобретенной легкой патиной, что делает его уникальным. Когда платина выходит из-под земли, она естественно белая. Платина всегда остается естественно белой без дополнительного ухода.
Когда платина выходит из-под земли, она естественно белая. Платина всегда остается естественно белой без дополнительного ухода. Родий относится к группе платиновых.Обычно родий гальванизируется для обеспечения консистенции и однородности цвета другого белого металла, используемого в ювелирных изделиях.
Родий относится к группе платиновых.Обычно родий гальванизируется для обеспечения консистенции и однородности цвета другого белого металла, используемого в ювелирных изделиях. Металл просто регулируется, чтобы оставить место для царапины. Это означает, что платина не теряет незначительного количества металла, которое исчезает при царапании других драгоценных металлов.Это объясняет, почему дизайнерские работы и гравировки на платиновых украшениях сохраняются гораздо дольше.
Металл просто регулируется, чтобы оставить место для царапины. Это означает, что платина не теряет незначительного количества металла, которое исчезает при царапании других драгоценных металлов.Это объясняет, почему дизайнерские работы и гравировки на платиновых украшениях сохраняются гораздо дольше. Хотя платина служит дольше, она также мягче (больше царапается). Платина более податлива, поэтому ее легче забивать или придавать форму, не ломая и не трескаясь.
Хотя платина служит дольше, она также мягче (больше царапается). Платина более податлива, поэтому ее легче забивать или придавать форму, не ломая и не трескаясь.
 Когда страх в экономике высок, цены на золото обычно также высоки.
Когда страх в экономике высок, цены на золото обычно также высоки. Любой ювелирный предмет, содержащий 950 частей платины или выше, может быть помечен только платиной или платиной.
Любой ювелирный предмет, содержащий 950 частей платины или выше, может быть помечен только платиной или платиной.