Медь, химические свойства | Технологии Металловъ
Химическая активность меди невелика. В сухой атмосфере медь практически не изменяется. Во влажном воздухе на поверхности меди в присутствии углекислого газа образуется зеленоватая пленка состава Cu(OH)2·CuCO3. Так как в воздухе всегда имеются следы сернистого газа и сероводорода, то в составе поверхностной пленки на металлической меди обычно имеются и сернистые соединения меди. Такая пленка, возникающая с течением времени на изделиях из меди и ее сплавов, называется патиной. Патина предохраняет металл от дальнейшего разрушения.
При нагревании на воздухе медь тускнеет и в конце концов чернеет из-за образования на поверхности оксидного слоя. Сначала образуется оксид Cu2O, затем — оксид CuO.
В сухом воздухе и кислороде при нормальных условиях медь не окисляется. Но она достаточно легко вступает в реакции: уже при комнатной температуре с галогенами, например с влажным хлором образует хлорид CuCl2, при нагревании с серой образует сульфид Cu Но с водородом, углеродом и азотом медь не взаимодействует даже при высоких температурах. Кислоты, не обладающие окислительными свойствами, на медь не действуют, например, соляная и разбавленная серная кислоты. Но в присутствии кислорода воздуха медь растворяется в этих кислотах с образованием соответствующих солей:
Но с водородом, углеродом и азотом медь не взаимодействует даже при высоких температурах. Кислоты, не обладающие окислительными свойствами, на медь не действуют, например, соляная и разбавленная серная кислоты. Но в присутствии кислорода воздуха медь растворяется в этих кислотах с образованием соответствующих солей:
2Cu + 4HCl + O2 = 2CuCl2 + 2H2O.
Кроме того, медь можно перевести в раствор действием водных растворов цианидов или аммиака:
2Cu + 8NH3·H2O + O2 = 2[Cu(NH3)4](OH)2 + 6H2O
При нагревании металла на воздухе или в кислороде образуются оксиды меди: желтый или красный Cu2O и черный CuO. Повышение температуры способствует образованию преимущественно оксида меди(I) Cu2O. В лаборатории этот оксид удобно получать восстановлением щелочного раствора соли меди(II) глюкозой, гидразином или гидроксиламином:
2CuSO4 + 2NH2OH + 4NaOH = Cu2O + N2 + 2Na2SO4 + 5H2O
Эта реакция – основа чувствительного теста Фелинга на сахара и другие восстановители. К испытываемому веществу добавляют раствор соли меди(II) в щелочном растворе. Если вещество является восстановителем, появляется характерный красный осадок.
К испытываемому веществу добавляют раствор соли меди(II) в щелочном растворе. Если вещество является восстановителем, появляется характерный красный осадок.
Поскольку катион Cu+ в водном растворе неустойчив, при действии кислот на Cu2O происходит либо дисмутация, либо комплексообразование:
Cu2O + H2SO4 = Cu + CuSO4 + H2O
Cu2O + 4HCl = 2 H[CuCl2] + H2O
Оксид Cu2O заметно взаимодействует со щелочами. При этом образуется комплекс:
Cu2O + 2NaOH + H2O = 2Na[Cu(OH)2]
Оксиды меди не растворимы в воде и не реагируют с ней. Единственный гидроксид меди Cu(OH)2 обычно получают добавлением щелочи к водному раствору соли меди(II). Бледно-голубой осадок гидроксида меди(II), проявляющий амфотерные свойства (способность химических соединений проявлять либо основные, либо кислотные свойства), можно растворить не только в кислотах, но и в концентрированных щелочах. При этом образуются темно-синие растворы, содержащие частицы типа [Cu(OH)4]2–. Гидроксид меди(II) растворяется также в растворе аммиака:
При этом образуются темно-синие растворы, содержащие частицы типа [Cu(OH)4]2–. Гидроксид меди(II) растворяется также в растворе аммиака:
Cu(OH)2 + 4NH3*H2O = [Cu(NH3)4](OH)2 + 4H2O
Гидроксид меди(II) термически неустойчив и при нагревании разлагается:
Cu(OH)2 = CuO + H 2O
Большой интерес к химии оксидов меди в последние два десятилетия связан с получением высокотемпературных сверхпроводников, из которых наиболее известен YBa2Cu3O7. В 1987 было показано, что при температуре жидкого азота это соединение является сверхпроводником. Главные проблемы, препятствующие его широкомасштабному практическому применению, лежат в области обработки материала. Сейчас наиболее перспективным считается изготовление тонких пленок.
Многие из халькогенидов меди – нестехиометрические соединения. Сульфид меди(I) Cu2S образуется при сильном нагревании меди в парах серы или в среде сероводорода. При пропускании сероводорода через водные растворы, содержащие катионы Cu2+, выделяется коллоидный осадок состава CuS. Однако, CuS – не простое соединение меди(II). Оно содержит группу S2 и лучше описывается формулой CuI
При пропускании сероводорода через водные растворы, содержащие катионы Cu2+, выделяется коллоидный осадок состава CuS. Однако, CuS – не простое соединение меди(II). Оно содержит группу S2 и лучше описывается формулой CuI
Практическое значение имеет способность меди реагировать с растворами солей железа (III), причем медь переходит в раствор, а железо (III) восстанавливается до железа (II):
2FeCl3 + Cu = CuCl2 + 2FeCl2
Этот процесс травления меди хлоридом железа (III) используют, в частности, при необходимости удалить в определенных местах слой напыленной на пластмассу меди.
Ионы меди Cu2+ легко образуют комплексы с аммиаком, например, состава [Cu(NH3)]2+. При пропускании через аммиачные растворы солей меди ацетилена С2Н2 в осадок выпадает карбид (точнее, ацетиленид) меди CuC 2.
При пропускании через аммиачные растворы солей меди ацетилена С2Н2 в осадок выпадает карбид (точнее, ацетиленид) меди CuC 2.
Химические свойства меди
Поговорим о первом из металлов, освоенных человеком. О меди. В периодической таблице химических элементов, медь находится в одиннадцатой группе, в так называемой, троице дорогих металлов – меди, серебра и золота. Согласно археологическим данным, первые медные изделия человек начал изготавливать в VII тысячелетии до н.э. То есть, около девяти тысяч лет назад. Из-за своей малой активности, медь была первым металлом, полученным человеком в чистом виде.
Процесс получения меди очень прост. Берется малахитовая руда или основной карбонат меди и смешивается с углем.
Затем смесь нагревается.
 Металлическая медь не растворяется в разбавленных серной и соляных кислотах, так как находится в ряду напряжений металлов после водорода. Однако, с концентрированной азотной кислотой, медь реагирует довольно активно, образуя диоксид азота — бурый газ и с неприятным запахом и нитрат меди. Если перейти к соединению меди, то самая часто встречающаяся медная соль, в обычной жизни, это конечно же, медный купорос и сульфат меди. Его используют для дезинфекции растений от насекомых, а так же в аналитической химии.
Металлическая медь не растворяется в разбавленных серной и соляных кислотах, так как находится в ряду напряжений металлов после водорода. Однако, с концентрированной азотной кислотой, медь реагирует довольно активно, образуя диоксид азота — бурый газ и с неприятным запахом и нитрат меди. Если перейти к соединению меди, то самая часто встречающаяся медная соль, в обычной жизни, это конечно же, медный купорос и сульфат меди. Его используют для дезинфекции растений от насекомых, а так же в аналитической химии.
Если к сульфату меди прилить гидроксид натрия, в осадок выпадет гидроксид меди, с помощью которого можно определить наличие сахара во фруктах. В стаканчик с гидроксидом меди добавим натертого яблока и нагреем смесь. Со временем, глюкоза, содержащаяся в яблочном соке, восстанавливает медь из двухвалентного состояния до одновалентного. И спустя время, раствор становится оранжевым.
В стаканчик с раствором медного купароса приливают мощный растворитель – раствор гидразина. При этом, атомы азота в гидразине окисляются, а медь восстанавливается из раствора до металла, покрывая стенки стакана блестящим, красивым слоем меди. Но на этом, свойства сульфата меди не заканчиваются. Если нагреть синий, привычный всем, сульфат меди, то со временем он побелеет, из-за того, что при нагревании сульфата меди, испаряется вода, оставляя безводный сульфат белого цвета. Если к такому сульфату меди добавить воды, синий цвет снова вернется. Так как, к молекуле сульфата меди снова присоединится вода, образуя кристаллогидрат. Если внести медный купорос в пламя горелки, то оно окрасится в зеленый цвет из-за ионов меди. Сама по себе, металлическая медь является одним из лучших проводников тепла и электричества. Из-за этого свойства, сейчас из меди делают провода во многих приборах, а также теплоотводов в компьютерах. Свойство меди хорошо проводить электричество я продемонстрирую на одном опыте. Сначала посмотрим, как падает мощный неодимовый магнит на поверхность стола. А теперь сравним с этим падением магнита медную пластину.
При этом, атомы азота в гидразине окисляются, а медь восстанавливается из раствора до металла, покрывая стенки стакана блестящим, красивым слоем меди. Но на этом, свойства сульфата меди не заканчиваются. Если нагреть синий, привычный всем, сульфат меди, то со временем он побелеет, из-за того, что при нагревании сульфата меди, испаряется вода, оставляя безводный сульфат белого цвета. Если к такому сульфату меди добавить воды, синий цвет снова вернется. Так как, к молекуле сульфата меди снова присоединится вода, образуя кристаллогидрат. Если внести медный купорос в пламя горелки, то оно окрасится в зеленый цвет из-за ионов меди. Сама по себе, металлическая медь является одним из лучших проводников тепла и электричества. Из-за этого свойства, сейчас из меди делают провода во многих приборах, а также теплоотводов в компьютерах. Свойство меди хорошо проводить электричество я продемонстрирую на одном опыте. Сначала посмотрим, как падает мощный неодимовый магнит на поверхность стола. А теперь сравним с этим падением магнита медную пластину.
Сейчас из меди изготавливают и медные трубы. Медь входит в состав и множества сплавов, таких, как бронзовые сплавы, семейство латунных сплавов, мельхиор и другие. Многим известно выражение – «голубая кровь». В действительности, ни земле есть существа, кровь которых голубого цвета из-за содержащегося в ней белка гемоцианина, аналога гемоглобина, содержащего ионы меди вместо ионов железа. Голубую кровь мечехвостов используют для тестирования медицинских препаратов на наличие заражения. Оказалось, что обычная и всем привычная медь является не такой простой, как кажется.
В действительности, ни земле есть существа, кровь которых голубого цвета из-за содержащегося в ней белка гемоцианина, аналога гемоглобина, содержащего ионы меди вместо ионов железа. Голубую кровь мечехвостов используют для тестирования медицинских препаратов на наличие заражения. Оказалось, что обычная и всем привычная медь является не такой простой, как кажется.
польза и вред. Как ухаживать за медной посудой.
Медная посуда: польза и вред. Как ухаживать за медной посудой. Многие кулинары-любители мечтают раскрыть секреты знаменитых поваров. Но бывает, что необыкновенный вкус приготовленного блюда зависит не столько от правильно подобранных составляющих и всевозможных специй, сколько от полезных качеств используемой посуды. На кухне дорогого ресторана, где работают профессионалы, и у опытной хозяйки всегда найдется медная посуда. Польза и вред, оказываемые ею на здоровье человека, обязательно должны учитываться перед приобретением этих предметов кухонной утвари. Достоинства медной посуды Наиболее важной характеристикой медной посуды следует считать ее высокую теплопроводность, которая в 10 раз выше, чем у стальной или алюминиевой емкости. Это способствует равномерному распределению тепла по всей поверхности, что значительно ускоряет процесс приготовления пищи, не снижая ее вкусовые качества. Считается, что особенно вкусное варенье или пикантный соус получаются, если готовятся именно в медной посуде. За счет снижения времени на термическую обработку пищи ее полезные вещества сохраняются. Легкий вес и долговечность также являются неоспоримыми достоинствами, которыми обладает медная посуда. Польза и вред, которые может принести медь здоровью человека, заслуживают отдельного внимания. Полезные свойства медной посуды На протяжении многих веков используется людьми медная посуда. Свойства, недостатки, и как ухаживать за кастрюлями и сковородками, выполненными из меди, — все это известно с давних пор. Одним из самых главных полезных свойств медной посуды следует назвать ее антибактериальное действие.
Достоинства медной посуды Наиболее важной характеристикой медной посуды следует считать ее высокую теплопроводность, которая в 10 раз выше, чем у стальной или алюминиевой емкости. Это способствует равномерному распределению тепла по всей поверхности, что значительно ускоряет процесс приготовления пищи, не снижая ее вкусовые качества. Считается, что особенно вкусное варенье или пикантный соус получаются, если готовятся именно в медной посуде. За счет снижения времени на термическую обработку пищи ее полезные вещества сохраняются. Легкий вес и долговечность также являются неоспоримыми достоинствами, которыми обладает медная посуда. Польза и вред, которые может принести медь здоровью человека, заслуживают отдельного внимания. Полезные свойства медной посуды На протяжении многих веков используется людьми медная посуда. Свойства, недостатки, и как ухаживать за кастрюлями и сковородками, выполненными из меди, — все это известно с давних пор. Одним из самых главных полезных свойств медной посуды следует назвать ее антибактериальное действие. Медь способна бороться с целым рядом грибков и бактерий, не допуская их попадания в пищу. В старину в медных емкостях хранили воду с целью ее обеззараживания. Американские ученые экспериментальным путем доказали, что медь успешно справляется со штаммами сальмонеллы, а также кишечной палочки. Пища, которая готовится в медной посуде, обеззараживается, предотвращая появление заболеваний желудочно-кишечного тракта. Недаром издавна медь применялась в народной медицине для лечения многих заболеваний: при интоксикации организма, судорогах, язвах, геморрое и т. д. Вред медной посуды Кроме положительных свойств, которыми обладает медь, ученые обнаружили и ряд отрицательных факторов, которые могут нанести вред здоровью или негативно повлиять на качество приготовляемых в такой посуде продуктов: Аскорбиновая кислота, которая содержится во фруктах и ягодах, под агрессивным воздействием меди разрушается. При хранении продуктов в медной посуде происходит потеря витаминов и окисление полиненасыщенных жирных кислот, что может способствовать возникновению онкозаболеваний.
Медь способна бороться с целым рядом грибков и бактерий, не допуская их попадания в пищу. В старину в медных емкостях хранили воду с целью ее обеззараживания. Американские ученые экспериментальным путем доказали, что медь успешно справляется со штаммами сальмонеллы, а также кишечной палочки. Пища, которая готовится в медной посуде, обеззараживается, предотвращая появление заболеваний желудочно-кишечного тракта. Недаром издавна медь применялась в народной медицине для лечения многих заболеваний: при интоксикации организма, судорогах, язвах, геморрое и т. д. Вред медной посуды Кроме положительных свойств, которыми обладает медь, ученые обнаружили и ряд отрицательных факторов, которые могут нанести вред здоровью или негативно повлиять на качество приготовляемых в такой посуде продуктов: Аскорбиновая кислота, которая содержится во фруктах и ягодах, под агрессивным воздействием меди разрушается. При хранении продуктов в медной посуде происходит потеря витаминов и окисление полиненасыщенных жирных кислот, что может способствовать возникновению онкозаболеваний.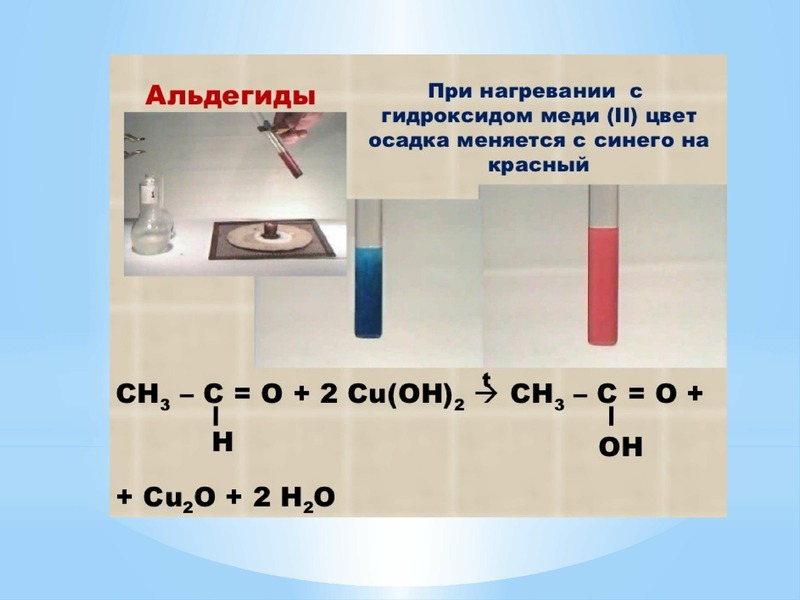 Вред посуды особенно серьезен, если она находится во влажной среде. Повышенная влажность вызывает окисление меди, это проявляется в виде зеленого налета. При взаимодействии с пищевыми кислотами во время нагревания вырабатываются особо вредные для организма вещества. Поэтому при появлении на посуде такого налета необходимо его тщательно удалить, протерев поверхность поваренной солью, смоченной в уксусе. Покрытие медной посуды С продуктами, обладающими повышенной кислотностью, медная посуда взаимодействует отрицательно. Для того чтобы предотвратить окисление и сделать приготовление пищи безопасным, изнутри медную емкость покрывают обычно специальными сплавами олова, железа или никеля. Когда такое покрытие протирается — посуду следует менять. При приготовлении пищи в медной посуде лучше всего пользоваться деревянной лопаточкой, чтобы не поцарапать внутреннюю поверхность. Уход за посудой из меди Медная посуда нуждается в более бережном уходе по сравнению с какой-либо другой. Ее необходимо периодически тщательно полировать, чтобы избежать налета, соблюдать условия хранения — такая посуда не терпит высокой влажности.
Вред посуды особенно серьезен, если она находится во влажной среде. Повышенная влажность вызывает окисление меди, это проявляется в виде зеленого налета. При взаимодействии с пищевыми кислотами во время нагревания вырабатываются особо вредные для организма вещества. Поэтому при появлении на посуде такого налета необходимо его тщательно удалить, протерев поверхность поваренной солью, смоченной в уксусе. Покрытие медной посуды С продуктами, обладающими повышенной кислотностью, медная посуда взаимодействует отрицательно. Для того чтобы предотвратить окисление и сделать приготовление пищи безопасным, изнутри медную емкость покрывают обычно специальными сплавами олова, железа или никеля. Когда такое покрытие протирается — посуду следует менять. При приготовлении пищи в медной посуде лучше всего пользоваться деревянной лопаточкой, чтобы не поцарапать внутреннюю поверхность. Уход за посудой из меди Медная посуда нуждается в более бережном уходе по сравнению с какой-либо другой. Ее необходимо периодически тщательно полировать, чтобы избежать налета, соблюдать условия хранения — такая посуда не терпит высокой влажности. Это для меди враг номер один. Не рекомендуется мыть медные предметы в посудомоечной машине, т. к. использование при этом сильных моющих средств может повредить их, значительно сократив срок службы. По этой же причине не стоит применять для чистки моющие средства, содержащие отбеливатель. Для мытья нужно использовать мягкую тряпочку или губку без абразивного слоя, чтобы не повредить защитный слой на внутренней поверхности.
Это для меди враг номер один. Не рекомендуется мыть медные предметы в посудомоечной машине, т. к. использование при этом сильных моющих средств может повредить их, значительно сократив срок службы. По этой же причине не стоит применять для чистки моющие средства, содержащие отбеливатель. Для мытья нужно использовать мягкую тряпочку или губку без абразивного слоя, чтобы не повредить защитный слой на внутренней поверхности.
Как очистить медь | Средства и советы по уходу
Изделия из меди отличаются долговечностью и роскошным внешним видом и часто используются не только в бытовых, но и декоративных целях.
Медная посуда обладает хорошей теплопроводимостью, что позволяет ей быстро и эффективно нагревать еду. Ювелирные украшения из меди выглядят элегантно, а некоторые медики рекомендуют носить медные браслеты людям с заболеваниями сердечно-сосудистой системы, так как этот металл нормализует давление и оказывает благотворное влияние на здоровье человека.
Однако, с течением времени, медь тускнеет, мутнеет и покрывается зеленоватым налетом. Это неизбежный процесс окисления металла, происходящий в результате контакт с кислородом, особенно при нагревании. Но если предотвратить старение металла невозможно, то вернуть медным изделиям первозданный блеск в домашних условиях можно в два счета.
Это неизбежный процесс окисления металла, происходящий в результате контакт с кислородом, особенно при нагревании. Но если предотвратить старение металла невозможно, то вернуть медным изделиям первозданный блеск в домашних условиях можно в два счета.
Помните, какой бы способы чистки меди вы ни выбрали, внимательно ознакомьтесь с инструкциями, а затем протестируйте его на небольшом и малозаметном участке поверхности.
Способы чистки меди
Существует множество специальных средств, а также народных рецептов очистки медных изделий от окиси и удаления темного налета:
- Наиболее простой способ чистки медных предметов – это поместить их в горячую воду с добавлением моющего средства, потереть мягкой губкой или тряпкой и промыть водой
- Если медный предмет невозможно поместить в кастрюлю, попробуйте натереть его долькой лимона, почистить щеткой, а затем вымыть водой
- Для придания изделию блеска, натрите его смесью муки, крупной соли и уксуса, затем отполируйте мягкой тканью
- Также рекомендуется полировать изделие смятой в небольшой шар газетой – старое доброе средство, которым наши бабушки чистили окна
- Для чистки старинных изделий и борьбы с сильными загрязнениями, рекомендуется прокипятить медные предметы в растворе уксуса с добавлением двух столовых ложек соли.
 Когда изделие остынет, промойте его водой и насухо вытрите мягкой тряпкой
Когда изделие остынет, промойте его водой и насухо вытрите мягкой тряпкой - Самый необычный метод, рекомендуемый многими домохозяйками, это чистка меди обыкновенным томатным кетчупом. Нанесите густой слой кетчупа на изделие и оставьте на несколько минут, затем смойте водой. Это придаст изделию блеск и теплый красноватый оттенок, характерный для этого металла
Чистка медных монет и антикварных изделий
Чистить предметы, имеющие высокую рыночную стоимость, в домашних условиях нужно крайне осторожно, чтобы не испортить дорогостоящего изделия. Способ чистки зависит от типа загрязнения:
- Чтобы удалить зеленоватый налет, поместите изделие в 10% раствор лимонной кислоты. Когда увидите, что налет растворяется, выньте, промойте и отполируйте медный предмет
- Для удаления красноватого налета, поместите изделие в 5% раствор аммиака или углекислый аммоний, пока не увидите желаемого результата
- Желтоватый налет образуется в результате контакта со свинцом.
 Удалить его можно погрузив предмет в 10% раствор уксуса
Удалить его можно погрузив предмет в 10% раствор уксуса
Чтобы вернуть изделию былой блеск и придать товарный вид, нанесите на него слой искусственной платины. Растворите 50 граммов медного купороса и 5 граммов марганцовки в литре дистиллированной воды. Нагрейте смесь до 80-90 градусов, поместите медные изделия и оставьте на некоторое время, периодически переворачивая. Добившись желаемого результата, высушите медные изделия и покройте защитным слоем спирта и бензола, смешанных в равных пропорциях.
Оксид меди(II) — это… Что такое Оксид меди(II)?
Окси́д ме́ди(II) (окись меди) CuO — основный оксид двухвалентной меди. Кристаллы чёрного цвета, в обычных условиях довольно устойчивые, практически нерастворимые в воде. В природе встречается в виде минерала тенорита (мелаконита) чёрного цвета.
Кристаллическая решётка оксида меди относится к типу моноклинных решёток, с симметрией группы C2h и параметрами решётки a = 4.6837(5), b = 3. 4226(5), c = 5.1288(6), α = 90° , β = 99.54(1)°, γ = 90°. Атом меди окружён четырьмя атомами кислорода и имеет искажённую плоскую конфигурацию.
4226(5), c = 5.1288(6), α = 90° , β = 99.54(1)°, γ = 90°. Атом меди окружён четырьмя атомами кислорода и имеет искажённую плоскую конфигурацию.
Получение
Получить оксид меди(II) можно:
- нагревая металлическую медь на воздухе (при температурах ниже 1100 °C получается оксид меди(II):
Химические свойства
Оксид меди(II) реагирует с кислотами с образованием соответствующих солей меди(II) и воды:
При сплавлении CuO со щелочами образуются купраты:
При нагревании до 1100 °C разлагается:
Оксиду меди(II) соответствует гидроксид меди(II) Cu(OH)2, который является очень слабым основанием. Он способен растворяться в концентрированных растворах щелочей с образованием комплексов (то есть обладает слабыми амфотерными свойствами):
- (тетрагидроксокупрат(II) натрия).

- (тетрагидроксокупрат(II) натрия).
Оксид меди(II) восстанавливается до металлической меди аммиаком, монооксидом углерода, водородом, углем:
Применение
CuO используют при производстве стекла и эмалей для придания им зелёной и синей окраски. Кроме того, оксид меди применяют в производстве медно-рубинового стекла.
В лабораториях применяют для обнаружения восстановительных свойств веществ. Вещество восстанавливает оксид до металлической меди, при этом чёрный цвет оксида меди переходит в розовую окраску меди.
Примечания
- ↑ под давлением О2
Литература
- Реми Г. «Курс неорганической химии» М.: Иностранная литература, 1963
- The effect of hydrostatic pressure on the ambient temperature structure of CuO, Forsyth J.B., Hull S., J. Phys.: Condens. Matter 3 (1991) 5257-5261
Меди сульфат трехосновный | справочник Пестициды.ru
Физико-химические свойства
Сульфат меди трехосновный – смесь гидроксида меди и сульфата меди (содержащая 2 части сульфата и одну часть гидроксида). Основным компонентом является сульфат меди СuSO4.
Основным компонентом является сульфат меди СuSO4.
Сульфат меди
Сульфат меди СuSO4 – белое, весьма гигроскопичное вещество. Низкоплавкое, при сильном нагревании разлагается.[3]
Физические характеристики
- Молекулярная масса 159,61
- Относительная плотность (при комн.температуре) 3,603;
- Температура плавления ~ 200 °С.[3]
Получение
Сульфат меди получают взаимодействием меди с безводной серной кислотой. 2Сu + 2H2SO4 (безводн). = Сu2SO4↓ + 2H2O + SO2↑ (200 °С).[3]
Гидроксид меди
Гидроксид меди Cu(OH)2 – кристаллическое вещество ярко-голубого цвета или аморфное соединение светло-голубого. Термически неустойчиво. В воде не растворяется, в раствор переводится действием гидрата аммиака. Проявляет амфотерные свойства (преобладание основных свойств). Реагирует с концентрированными щелочами, разбавленными кислотами. Слабый окислитель и восстановитель.[3]
Реагирует с концентрированными щелочами, разбавленными кислотами. Слабый окислитель и восстановитель.[3]
Физические характеристики
- Молекулярная масса 97,56;
- Относительная плотность (комн.температура) 3,368 (аморфн.).[3]
Получение
Гидроксид меди может быть получен по следующим реакциям:
- Сu(NO3)2 + 2NaOH (разб.)= Cu(OH)2↓ + 2NaNO3;
- Сu2SO4 (разб.) + 2NaOH (т.)= Cu(OH)2↓ + Na2SO4.[3]
Пестициды, содержащие
Меди сульфат трехосновный
для сельского хозяйства:
для личных подсобных
хозяйств:
закончился срок регистрации:
Применение
Зарегистрированные препараты на основе сульфата меди трехосновного разрешены к применению в сельском хозяйстве против болезней яблони (парша), томата (фитофтороз), огурцы (угловатая бактериальная пятнистость, пероноспороз), свеклы сахарной (церкоспороз, мучнистая роса), винограда (милдью). [2]
[2]
Баковые смеси. Препарат совместим со многими фунгицидами и инсектицидами.[6]
Фитотоксичность. При соблюдении рекомендаций по применению препарат не фитотоксичен. На сортах яблони, которые чувствительны к медьсодержащим препаратам, при опрыскивании после цветения может образоваться «сетка» на плодах и листьях.[6]
Токсикологические данные |
|
| ДСД (мг/кг массы тела человека) | 0,17 |
| ПДК в почве (мг/кг) | 3,0 |
| ПДК в воде водоемов (мг/дм3) | 1,0 (орг.) |
| ПДК в воздухе рабочей зоны (мг/м3) | 0,5 |
| ПДК в атмосферном воздухе (мг/м3) | 0,0008 |
| МДУ в продукции (мг/кг): | |
в бахчевых |
5,0 |
в винограде |
5,0 |
в картофеле |
2,0 |
в луке |
5,0 |
в мясе |
2,0 |
в овощах |
5,0 |
в огурцах |
5,0 |
в плодовых (косточковые, семечковые) |
5,0 |
в свекле сахарной |
5,0 |
в томатах |
5,0 |
в цитрусовых |
20,0 |
в ягодах |
5,0 |
в яйцах |
2,0 |
| ВМДУ в продукции (мг/кг): | |
в хмеле сухом |
10,0 |
Токсикологические свойства и характеристики
Препарат запрещено применять в санитарной зоне вокруг рыбохозяйственных водоемов. [4]
[4]
Энтомофаги. Малоопасен для пчел.[6]
Классы опасности. Препараты на основе сульфата меди трехосновного относятся к 3 классу опасности для человека и 3 классу опасности для пчел.[2]
Таблица Токсикологические данные составлена в соответствии с ГН 1.2.3111-13.[1]
Соединения меди | справочник Пестициды.ru
Пестициды, содержащие медь, широко применяются для защиты садов и виноградников от вредителей и болезней, а также в качестве протравителей семян. Соединения меди являются одной из наиболее важных групп фунгицидов, используемых самостоятельно и в смеси с другими органическими препаратами.[6]
Более ста лет они находят применение в борьбе с ложномучнисторосяными и несовершенными грибами, вызывающими пятнистости вегетативных органов растений. Это основная группа препаратов в системе антирезистентной программы к системным фунгицидам. [2]
[2]
История
В 1761 г. Шалтесом или в 1783 г. Тессиром был предложен сульфат меди для протравливания семян пшеницы. В 1807 г. Превост опубликовал данные о головневых болезнях пшеницы и борьбе с ними, а также о влиянии сульфата меди и температуры на прорастание хламидоспор головни. Таким образом, были заложены основы лабораторных испытаний фунгицидов.[3] Во Франции в 1887 г. А.Милярде и У.Гейон предложили смесь раствора с известковым молоком (бордоская жидкость), которую до сих пор применяют в защите растений.[2]
Бордоская смесьБордоская смесь
Установка, применяемая для приготовления бордоской жидкости в начале прошлого века.
Использовано изображение: [8]
Действие на вредные организмы
Все препараты на основе солей меди являются контактными фунгицидами защитного действия. Они активно подавляют прорастание конидий и спор грибов только в момент прорастания в капле воды и обладают бактерицидными свойствами. Для обеспечения высокой эффективности препараты меди должны быть нанесены на растения до начала прорастания конидий или спор патогена. Большое значение имеет равномерное и тщательное покрытие всего растения. Продолжительность защитного действия зависит от метеорологических условий (осадки), качества препаративной формы (размер частиц, прилипаемость) и скорости роста растения. Обычно защитное действие длится не более 10 дней.[7]
Они активно подавляют прорастание конидий и спор грибов только в момент прорастания в капле воды и обладают бактерицидными свойствами. Для обеспечения высокой эффективности препараты меди должны быть нанесены на растения до начала прорастания конидий или спор патогена. Большое значение имеет равномерное и тщательное покрытие всего растения. Продолжительность защитного действия зависит от метеорологических условий (осадки), качества препаративной формы (размер частиц, прилипаемость) и скорости роста растения. Обычно защитное действие длится не более 10 дней.[7]
Соединения меди, —
действующие вещества
Важная роль в фунгитоксичности принадлежит сорбционной способности протоплазмы клеток грибов и переходу ионов меди в раствор из осадка на листьях. Растворенная медь адсорбируется спорами, вследствие чего равновесие нарушается, и часть меди снова переходит в растворимое состояние. Данный процесс происходит до тех пор, пока спорой не кумулируется токсическая доза. Переводу меди в раствор способствуют аммонийные соли, углекислота и другие вещества, присутствующие в атмосфере, росе, осадках, выделениях листьев, спор грибов.[3]
Растворенная медь адсорбируется спорами, вследствие чего равновесие нарушается, и часть меди снова переходит в растворимое состояние. Данный процесс происходит до тех пор, пока спорой не кумулируется токсическая доза. Переводу меди в раствор способствуют аммонийные соли, углекислота и другие вещества, присутствующие в атмосфере, росе, осадках, выделениях листьев, спор грибов.[3]
Как и все препараты контактного действия, медьсодержащие соединения не проникают внутрь листа, поэтому не могут вызвать гибель находящихся там гиф и мицелия гриба. Они взаимодействуют в основном со спорами, препятствуя их прорастанию.[1]
Биологические свойства медьсодержащих препаратов определяются способностью ионов меди активно реагировать с ферментными и липопротеиновыми комплексами живых клеток и вызывать необратимые изменения (коагуляцию) протоплазмы. Ионы меди, поступившие в достаточно высокой концентрации в клетки патогена, взаимодействуют с различными ферментами, содержащими имидазольные, карбоксильные и тиольные группы, и подавляют их активность. Прежде всего, при этом ингибируются процессы, которые входят в дыхательный цикл, в частности, процесс превращения пировиноградной кислоты в ацетилфермент А. Также они вызывают неспецифическую денатурацию белков. Их избирательность по отношению к полезным организмам зависит от количества ионов меди, поступивших в клетки и накопившихся в них. Конидии и споры грибов, прорастающие на поверхности растений в капле воды, способны внутри своей клетки накапливать ионы меди, создавая концентрацию в 100 и более раз выше, чем в растительных клетках или снаружи.[7]
Прежде всего, при этом ингибируются процессы, которые входят в дыхательный цикл, в частности, процесс превращения пировиноградной кислоты в ацетилфермент А. Также они вызывают неспецифическую денатурацию белков. Их избирательность по отношению к полезным организмам зависит от количества ионов меди, поступивших в клетки и накопившихся в них. Конидии и споры грибов, прорастающие на поверхности растений в капле воды, способны внутри своей клетки накапливать ионы меди, создавая концентрацию в 100 и более раз выше, чем в растительных клетках или снаружи.[7]
Бордоская смесь обладает репеллентными свойствами для многих насекомых.[3]
. Бордоская смесь не эффективна против пероноспороза махорки и табака, а также против настоящих мучнистых рос.[5]. Бордоская смесь подавляет листоблошек на картофеле. Проявляет овицидное действие.[3] Бордосская жидкостьБордосская жидкость
Применение
Медьсодержащие соединения используются для предупреждения заболеваний растений. Их применяют заранее, до появления массового заражения.[1]
Их применяют заранее, до появления массового заражения.[1]
Соединения меди активно подавляют развитие пятнистостей винограда, сахарной свеклы, ложных мучнистых рос, макроспориоза и фитофтороза картофеля, монилиоза, ржавчины, парши семечковых, кластероспороза и коккомикоза косточковых плодовых культур, а также сдерживают развитие настоящей мучнистой росы и ряда бактериозов.[7]
. Бордоскую жидкость нельзя смешивать с фосфорорганическими инсектицидами и другими препаратами, которые разлагаются в щелочной среде.[4]Хлорокись меди входит в состав многих комбинированных фунгицидов.[2] Суспензию можно применять совместно с большинством пестицидов, но нельзя смешивать с препаратами, содержащими известь. Средство применяется также в смеси с антииспарителями.[1]
. Фитотоксичность особенно проявляется в годы с повышенной влажностью воздуха и продолжительным периодом выпадения осадков, а также в период активного роста растений. Кроме того, многолетнее использование медьсодержащих фунгицидов (при их накоплении в почве) отрицательно действует на деревья, вызывая сильное опадение листьев и завязей в начале лета.[1]
Кроме того, многолетнее использование медьсодержащих фунгицидов (при их накоплении в почве) отрицательно действует на деревья, вызывая сильное опадение листьев и завязей в начале лета.[1]Фитотоксичность препаратов меди зависит от концентрации меди в растворе на поверхности растений и способности стеблей и листьев поглощать ее ионы.[7]
В связи с тем, что фитотоксичность сильнее проявляется в период активного роста растений, рекомендуется чередование обработок медьсодержащими препаратами с обработками органическими средствами. Перед цветением растений и во время него следует применять органические препараты, безопасные для цветков и стимулирующие рост побегов и листьев. Перед созреванием плодов используют хлорокись меди. Она менее фитотоксична, чем бордоская жидкость, но хуже удерживается на растениях.[4]
Токсикологические свойства и характеристики
. Бордоская смесь не является ядовитой для хищных клещей, личинок и имаго златоглазок, кокцинеллид, хищных галлиц и таких перепончатокрылых, как их невмониды, афелиниды, птеромалиды. [3]
[3]Хлорокись меди не токсична для яиц златоглазки, умеренно токсична для ее личинок и имаго; высокотоксична для перепончатокрылых из семейства трихограмматид.[3]
. Препараты меди ядовиты для человека и теплокровных животных. Доза 10 г является абсолютно смертельной для человека. Дозы 0,2-0,5 г вызывают рвоту.[6]. Соединения меди стабильны во внешней среде, активно участвуют в кругообороте веществ в природе, переходят из почвы в растения, употребляемые человеком и животными. Установлено, что применение бордоской жидкости для опрыскивания яблоневого сада и виноградников, ранее не обрабатываемых никакими пестицидами, приводило к увеличению содержания меди в почве.[6] Поведение попавших в почву медьсодержащих пестицидов зависит в основном от типа почвы, ее физико-химических свойств, содержания гумуса, влажности. При внесении пестицидов в почву, а также при различных способах обработки наземных частей растений могут загрязняться как открытые водоемы, так и подземные источники водоснабжения. В воде колодца, питающегося грунтовыми водами и расположенного на супесчаной почве, количество меди за вегетационный период повысилось в 10 раз.[6]
В воде колодца, питающегося грунтовыми водами и расположенного на супесчаной почве, количество меди за вегетационный период повысилось в 10 раз.[6]
Установлено также, что медь и ее соединения оказывают бактерицидное действие на микроорганизмы почвы и водоемов, что может привести к угнетению почвенной микрофлоры и процессов минерализации органических веществ.[6]
. Установлено, что при применении медьсодержащих пестицидов загрязняются также плоды. Так, концентрация меди в яблоках, обработанных 1%-ной бордоской жидкостью, составляла 4,14 мг/кг, в то время как в плодах, отобранных на контрольном участке, содержалось 0,93 мг/кг.[6]. Соли меди при непосредственном воздействии на ткани образуют с тканевыми белками альбуминаты, что обуславливает их вяжущее и прижигающее действие. Они сильно раздражают слизистые оболочки желудочно-кишечного тракта, а также верхних дыхательных путей.[6] Клиническая картина отравления человека при попадании соединений меди в желудочно-кишечный тракт характеризуется неприятным металлическим и вяжущим вкусом во рту, обильным слюнотечением, тошнотой, рвотой. Рвотные массы окрашены в зеленый или сине-зеленый цвет. Отмечаются схваткообразные боли в животе. Резко выражено гемолитическое действие с быстрым появлением билирубина в плазме и моче, отмечается желтуха, иногда уремия, обнаруживается белок в моче, развивается слабость, головокружение, затрудненное дыхание.[6]
Рвотные массы окрашены в зеленый или сине-зеленый цвет. Отмечаются схваткообразные боли в животе. Резко выражено гемолитическое действие с быстрым появлением билирубина в плазме и моче, отмечается желтуха, иногда уремия, обнаруживается белок в моче, развивается слабость, головокружение, затрудненное дыхание.[6]
При поступлении солей меди (СuCO3, CuSO4) через дыхательные пути развивается симптомокомплекс «меднопротравной» лихорадки. Описаны случаи отравления работающих на протравливании зерна углекислой медью. Явления интоксикации начинались с сильного озноба, продолжающегося несколько часов, повышения температуры тела (до 39). При тяжелой форме интоксикации заболевание может длиться три-четыре дня.[6]
Соединения меди могут оказывать также местнораздражающее действие на кожу: иногда появляется мелкая красная сыпь с зудом, экзема, кожная пурпура.[6]
Особенно опасным является поступление солей меди в виде пыли в дыхательные пути. При этом наблюдаются признаки раздражения слизистой оболочки верхних дыхательных путей, сильный бронхиальный кашель в сочетании с рвотой и болями в желудке, носовые кровотечения. Хроническая токсичность соединений меди не выражена.[7]
При этом наблюдаются признаки раздражения слизистой оболочки верхних дыхательных путей, сильный бронхиальный кашель в сочетании с рвотой и болями в желудке, носовые кровотечения. Хроническая токсичность соединений меди не выражена.[7]
Статья составлена с использованием следующих материалов:
Литературные источники:
1.Белов Д.А. Химические методы и средства защиты растений в лесном хозяйстве и озеленении: Учебное пособие для студентов. –М.: МГУЛ, 2003. – 128 с
2.Ганиев М.М., Недорезков В.Д. Химические средства защиты растений. – М.: КолосС, 2006. – 248 с.
3.Голышин Н. М. Фунгициды. — М.: Колос, 1993. -319 с.: ил.
4.Груздев Г.С. Химическая защита растений. Под редакцией Г.С. Груздева — 3-е изд., перераб. и доп. — М.: Агропромиздат, 1987. — 415 с.: ил.
5.Зинченко В.А. Химическая защита растений: средства, технология и экологическая безопасность. – М.: «КолосС», 2012. – 127 с.
6.Медведь Л.И. Справочник по пестицидам (гигиена применения и токсикология) / Коллектив авторов, под ред. академика АМН СССР, профессора Медведя Л.И. -К.: Урожай, 1974. 448 с.
академика АМН СССР, профессора Медведя Л.И. -К.: Урожай, 1974. 448 с.
Попов С.Я. Основы химической защиты растений. Попов С.Я., Дорожкина Л.А., Калинин В.А./ Под ред. профессора С.Я Попова. — М.: Арт-Лион, 2003. — 208 с.
Изображения (переработаны):
8.Altus Lacy Quaintance, Cornelius Lott Shear U.S. Dept. of Agriculture, 1907. Иллюстрации из книги
Свернуть Список всех источниковМедь в вашем доме: водопровод, отопление и охлаждение
Системы лучистого отопления
Для комфорта в помещении нет ничего лучше лучистого отопления. Лучистые полы с подогревом существуют уже много веков, начиная с римлян, которые выпускали горячий воздух под полы своих вилл. Популярное в Европе в течение последних нескольких десятилетий, а теперь, когда энергоэффективность является горячей темой для домовладельцев и строителей, лучистое отопление становится все более популярным среди американских домовладельцев и строителей.
Люди не только любят просыпаться и не наступать на холодный пол, им также нравится простота управления и бесшумная работа, дизайнерские возможности — можно использовать практически любое напольное покрытие — экономичность и надежность. А для оптимальной теплопередачи нет ничего лучше медных трубок.
А для оптимальной теплопередачи нет ничего лучше медных трубок.
Существует три типа лучистого напольного отопления: водяное (водяное), электрическое и принудительное, при котором горячий воздух направляется через пол. Эти системы бывают двух типов установки.При «мокрой» установке трубы закладываются в бетонную плиту или легкий бетон поверх деревянного основания. При сухой установке трубы излучающего пола протягивают между двумя слоями фанеры или прикрепляют под готовым полом.
Хотя каждый тип системы является функциональным и подходит для определенных применений, с точки зрения жилых домов, есть некоторые недостатки. Системы лучистого воздуха, например, не очень распространены в жилых помещениях, потому что воздух не удерживает и не удерживает большое количество тепла, что делает их не очень рентабельными.Электрические системы могут быть рентабельными только в том случае, если вы живете в районе, где тарифы на электроэнергию низкие или ваша электроэнергетическая компания предлагает тарифы на время использования. Эти планы позволяют вам «заряжать» полы — создавать запас тепла — в непиковые часы, экономя значительную энергию и деньги по сравнению с использованием того же количества электроэнергии в часы пик.
Эти планы позволяют вам «заряжать» полы — создавать запас тепла — в непиковые часы, экономя значительную энергию и деньги по сравнению с использованием того же количества электроэнергии в часы пик.
Гидравлические (жидкостные) системы — самые популярные и экономичные системы лучистого отопления для жилых помещений. Эти системы работают, перекачивая горячую воду по трубам, проложенным под полом.Зональные клапаны и термостаты регулируют температуру в отдельных помещениях по всей системе.
Медь используется в системах водяного лучистого отопления с 1940-х годов. Это выбор многих установщиков и домовладельцев из-за его превосходных характеристик теплопередачи. Он также негорючий и чрезвычайно надежный.
Температура воды очень важна в системах лучистого отопления. Системы лучистого отопления работают с температурой воды 90-140 градусов. Для сравнения, плинтус или радиаторная система с горячей водой работает при температуре воды 160-210 градусов.150 градусов могут потенциально повредить систему лучистого отопления или ее трубки. Однако медная трубка способна выдерживать температуры и колебания без повреждения самой трубки.
Однако медная трубка способна выдерживать температуры и колебания без повреждения самой трубки.
Системы лучистого отопления с медными трубами и фитингами имеют явные преимущества перед другими материалами. Помимо свойств теплопередачи, отожженная медная труба намного прочнее, чем резиновая или пластмассовая. Паяные медные соединения — самые надежные из соединений. Они редко, если вообще когда-либо, ломаются или портятся.Излучающие системы с медными и латунными соединениями также легче установить, потому что фитинги стандартизированы. Установщики могут найти совместимые детали в любом магазине сантехники, и им не нужно ограничиваться одним поставщиком или производителем, как в случае патентованных систем пластиковых или резиновых трубок. Поскольку стоимость медных трубок сейчас значительно ниже, чем несколько лет назад, они становятся все более популярными из-за своих превосходных теплопередающих свойств по сравнению с трубками на пластиковой основе.
Еще одним положительным признаком медных систем лучистого отопления является то, что медная трубка обладает внутренним сопротивлением проникновению кислорода, что предотвращает образование точечных утечек. Хотя производители других излучающих систем ввели меры предосторожности против повреждений, вызванных проникновением кислорода, они все еще не зарекомендовали себя испытанием временем, как медь.
Хотя производители других излучающих систем ввели меры предосторожности против повреждений, вызванных проникновением кислорода, они все еще не зарекомендовали себя испытанием временем, как медь.
Если медные системы установлены и правильно обслуживаются, они могут прослужить всю жизнь. Некоторым медным излучающим системам уже 70 лет, и у них никогда не было ни одной утечки. Системы лучистого отопления из меди также используются для наружной установки для таяния снега на наклонных проездах, тротуарах, парковках и пешеходных зонах.
Тепловые насосы
Одним из наиболее рентабельных средств отопления и охлаждения являются геотермальные тепловые насосы. Для получения дополнительной информации перейдите по ссылкам ниже:
Контакты для теплового насоса Информация:
Крис Пэмплин
American Geothermal
1037 Old Salem Road
Murfreesboro, TN 37129
Тел. 1 800 776-8039
Факс 1 800 890-6926
Электронная почта: AmGeo@bellsouth. net
net
Джо Парсонс
ECR Technologies
1248 George Jenkins Blvd.
Building B3
Lakeland, FL 33801
Тел. 941 688-0880
Факс 941 688-0929
Передовые геотермальные технологии
P.O. Box 6469
Reading, PA 19610
Тел. 610 736-0570
Факс 610 736-0571
K. W. Lambert Construction and Equipment
405 Mt. Crawford Ave.
Bridgewater, VA 22812
Тел. 540 828-3147
Факс 540 828-7474
Последовательность химических реакций
Превращение меди: Последовательность химических реакцийЦели
- Проиллюстрируйте множество веществ, в состав которых может входить тот или иной элемент:
металл -> синий раствор -> синее твердое вещество -> черное твердое вещество -> синий раствор (снова) -> металл (снова).
- Сохранение массы и родинок:
- Мы должны извлечь столько же меди, сколько мы начали.

- Одинаковое количество меди на каждой стадии: одинаковое количество молей.
- Мы должны извлечь столько же меди, сколько мы начали.
- Опыт применения стандартных химических методов: фильтрации и количественного переноса.
Реакция
Cu (s) -> [Cu (H 2 O) 6 ] 2+ (водн.) -> Cu (OH) 2 (s) -> CuO (s) -> [Cu (H 2 O) 6 ] 2+ (водн.) -> Cu (s)- Металлическая медь «растворяется» в азотной кислоте (HNO 3 ).Фактически, нитрат-ион окисляет металлическую медь до иона меди (II), при этом сам превращаясь в газ NO 2 ; затем ион меди (II) связывается с шестью молекулами воды. Физическое изменение, которое вы должны наблюдать, — это исчезновение окрашенного в медь металла, когда раствор становится синим (из [Cu (H 2 O) 6 ] 2+ , ион гексааквакоппера) и коричневого газа (NO 2). ) развивается.
Cu (s) + 4 H 3 O + (водн.
 ) + 2 NO 3 — (водн.) -> [Cu (H 2 O) 6 ] 2+ (водн.) + 2 NO 2 (г)
) + 2 NO 3 — (водн.) -> [Cu (H 2 O) 6 ] 2+ (водн.) + 2 NO 2 (г) - Ион гидроксида (OH — ) связывается с ионом меди (II) даже сильнее, чем вода.В результате ион гидроксида может вытеснять воду из иона меди (II), давая гидроксид меди Cu (OH) 2 , синий осадок.
[Cu (H 2 O) 6 ] 2+ (водн.) + 2 OH — -> Cu (OH) 2 (s) + 6 H 2 O (l)
- При нагревании гидроксида меди образуется оксид меди CuO, твердое вещество черного цвета.
Cu (OH) 2 (s) -> CuO (s) + H 2 O (l)
- Оксид меди растворяется в кислоте, регенерируя ион меди (II), который снова связывается с вода.
CuO (т.) + 2 H 3 O + (водн.) + 3 H 2 O (l) -> [Cu (H 2 O) 6 ] 2+ (водн.
 )
) - Наконец, металлический цинк восстанавливает гидратированный ион меди (II) обратно до металлической меди, а сам превращается в ионы цинка (II), окисляясь. Мы уже видели эту реакцию в лаборатории хлорида меди).
[Cu (H 2 O) 6 ] 2+ (водн.) + Zn (s) -> Cu (s) + Zn 2+ (водн.) + 6 H 2 O ( водн.)
В то же время часть металлического цинка, который присутствует в избытке, восстанавливает ионы гидроксония до H 2 .Zn (т) + 2 H 3 O + (водн.) -> Zn 2+ (водн.) + H 2 (г) + 2 H 2 O (л)
Процедура
Я не буду вдаваться в подробности процедуры, но подчеркну некоторые моменты безопасности и (выделено жирным шрифтом ) некоторые места, где наша процедура отличается от процедуры в лабораторном пакете.- Преобразование Cu (s) в [Cu (H 2 O) 6 ] 2+ (водн.
 )
)- Возьмите кусок медной проволоки и взвесьте его с точностью до 0.01 г . Кусочки проволоки ближе к 0,50 г, чем 0,35 г. Ничего страшного: используйте то, что мы предлагаем.
- Используйте примерно 4-5 мл концентрированного раствора HNO 3 .
- Будьте осторожны с азотной кислотой: как и другие сильные кислоты, при попадании на кожу она вызывает жжение и может повредить одежду; в отличие от большинства других кислот, он также окрашивает пораженный участок в желтый цвет.
- Если некоторое количество меди остается нерастворенной к моменту завершения производства газа, поставьте стакан на горячие плиты в вытяжных шкафах, чтобы ускорить реакцию.
- Важно выполнять этот шаг в вытяжном шкафу, потому что коричневый газ NO 2 является раздражителем. Держите смеси в вытяжке до тех пор, пока вы не добавите 10 мл дистиллированной воды после полного растворения меди.
- Преобразование [Cu (H 2 O) 6 ] 2+ (водн.
 ) В Cu (OH) 2 (s)
) В Cu (OH) 2 (s)- Будьте осторожны при обращении с NaOH, так как это сильное основание, которое при контакте с кожей будет жалить. К раствору меди по каплям добавляют раствор NaOH.
- После образования синего осадка периодически проверяйте кислотность раствора, погружая палочку для перемешивания в раствор и касаясь ею красной лакмусовой бумаги. Старайтесь не переносить синий осадок на лакмусовую бумагу: это приведет к некоторой потере меди и, возможно, ложному синему цвету на лакмусовой бумаге. Вначале раствор становится кислым из-за избытка азотной кислоты на предыдущем этапе, поэтому первый добавленный ОН- идет на нейтрализацию кислоты; как только кислота нейтрализована, следующий добавленный OH — идет на образование синего осадка Cu (OH) 2 .Только после этого добавленный OH — зависает в режиме ожидания, и только в это время он станет красной лакмусовой бумажкой и станет синей. Мы хотим убедиться, что вся присутствующая медь превратилась в Cu (OH) 2 , поэтому мы добавляем OH — , пока раствор не станет синей лакмусовой бумажкой.

- Преобразование Cu (OH) 2 (s) в CuO (s)
- Добавить воду к реакционной смеси, полученной на предыдущем этапе, и добавить еще один или два кипящих камня .
- Нагрейте содержимое стакана, но не кипятите . При кипячении черный CuO становится настолько мелким, что этап фильтрации становится чрезмерно длинным. Нагрейте стакан до тех пор, пока весь синий Cu (OH) 2 не исчезнет и не заменится черным CuO.
- Отфильтруйте и промойте CuO, как описано в процедуре (часть C). Оставьте твердое вещество на фильтровальной бумаге и выбросьте фильтрат.
- Превратить CuO (s) обратно в [Cu (H 2 O) 6 ] 2+ (водн.)
- Растворите CuO на фильтровальной бумаге, как описано в процедуре (часть D).
- Раствор серной кислоты вызывает коррозию и вызывает раздражение кожи, с которой соприкасается.
- Преобразование [Cu (H 2 O) 6 ] 2+ (водн.
 ) Обратно в Cu (s)
) Обратно в Cu (s)- Добавьте примерно 1 г Zn к синему раствору, полученному на предыдущем этапе, и после того, как раствор потеряет весь свой синий цвет, вам может потребоваться добавить немного серной кислоты для реакции любого избытка Zn.
- Промойте металлическую медь три раза дистиллированной водой и перенесите ее в чашу для выпаривания, как описано в процедуре (часть E), а затем трижды промойте ее изопропанолом порциями по 5 мл.Промывка изопропанолом сокращает время, необходимое для стадии сушки.
- Высушите медь в стакане с кипящей водой, как описано в процедуре (E). Взвесьте сухую медь и запишите массу. Вычислите процент извлеченной меди.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки вашего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом.Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.
Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.

Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.Например, сайт
не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к
остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Свойства и применение меди — электрическая, термическая, коррозионная стойкость, легирование и др.
Слово медь происходит от латинского слова «купрум», что означает «руда Кипра». Вот почему химический символ меди — Cu.Медь обладает множеством чрезвычайно полезных свойств, в том числе:
- хорошая электропроводность
- хорошая теплопроводность
- коррозионная стойкость
Это также:
- легко легируется
- гигиенический
- легко присоединился к
- пластичный
- жесткий
- немагнитный
- привлекательный
- перерабатываемый
- каталитический
См. Ниже дополнительную информацию о каждом из этих свойств и о том, какую пользу они приносят нам в повседневной жизни.
Хорошая электропроводность
Медь имеет лучшую электропроводность из всех металлов, кроме серебра.
Хорошая электропроводность — это то же самое, что и небольшое электрическое сопротивление. Электрический ток будет протекать через все металлы, однако они все еще имеют некоторое сопротивление, а это означает, что ток должен проталкиваться (батареей), чтобы продолжать течь. Чем больше сопротивление, тем сильнее мы должны толкать (и тем меньше ток). Ток легко протекает через медь благодаря ее небольшому электрическому сопротивлению без больших потерь энергии.Вот почему медные провода используются в сетевых кабелях в домах и под землей (хотя воздушные кабели, как правило, из алюминия, потому что они менее плотные). Однако там, где важен размер, а не вес, лучшим выбором будет медь. Толстая медная полоса используется для молниеотвода на высоких зданиях, таких как церковные шпили. Медная полоса должна быть толстой, чтобы пропускать большой ток без плавления.
Электрический ток будет протекать через все металлы, однако они все еще имеют некоторое сопротивление, а это означает, что ток должен проталкиваться (батареей), чтобы продолжать течь. Чем больше сопротивление, тем сильнее мы должны толкать (и тем меньше ток). Ток легко протекает через медь благодаря ее небольшому электрическому сопротивлению без больших потерь энергии.Вот почему медные провода используются в сетевых кабелях в домах и под землей (хотя воздушные кабели, как правило, из алюминия, потому что они менее плотные). Однако там, где важен размер, а не вес, лучшим выбором будет медь. Толстая медная полоса используется для молниеотвода на высоких зданиях, таких как церковные шпили. Медная полоса должна быть толстой, чтобы пропускать большой ток без плавления.
Медный провод можно намотать в катушку. Катушка будет создавать магнитное поле и, поскольку она сделана из меди, не расходует много электроэнергии.Медные катушки можно найти в:
.| Устройство | Использовать |
| Электромагниты | Замки, краны для свалок, звонки электрические. (См. Электромагниты.) (См. Электромагниты.) |
| Двигатели | Насосы, бытовая техника (стиральные машины, посудомоечные машины, холодильники, пылесосы), автомобили (стартеры, дворники, электрические стеклоподъемники), компьютеры (дисководы, вентиляторы), развлекательные системы (DVD-плееры). (См. Электродвигатели.) |
| Динамо | Велосипеды, электростанции |
| Трансформаторы | Сетевые адаптеры, подстанции, электростанции. (См. Медь и электричество: трансформаторы и сеть.) |
Как медь проводит
Медь — это металл, состоящий из плотно упакованных атомов меди.
Если бы мы могли присмотреться, мы бы увидели, что между атомами меди движутся электроны.
Каждый атом меди потерял один электрон и стал положительным ионом. Итак, медь представляет собой решетку положительных ионов меди со свободными электронами, движущимися между ними. (Электроны немного похожи на частицы газа, которые могут свободно перемещаться по поверхности провода).
Электроны могут свободно перемещаться по металлу. По этой причине они известны как свободные электроны. Они также известны как электроны проводимости, потому что они помогают меди быть хорошим проводником тепла и электричества.
Ионы меди колеблются (см. Рисунок 1). Обратите внимание, что они колеблются примерно в одном и том же месте, тогда как электроны могут двигаться через решетку. Это очень важно, когда мы подключаем провод к батарее.
Рисунок 1 — Медный провод состоит из решетки ионов меди. Есть свободные электроны, которые движутся через эту решетку, как газ.
Проводка электричестваМы можем подключить медный провод к батарее и переключателю.Обычно свободные электроны беспорядочно перемещаются в металле. Когда мы замыкаем выключатель, течет электрический ток. Теперь свободные электроны проходят через проволоку (рис. 2), они движутся слева направо (и по-прежнему движутся беспорядочно).
Рис. 2 — Работа переключателя в приведенной выше схеме заставляет электроны течь слева направо в направлении, противоположном току.
2 — Работа переключателя в приведенной выше схеме заставляет электроны течь слева направо в направлении, противоположном току.
Электроны имеют отрицательный заряд. Они притягиваются к положительному полюсу аккумулятора.Свободные электроны движутся через медь, протекая от отрицательного к положительному полюсу батареи (обратите внимание, что они текут в направлении, противоположном обычному току; это потому, что они имеют отрицательный заряд).
Ионы меди в проволоке колеблются. Иногда ион преграждает путь движущемуся электрону. Электрон сталкивается с ионом и отскакивает от него. Это замедляет электрон. Часть его энергии была передана иону, который колеблется быстрее.
Таким образом, энергия передается от движущихся электронов к ионам меди.Медь нагревается. Это объясняет, почему:
- Металлы обладают электрическим сопротивлением.
- металла нагреваются при протекании через них тока.
Хорошая теплопроводность
Медь — хороший проводник тепла. Это означает, что если вы нагреете один конец куска меди, другой конец быстро достигнет той же температуры. Большинство металлов — довольно хорошие проводники; Однако, кроме серебра, лучше всего медь.
Это означает, что если вы нагреете один конец куска меди, другой конец быстро достигнет той же температуры. Большинство металлов — довольно хорошие проводники; Однако, кроме серебра, лучше всего медь.
| Металл | Относительная проводимость |
| Медь | 394 |
| Серебристый | 418 |
| Алюминий | 238 |
| Нержавеющая сталь | 13 |
Теплопроводность обычных металлов.Когда вы нагреете одну сторону материала, другая сторона нагреется. Приведенные выше значения являются мерой того, насколько быстро другая сторона становится такой же горячей, как и нагретая.
Он используется во многих системах отопления, поскольку не подвержен коррозии и имеет высокую температуру плавления. Единственный другой материал, обладающий такой же устойчивостью к коррозии, — это нержавеющая сталь. Однако его теплопроводность в 30 раз хуже, чем у меди.
Применения
Медь позволяет теплу быстро проходить через нее.Поэтому он используется во многих приложениях, где важна быстрая теплопередача. К ним относятся:
| Устройство | Использовать |
| Медная пластина | Дно кастрюль. |
| Медные трубы | Теплообменники в резервуарах для горячей воды, системах подогрева полов, всепогодных футбольных полях и автомобильных радиаторах. |
| Радиаторы | Компьютеры, дисководы, телевизоры. |
Проводя тепло
Медь состоит из решетки ионов со свободным электроном (см. Рисунок 1).Ионы колеблются, а электроны могут двигаться через медь (как газ).
На рисунке 3 показано, что происходит, когда один конец куска меди становится более горячим. Ионы меди на горячем конце вибрируют сильнее. Примечание: электроны исключены из изображения, чтобы оно было четким.
Рисунок 3 — Левый конец куска меди более горячий. Ионы меди на горячем конце вибрируют сильнее. (Примечание: электроны были исключены из изображения, чтобы оно было четким.)
Рисунок 4 сфокусирован всего на нескольких электронах, чтобы увидеть, как они проводят тепло слева направо.
- Свободный электрон сталкивается с ионом на горячем конце и получает кинетическую энергию (ускоряется).
- Перемещается к холодному концу.
- Он сталкивается с «холодным ионом», заставляя ранее холодный ион вибрировать сильнее. Это нагревает холодный конец.
- Таким образом, энергия передается через медь от горячей к холодной.
Рис. 4. Как электроны проводят тепло слева направо (показаны лишь некоторые из них, чтобы их было легче увидеть).
Неметаллы, проводящие тепло
Сравните это с тем, как тепло проводится в неметалле. Колеблющиеся частицы передают свои колебания ближайшим соседям. Это намного медленнее. Вот почему металлы являются лучшими проводниками — их свободные электроны могут переносить энергию по своей длине.
Это намного медленнее. Вот почему металлы являются лучшими проводниками — их свободные электроны могут переносить энергию по своей длине.
Коррозионная стойкость
Медь с низкой реакционной способностью. Это означает, что он не подвержен коррозии. Это важно при использовании для труб, электрических кабелей, кастрюль и радиаторов отопления.
Это также означает, что он хорошо подходит для декоративного использования. Украшения, статуи и части зданий могут быть сделаны из меди, латуни или бронзы и оставаться привлекательными в течение тысяч лет.
Для получения дополнительной информации о преимуществах коррозионной стойкости меди для морских применений см. Ресурс «Медные сплавы в аквакультуре».
Сплавы легко
Медь легко комбинируется с другими металлами для получения сплавов. Первым произведенным сплавом была медь, расплавленная с оловом для образования бронзы — открытие настолько важное, что периоды в истории называют бронзовым веком.
Намного позже появилась латунь (медь и цинк), а в современную эпоху — мельхиор (медь и никель). Сплавы тверже, прочнее и жестче, чем чистая медь. Их можно сделать еще более твердыми, ударив по ним молотком — процесс, называемый «наклеп».
В дереве медных сплавов показаны варианты добавления других металлов для получения различных сплавов. Ниже приведены некоторые примеры. Нажмите на диаграмму выше, чтобы увидеть увеличенную версию.
Медь + олово = оловянная бронза
Медь + олово + фосфор = фосфорная бронза
Медь + алюминий = алюминиевая бронза
Медь + цинк = латунь
Медь + олово + цинк = бронза
Медь + никель = медно-никель
Медь + никель + цинк = нейзильбер.
Для получения дополнительной информации см. Ресурс «Медь в чеканке». Вы также можете просмотреть страницы Ассоциации разработчиков меди, посвященные меди и ее сплавам.
Гигиенический
Медь по своей природе гигиенична, что означает, что она враждебна бактериям, вирусам и грибкам, которые поселяются на ее поверхности. Это свойство видит установку поверхностей из меди и медных сплавов в больницах и других областях, где гигиена является ключевой проблемой.
Это свойство видит установку поверхностей из меди и медных сплавов в больницах и других областях, где гигиена является ключевой проблемой.
Легко присоединяется
Медь легко соединяется пайкой или пайкой.Это полезно для трубопроводов и для изготовления герметичных медных сосудов.
Дуктильный
Медь — пластичный металл. Это означает, что из него легко могут быть сформированы трубы и вытянуты проволоки. Медные трубы легкие, потому что у них могут быть тонкие стенки. Они не подвержены коррозии, и их можно согнуть, чтобы подогнать под углы. Трубы можно соединить пайкой, и они безопасны при пожаре, поскольку не горят и не поддерживают горение.
Жесткий
Медь и медные сплавы прочные.Это означает, что они хорошо подходили для изготовления инструментов и оружия. Представьте себе радость древнего человека, когда он обнаружил, что его аккуратно сформированные наконечники стрел больше не разбиваются при ударе.
Свойство вязкости жизненно важно для меди и медных сплавов в современном мире. Они не разбиваются при падении и не становятся хрупкими при охлаждении ниже 0 ° C.
Они не разбиваются при падении и не становятся хрупкими при охлаждении ниже 0 ° C.
Немагнитный
Медь немагнитна и не искрит. Из-за этого он используется в специальных инструментах и военном оборудовании.
Привлекательный цвет
Медь и ее сплавы, такие как латунь, используются для изготовления ювелирных изделий и украшений. Они имеют привлекательный золотистый цвет, который зависит от содержания меди. Они обладают хорошей устойчивостью к потускнению, что делает их долговечными.
Вторичная переработка
Медь может быть переработана без потери качества. Около 40% потребностей Европы удовлетворяется за счет вторичной меди.
Для получения дополнительной информации см. Ресурс «Вторичная переработка меди и устойчивое развитие».
Каталитический
Медь может действовать как катализатор, то есть вещество, которое может ускорить химическую реакцию и повысить ее эффективность. Это достигается за счет снижения энергии активации. Катализаторы биологических реакций называются ферментами.
Катализаторы биологических реакций называются ферментами.
Медь ускоряет реакцию между цинком и разбавленной серной кислотой. Он содержится в некоторых ферментах, один из которых участвует в дыхании. Это действительно жизненно важный элемент!
Быстрый нагрев вызвал сверхвысокую стабильность нанозернистой меди
Реферат
Тепловая и механическая нестабильность, присущая нанозернистым материалам, является узким местом их обработки и технологических применений.В дополнение к традиционной стратегии стабилизации, которая основана на легировании, недавно было обнаружено, что релаксация границ зерен эффективна для стабилизации чистых металлов с нанозернистыми частицами. Релаксация границ зерен может быть вызвана деформацией очень мелких нанозерен ниже критического размера, обычно нескольких десятков нанометров. Здесь мы обнаружили, что быстрый нагрев может вызвать интенсивную граничную релаксацию нанозерен чистой Cu с размерами до субмикрометров, масштабом длины с заметной нестабильностью в металлах. Быстро нагретые нанозерна Cu остаются стабильными при температурах до 0,6 T m (точка плавления), даже выше, чем температура рекристаллизации деформированной крупнозернистой меди. Термически индуцированная релаксация границ зерен, возникающая в результате генерации нанодвойников высокой плотности, предлагает альтернативный подход к стабилизации наноструктурированных материалов.
Быстро нагретые нанозерна Cu остаются стабильными при температурах до 0,6 T m (точка плавления), даже выше, чем температура рекристаллизации деформированной крупнозернистой меди. Термически индуцированная релаксация границ зерен, возникающая в результате генерации нанодвойников высокой плотности, предлагает альтернативный подход к стабилизации наноструктурированных материалов.
ВВЕДЕНИЕ
Металлы затвердевают после пластической деформации, но становятся нестабильными при повышенных температурах, так как деформационные дефекты, такие как дислокации и границы зерен (ГЗ), устраняются за счет восстановления и рекристаллизации.В металлах с нормальной чистотой (~ 100 частей на миллион примесей) рекристаллизация обычно начинается примерно при 0,4 T m (температура плавления) ( 1 , 2 ). Температура рекристаллизации падает с увеличением деформации (плотности дефектов) ( 3 ). Сильно деформированные металлы с чрезвычайно высокой плотностью ГБ и дислокаций, т. е. нанозернистые или субмикрозернистые материалы, могут стать нестабильными даже при температуре окружающей среды ( 1 , 4 ).
е. нанозернистые или субмикрозернистые материалы, могут стать нестабильными даже при температуре окружающей среды ( 1 , 4 ).
Стабилизация деформируемых металлов имеет решающее значение для их технологических применений, особенно для наноструктурированных металлов с индивидуальными свойствами. Легирование традиционно используется для замедления кинетики рекристаллизации, поскольку растворенные атомы могут подавлять подвижность ГБ ( 5 — 7 ). Использование низкоэнергетических границ, таких как двойниковые границы и малоугловые ГЗ, которые менее склонны к рекристаллизации ( 8 — 10 ), является альтернативной стратегией стабилизации без изменения химического состава материала.Наше недавнее исследование показало, что нанозернистые металлы со случайными ГБ могут быть стабилизированы посредством релаксации ГБ ( 11 — 13 ). Как термическая, так и механическая стабильность очень мелких нанозерен в ряде металлов с гранецентрированной кубической (ГЦК) структурой значительно улучшены, что происходит из-за вызванной деформацией автономной релаксации ГЗ к более низким энергетическим состояниям через эмиссию дефектов упаковки или двойников с границ. Тем не менее, этот эффект ограничивается нанозернами ниже критического размера, обычно нескольких десятков нанометров.Стабилизация более крупных зерен в чистых металлах действительно является сложной задачей, например, с субмикронными зернами, которые обычно получают с помощью методов пластической деформации.
Тем не менее, этот эффект ограничивается нанозернами ниже критического размера, обычно нескольких десятков нанометров.Стабилизация более крупных зерен в чистых металлах действительно является сложной задачей, например, с субмикронными зернами, которые обычно получают с помощью методов пластической деформации.
В принципе, релаксация ГЗ может быть альтернативно инициирована термической активацией, поскольку двойники могут образовываться посредством термического отжига. Например, в металлах с низкой энергией дефекта упаковки, таких как Cu, аустенитные нержавеющие стали и некоторые суперсплавы на основе Ni, двойники часто появляются при рекристаллизации деформированных структур при отжиге при повышенных температурах ( 14 — 16 ).Двойники отжига используются в так называемой инженерии GB для улучшения коррозионной стойкости и других свойств материалов, в которых множество границ Σ3 или Σ3 n итеративно генерируются деформацией и последующим отжигом ( 17 , 18 ). Литература показала, что в Cu с чистотой от 99,9 до 99,99% и деформационной деформацией ниже 100% двойники отжига обычно образуются при отжиге при температуре от 473 до 523 К ( 19 , 20 ).К сожалению, это температурное окно намного выше, чем для укрупнения нанозерен в Cu, обычно от 393 до 450 К для размеров зерен от 50 до 200 нм ( 11 ). Другими словами, когда нанозерна нагреваются, укрупнение нанозерна из-за миграции ГЗ происходит до образования двойников отжига.
Литература показала, что в Cu с чистотой от 99,9 до 99,99% и деформационной деформацией ниже 100% двойники отжига обычно образуются при отжиге при температуре от 473 до 523 К ( 19 , 20 ).К сожалению, это температурное окно намного выше, чем для укрупнения нанозерен в Cu, обычно от 393 до 450 К для размеров зерен от 50 до 200 нм ( 11 ). Другими словами, когда нанозерна нагреваются, укрупнение нанозерна из-за миграции ГЗ происходит до образования двойников отжига.
ГБ Миграция — это процесс термической активации, зависящий от скорости нагрева. Более высокие скорости нагрева могут сдвинуть процесс на более высокие температуры. Как продемонстрировано в образцах субмикрозернистого никеля, полученных в результате пластической деформации, температура укрупнения зерна повышается от 420 до 500 К при увеличении скорости нагрева от 0.От 3 до 10 К / мин ( 21 ). В терминах уравнения Киссинджера для термически активированного процесса, такого как укрупнение зерна, начальная температура ( T x ) связана со скоростью нагрева ( HT ) соотношением ln (HTTx2) = — ERTx + constant, где E — кажущаяся энергия активации [72,5 кДж / моль для Cu ( 22 )], а R — газовая постоянная. Взяв T x = 393 K для зерен 80 нм ( 11 ) при скорости нагрева 1 K / мин, мы получили T x = 473 K при скорости 62 K / min, температура образования двойников отжига в Cu ( 19 , 20 ).Поскольку образование двойников отжига не показывает явной зависимости от скорости нагрева ( 23 ), ожидается, что нанозерна будут нагреваться достаточно быстро (выше критической скорости), так что начальная температура миграции ГЗ превысит температуру образования двойников, и двойникование может занять место в нанозернах перед укрупнением зерна. Следовательно, разумно предположить, что образование двойников отжига может запускать краевую релаксацию нанозерен, как в случае механически индуцированной релаксации ГЗ. В настоящем исследовании это будет использовано в нанозернистой чистой меди.
Взяв T x = 393 K для зерен 80 нм ( 11 ) при скорости нагрева 1 K / мин, мы получили T x = 473 K при скорости 62 K / min, температура образования двойников отжига в Cu ( 19 , 20 ).Поскольку образование двойников отжига не показывает явной зависимости от скорости нагрева ( 23 ), ожидается, что нанозерна будут нагреваться достаточно быстро (выше критической скорости), так что начальная температура миграции ГЗ превысит температуру образования двойников, и двойникование может занять место в нанозернах перед укрупнением зерна. Следовательно, разумно предположить, что образование двойников отжига может запускать краевую релаксацию нанозерен, как в случае механически индуцированной релаксации ГЗ. В настоящем исследовании это будет использовано в нанозернистой чистой меди.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Мы приготовили градиентный нанозернистый поверхностный слой на крупнозернистом образце бескислородного бруска меди с чистотой 99,97%, используя поверхностную механическую шлифовку (SMGT) в жидком азоте (таблица S1). В самом верхнем поверхностном слое обнаружены случайно ориентированные зерна со средним поперечным размером ~ 40 нм и соотношением сторон 1,7. Поперечные размеры зерен постепенно увеличивались с увеличением глубины до примерно 60 нм на глубине 18 мкм и до 200 нм на глубине 150 мкм.Обнаружена слабая текстура {111} 〈110〉 в нанозернистом слое. Деформированные крупнозернистые структуры можно обнаружить под наноструктурированным поверхностным слоем. Затем полученные образцы с градиентным нанозернистым слоем нагревали с разными скоростями до заданной температуры 523 К [температура образования двойников отжига в крупнозернистой меди ( 19 , 20 )] и сразу охлаждали до температуры окружающей среды. Четыре скорости нагрева (1, 80, 160 и 240 К / мин соответственно), точно контролируемые на оборудовании для дифференциальной сканирующей калориметрии, были использованы для определения влияния скорости на кинетику укрупнения нанозерен.
В самом верхнем поверхностном слое обнаружены случайно ориентированные зерна со средним поперечным размером ~ 40 нм и соотношением сторон 1,7. Поперечные размеры зерен постепенно увеличивались с увеличением глубины до примерно 60 нм на глубине 18 мкм и до 200 нм на глубине 150 мкм.Обнаружена слабая текстура {111} 〈110〉 в нанозернистом слое. Деформированные крупнозернистые структуры можно обнаружить под наноструктурированным поверхностным слоем. Затем полученные образцы с градиентным нанозернистым слоем нагревали с разными скоростями до заданной температуры 523 К [температура образования двойников отжига в крупнозернистой меди ( 19 , 20 )] и сразу охлаждали до температуры окружающей среды. Четыре скорости нагрева (1, 80, 160 и 240 К / мин соответственно), точно контролируемые на оборудовании для дифференциальной сканирующей калориметрии, были использованы для определения влияния скорости на кинетику укрупнения нанозерен.
При нагревании образца со скоростью 1 К / мин укрупнение нанозерна с образованием зерен микрометрового размера начинается в приповерхностном слое глубже 18 ± 4 мкм, в котором исходные зерна крупнее 60 нм. Напротив, верхний слой толщиной 18 мкм, содержащий нанозерна со средним размером от 40 до 60 нм, остается стабильным после отжига (рис. 1А), что подтверждается наблюдениями просвечивающей электронной микроскопии (ПЭМ). В этом слое обнаружено несколько единичных аномально укрупненных зерен.Стабилизированный нанозернистый поверхностный слой, который согласуется с нашим предыдущим исследованием, был приписан механически индуцированной релаксации ГЗ в этом слое во время процесса SMGT ( 11 ). Температура нестабильности зерен 60 нм после механической релаксации ГЗ составляет около 523 К ( 11 ), что совпадает с нашими наблюдениями.
Напротив, верхний слой толщиной 18 мкм, содержащий нанозерна со средним размером от 40 до 60 нм, остается стабильным после отжига (рис. 1А), что подтверждается наблюдениями просвечивающей электронной микроскопии (ПЭМ). В этом слое обнаружено несколько единичных аномально укрупненных зерен.Стабилизированный нанозернистый поверхностный слой, который согласуется с нашим предыдущим исследованием, был приписан механически индуцированной релаксации ГЗ в этом слое во время процесса SMGT ( 11 ). Температура нестабильности зерен 60 нм после механической релаксации ГЗ составляет около 523 К ( 11 ), что совпадает с нашими наблюдениями.
( A ) Типичные СЭМ-изображения поперечного сечения градиентного нанозернистого поверхностного слоя в свежеприготовленном образце Cu, нагретом до 523 К с разной скоростью (1, 80 и 160 К / мин, соответственно).( B — D ) Типичные светлопольные изображения ПЭМ наноструктур на глубине ~ 25 мкм от поверхности [как указано в (A), со средним размером зерна около 80 нм в свежеприготовленном образце. ] в исходном и нагретом образцах с разной скоростью нагрева. На вставках показаны соответствующие электронограммы выбранной области. ( E ) Соответствующий диапазон размеров зерен в исходном состоянии в стабилизированном поверхностном слое градиентных нанозернистых образцов после нагрева до 523 К с различными скоростями.Сплошные и полые кружки представляют собой верхний и нижний пределы наблюдаемых стабильных размеров зерен соответственно. Пунктирная линия представляет средний размер зерна в исходном образце ( D * ~ 60 нм) после отжига при 523 К из ( 10 ). Планки погрешностей — стандартные ошибки среднего размера зерна.
] в исходном и нагретом образцах с разной скоростью нагрева. На вставках показаны соответствующие электронограммы выбранной области. ( E ) Соответствующий диапазон размеров зерен в исходном состоянии в стабилизированном поверхностном слое градиентных нанозернистых образцов после нагрева до 523 К с различными скоростями.Сплошные и полые кружки представляют собой верхний и нижний пределы наблюдаемых стабильных размеров зерен соответственно. Пунктирная линия представляет средний размер зерна в исходном образце ( D * ~ 60 нм) после отжига при 523 К из ( 10 ). Планки погрешностей — стандартные ошибки среднего размера зерна.
При нагревании со скоростью 80 К / мин (выше расчетной критической скорости нагрева) верхний поверхностный слой со стабильными нанозернами утолщается примерно до 28 ± 9 мкм, что соответствует исходному размеру зерна от 40 до 100 нм.Укрупнение зерна происходит в приповерхностном слое с исходными зернами более 100 нм. Размеры зерен в укрупненном слое намного меньше, чем при 1 К / мин, из-за меньшего времени укрупнения зерен.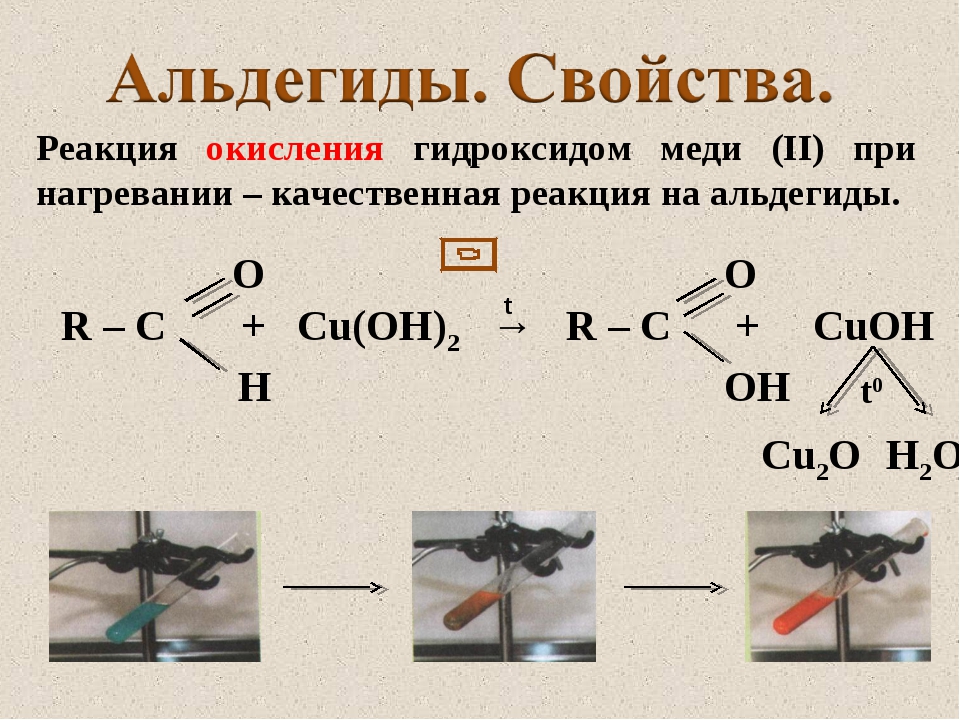 Очевидно, нанозерна размером от 60 до 100 нм, которые нестабильно нагреваются при 1 К / мин, стабилизируются при 80 К / мин. Когда скорость нагрева увеличивается до 160 К / мин, стабилизированный нанозернистый слой значительно утолщается, охватывая диапазон размеров зерен от 40 до 160 нм, а размеры зерен в укрупняющем слое становятся еще меньше.При дальнейшем увеличении до 240 К / мин толщина стабилизированного поверхностного слоя кажется насыщенной, как на рис. 1Е.
Очевидно, нанозерна размером от 60 до 100 нм, которые нестабильно нагреваются при 1 К / мин, стабилизируются при 80 К / мин. Когда скорость нагрева увеличивается до 160 К / мин, стабилизированный нанозернистый слой значительно утолщается, охватывая диапазон размеров зерен от 40 до 160 нм, а размеры зерен в укрупняющем слое становятся еще меньше.При дальнейшем увеличении до 240 К / мин толщина стабилизированного поверхностного слоя кажется насыщенной, как на рис. 1Е.
Стабилизированные нанозерна в поверхностном слое систематически характеризовались методом просвечивающей электронной микроскопии. На глубине около 25 мкм, соответствующей зернам 80 нм в свежеприготовленном образце, не было обнаружено явной разницы в распределении размеров зерен и среднем размере, а также на картине дифракции электронов после быстрого нагрева (при 160 K / мин; рис. 1, A, B, и D, и 3A).Напротив, микрозерна с резкими границами образуются на той же глубине при 1 К / мин (рис. 1С). Измеренная нанотвердость на этой глубине составила 2,35 ± 0,10 ГПа в исходном образце. После быстрого нагрева она немного увеличивается и составляет около 2,20 ± 0,12 ГПа. Эти данные подтвердили отсутствие укрупнения нанозерен размером от 40 до 155 нм в верхнем поверхностном слое после быстрого нагрева до 523 К. Такой диапазон размеров намного шире, чем в исходном образце после механической релаксации ГЗ (от 40 до 60 мкм). нм).Другими словами, область сверхстабилизированного размера зерна от 60 до 160 нм (красная область на рис. 1E) является результатом быстрого нагрева.
После быстрого нагрева она немного увеличивается и составляет около 2,20 ± 0,12 ГПа. Эти данные подтвердили отсутствие укрупнения нанозерен размером от 40 до 155 нм в верхнем поверхностном слое после быстрого нагрева до 523 К. Такой диапазон размеров намного шире, чем в исходном образце после механической релаксации ГЗ (от 40 до 60 мкм). нм).Другими словами, область сверхстабилизированного размера зерна от 60 до 160 нм (красная область на рис. 1E) является результатом быстрого нагрева.
Сравнивая изображения ПЭМ на рис. 1 (B и D), мы обнаружили двойники во многих нанозернах (обведены кружком) в быстро нагретом образце. При наклоне образца почти в каждом нанозерне появляются двойники, которые, кажется, исходят из ГЗ и заканчиваются на противоположных границах. Изображения ПЭМ высокого разрешения (рис. 2А) выявили многочисленные двойники сквозных зерен в нанозернах с расстоянием от нескольких до десятков нанометров.Морфология аналогична нанозернам после механической релаксации ГЗ ( 11 , 12 ). Плотность двойников в нанозернах на порядки выше, чем в деформированных крупных зернах после рекристаллизации. Хотя двойники существуют в некоторых очень мелких нанозернах в свежеприготовленном образце (рис. 1B), карты распределения характера GB, измеренные с помощью ПЭМ, показали, что плотность двойников значительно увеличивается после быстрого нагрева (рис. 2, B и C). Статистические результаты показали, что доля границ Σ3 увеличивается с 7.От 8% в свежеприготовленном образце до примерно 16,2% после быстрого нагревания (таблица S2).
Плотность двойников в нанозернах на порядки выше, чем в деформированных крупных зернах после рекристаллизации. Хотя двойники существуют в некоторых очень мелких нанозернах в свежеприготовленном образце (рис. 1B), карты распределения характера GB, измеренные с помощью ПЭМ, показали, что плотность двойников значительно увеличивается после быстрого нагрева (рис. 2, B и C). Статистические результаты показали, что доля границ Σ3 увеличивается с 7.От 8% в свежеприготовленном образце до примерно 16,2% после быстрого нагревания (таблица S2).
( A ) ПЭМ-изображение с высоким разрешением типичного нанозерна на рис. 1D с атомным изображением нанодвойников в нанозерне (вставка). ( B и C ) Типичные карты распределения характеристик GB для свежеприготовленных (B) и быстро нагретых [(C) со скоростью 160 К / мин] образцов.Цветные линии обозначают различные границы, включая двойниковые границы (красные), малоугловые границы (серые), обычные многоугольные границы (черные) и другие специальные границы (Σ <29, другие цвета). ( D и E ) ПЭМ-изображения с высоким разрешением типичных границ между нанозернами на рис. 1D; вставки — увеличенные изображения областей, выделенных красным.
( D и E ) ПЭМ-изображения с высоким разрешением типичных границ между нанозернами на рис. 1D; вставки — увеличенные изображения областей, выделенных красным.
Верхний поверхностный слой также был проанализирован с помощью микролучевой дифракции рентгеновских лучей для оценки вероятности двойников (β) на основе асимметрии дифракционного пика, статистической меры плотности двойников (см. Материалы и методы).Из полученных профилей дифракционных пиков для различных плоскостей ( hkl ) было вычислено значение β для быстро нагретого образца, равное примерно 1,37%, что означает один двойник в каждых 73 (111) плоскостях, что примерно соответствует наблюдениям ПЭМ. Значение β (0,15%) на порядок ниже в исходном образце. Хотя эта оценка включает относительно большие ошибки, гораздо более высокое значение β подтвердило очевидное увеличение плотности двойников после быстрого нагрева.
Приведенные выше свидетельства указывают на то, что при быстром нагреве зерна размером 80 нм не обнаруживают явного укрупнения.Вместо этого внутри нанозерна образуются двойники с высокой плотностью. Такое поведение резко отличается от явного укрупнения без двойникования в нанозернах того же размера, нагретых с низкой скоростью (рис. 1С). Это подтверждает наше предсказание о том, что процесс укрупнения нанозерен откладывается из-за быстрого нагрева до более высоких температур, так что двойники отжига образуются заранее. Обычно считается, что двойники отжига образуются во время миграции ГБ в процессе рекристаллизации в деформированной крупнозернистой меди, чтобы уменьшить общую избыточную энергию ГБ ( 24 , 25 ).Очевидно, что в данном случае двойникование происходит без укрупнения зерен или рекристаллизации в нанозернах при быстром нагреве. Двойникование, отделенное от процесса миграции ГБ, похоже, соответствует модели «выскакивающего» дефекта упаковки для переориентации ГБ, чтобы облегчить поглощение дислокаций ( 26 ).
Предыдущие экспериментальные исследования и моделирование некоторых ГЦК-металлов показали, что образование двойников или дефектов упаковки из ГЗ, оба из которых вызывают эмиссию частичных дислокаций, могут вызвать диссоциацию ГЗ ( 27 , 28 ).Он обеспечивает общий подход к релаксации ГЗ для понижения энергетического состояния, особенно в тех металлах с низкой энергией дефекта упаковки, как Cu. Увеличивая границы нанозерен быстро отожженных образцов с помощью ПЭМ высокого разрешения, мы наблюдали, что многие ГЗ связаны с двойниками, которые становятся ограненными, образуя ступеньки из плоскостей (111) длиной в несколько нанометров. Как показано на изображениях с высоким разрешением на рис. 2 (D и E), ступени соединены другими плоскостями (111), образуя зигзагообразные конфигурации.Очевидно, что после быстрого нагрева границы нанозерен имеют тенденцию перестраиваться в состояния с низкой избыточной энергией. Это наблюдение согласуется с предыдущим исследованием, в котором образование двойников нанометрового размера из ГЗ снижает его избыточную энергию в Cu, замедляя диффузию атомов вдоль ГЗ, прилегающих к тройной точке, где они встречаются с границей двойников ( 29 ). Таким образом, можно сделать вывод, что релаксация границ нанозерен в поверхностном слое вызывается нагревом при высоких скоростях нагрева, аналогичным механической активации посредством деформации.
Термическую стабильность нанозерен размером от 50 до 140 нм после термически индуцированной релаксации ГЗ определяли последующим отжигом при различных температурах от 573 до 873 К в течение 15 мин. Для нанозерен со средним размером 80 нм (рис. 3А) не было замечено никаких явных изменений размера зерна ниже 773 К (рис. S1). При 823 К стало очевидным укрупнение зерна. Нанотвердость зерен размером 80 нм после отжига при 773 К незначительно увеличивается до 2,4 ГПа. После отжига при 873 К она падает до 1,20 ГПа, что свидетельствует о явном укрупнении зерна.Из измеренного изменения размера зерна при различных температурах отжига температура начала укрупнения для зерен размером 80 нм была определена как около 810 К, ~ 0,6 T m .
Рис. 3 Сравнение термической стабильности нанозерен до и после быстрого нагрева.( A ) Распределение зерен по размерам из статистических измерений ПЭМ для исходных и быстро нагретых образцов с термически индуцированной релаксацией ГЗ (T-GBR) со средним размером зерна в исходном состоянии ~ 80 нм, отожженных при различных температурах от 673 до 823 К.( B ) Вариации измеренного размера зерна в зависимости от температуры отжига для двух нанозернистых структур со средним размером зерна 80 и 50 нм соответственно. Синие символы и линии представляют образцы, как только они были приготовлены, а красные — образцы T-GBR после быстрого нагревания. Также включены данные измерения нанотвердости образцов 80 нм после отжига при различных температурах. Столбики ошибок показывают SD среднего размера зерна.
Была также исследована термическая стабильность зерен размером 50 нм на глубине около 8 мкм от поверхности после быстрого нагрева.Из-за механической релаксации ГЗ в процессе SMGT температура нестабильности зерен размером 50 нм в исходном состоянии составляет примерно 600 К, что выше, чем у зерен размером 80 нм. Однако после термической релаксации ГЗ их термическая стабильность еще больше повышается. Очевидное укрупнение зерен начинается примерно при 810 К, что очень близко к укрупнению зерен размером 80 нм, как показано на рис. 3В. Аналогичным образом мы измерили начальную температуру укрупнения зерен размером 140 нм (на глубине около 65 мкм от поверхности) после тепловой релаксации ГЗ, которая составляет около 810 К.
Как показано на рис. 4, температура нестабильности нанозерен после термоиндуцированной релаксации ГЗ, по-видимому, не зависит от размера зерна в диапазоне от 50 до 140 нм, в отличие от сильной зависимости температуры нестабильности от размера зерна в образцах после механическая релаксация ГБ. Диапазон размеров зерен, стабилизируемый термической релаксацией ГЗ, намного шире, простираясь до субмикронного масштаба, типичного масштаба длины с заметной нестабильностью в металлах и типичного размера насыщения металлов и сплавов, подвергшихся сильной пластической деформации.
Рис. 4 Сверхвысокая термическая стабильность нанозернистой меди с термически индуцированной релаксацией ГЗ.Измеренные температуры укрупнения (нестабильности) зерна в зависимости от начального среднего размера зерна в Cu. Литературные данные (серые символы и линия) включены для чистой меди, обработанной различными методами, включая механическую обработку, равноканальное угловое прессование, динамическую пластическую деформацию, кручение под высоким давлением, холодную прокатку, SMGT и конденсацию инертного газа. Синие кружки представляют собой нанозерна после механически индуцированной релаксации ГБ (M-GBR) во время процесса SMGT ( 34 — 40 ).Красные звезды представляют собой нанозерна после T-GBR из настоящего исследования. Планки погрешностей указывают диапазон изменения измеренных температур нестабильности в пределах диапазона размеров зерен.
Нанозерна после термической релаксации ГЗ демонстрируют исключительно высокую термическую стабильность с начальной температурой укрупнения ~ 0,6 T m . Это не только выше, чем у нанозерен Cu после механической релаксации ГЗ (около 0,45 T m ), но также примерно на 280 К выше, чем обычная температура рекристаллизации деформированной крупнозернистой Cu (0.4 Т м ). Это означает, что в термически релаксированных границах нанозерен достигается более стабильное состояние, чем в обычных ГЗ деформированной крупнозернистой меди. О значительной разнице в стабильности ГЗ можно судить по гораздо более высокой плотности двойников в быстро нагретых нанозернах, границы которых более интенсивно релаксированы. Природу термически релаксированных ГЗ и их свойства при повышенных температурах будет важно изучить.
ВЫВОДЫ
Термически индуцированная релаксация ГЗ возникает из-за образования двойников на границах нанозерен во время быстрого нагрева.В принципе, эта новая стратегия стабилизации будет применима к другим наноструктурированным материалам с низкой энергией упаковки, включая технические сплавы, такие как аустенитные нержавеющие стали и суперсплавы на основе Ni. Следовательно, это имеет особое значение для продвижения наноструктурированных материалов для высокотемпературных применений. Двойники отжига трудно сформировать в материалах с высокой энергией дефектов упаковки, таких как Al и Ni; принципы и методы стабилизации этих наноструктурированных материалов нуждаются в дальнейших исследованиях.
МАТЕРИАЛЫ И МЕТОДЫ
Пробоподготовка
Чистая Cu (чистота 99,97 мас.%) Была отожжена при 450 ° C в течение 2 часов с образованием рекристаллизованных структур. Стержни из Cu диаметром 10 мм обрабатывали с использованием SMGT ( 30 ) в жидком азоте при 77 К с параметрами обработки, указанными в таблице S1. Для каждого образца процесс SMGT повторяли 10 раз для получения толстого и однородного градиентного нанозернистого поверхностного слоя. Обработанная поверхность очень гладкая с шероховатостью Ra = 0.3 мкм. В свежеприготовленных образцах SMGT поверхностных трещин обнаружено не было.
Определение структуры
Структурную характеристику образцов проводили на сканирующих электронных микроскопах (FEI Verios 460) и просвечивающих электронных микроскопах (FEI Tecnai F20 и FEI Talos F200X) соответственно. Компоненты текстуры в поверхностном слое образцов as-SMGT Cu определяли с помощью дифракции обратного рассеяния электронов, оснащенной сканирующими электронными микроскопами. Характеристики ГБ анализировались с помощью картографирования ориентации в просвечивающем электронном микроскопе для различных образцов, которое проводилось с использованием оборудования NanoMEGAS (Брюссель, Бельгия) и системы ASTAR.Подробную информацию об этой технике можно найти в ( 31 ). Вкратце, интересующая область в образце фольги сканировалась наноразмерным электронным пучком с очень мелким шагом (3,6 нм в этом исследовании) в режиме дифракции ПЭМ, и электронограмма (EDP) в каждой точке сканирования была получена при высокая скорость благодаря быстрой камере CCD (устройство с зарядовой связью). Затем каждый EDP автоматически индексируется с помощью методов взаимного корреляционного сопоставления с предварительно рассчитанными шаблонами EDP, и ориентация зерен может быть идентифицирована.Мы подсчитали долю границ Σ1, Σ3 и Σ5-29 и тройных стыков, связанных с границами Σ3 и Σ5-29. Мы обнаружили, что доля специальных низкоэнергетических ГБ, очевидно, увеличивается после быстрого нагрева, как указано в таблице S2.
Подготовка образцов поперечного сечения для сканирующей электронной микроскопии (SEM) и наблюдений с помощью просвечивающей электронной микроскопии осуществляется по обычному пути резки, механической полировки и окончательной электрохимической полировки или утонения. Окончательная обработка была выполнена электрохимическим методом с использованием электролита, состоящего из 25% спирта, 25% фосфорной кислоты и 50% деионизированной воды при 0 ° C для Cu.Перед резкой обработанная поверхность защищалась тонким слоем меди, нанесенным методом электроосаждения.
Обработка быстрым нагревом
Обработка быстрым нагревом проводилась на оборудовании для дифференциальной сканирующей калориметрии PerkinElmer с точностью контроля температуры ± 0,1 К. Образцы as-SMGT нагревали до заданной температуры 523 К при различных скоростях нагрева и температуре. немедленно охлаждали до комнатной температуры для наблюдений SEM и TEM. Выбраны четыре скорости нагрева: 1, 80, 160 и 240 К / мин.Мы также проводили обработки путем быстрого нагрева образцов as-SMGT до 523 K и выдерживания температуры в течение 15 мин. Мы обнаружили, что размер зерна подповерхностного укрупненного слоя увеличивается с увеличением времени выдержки. Однако время выдержки не оказывает очевидного влияния на нанозернистые структуры в верхнем поверхностном слое.
Мы провели еще один тест на влияние температуры на термически индуцированную релаксацию ГЗ. Готовые образцы быстро (со скоростью 160 К / мин) нагревали до 393 К и выдерживали в течение 15 мин.Эта температура ниже самой низкой температуры образования двойников отжига в чистой Cu (473 K). Затем быстро нагретый образец отжигали при 523 K в течение 15 мин; мы наблюдали резкое укрупнение нанозерен размером от 60 до 180 нм до нескольких микрометров в верхнем поверхностном слое, как показано на рис. S2. Было подтверждено, что быстрый нагрев ниже температуры образования двойников отжига не вызывает релаксации ГЗ в нанозернах.
Измерения термостабильности
Термическая стабильность as-SMGT и быстро нагретых образцов Cu определялась отжигом при различных заданных температурах и выдержкой в течение 15 мин в трубчатой печи в защитной атмосфере Ar и с точностью контроля температуры ± 2 К.После отжига образцы охлаждались для наблюдений с помощью СЭМ и ПЭМ.
Рентгеноструктурный анализ
Мы оценили плотность двойников в верхнем слое толщиной 50 мкм в градиентной нанозернистой меди до и после быстрого нагрева до 523 К с помощью дифракции рентгеновских лучей (XRD) (микроплощадь x- лучевая дифрактометрия) с использованием Co-Kα-лучей. Шаг сканирования 0,005 ° был применен для записи картины XRD в диапазоне 2θ от 40 ° до 120 °, а размер пятна рентгеновского излучения составляет 50 мкм в диаметре. Рентгенограммы свежеприготовленного образца и быстро нагретых образцов показаны на рис.S3. Значения вероятности двойников β были оценены по наблюдаемой асимметрии пиков в соответствии с соотношением ( 32 ) β = ∆.CG (2θ111 °) −∆.CG (2θ200 °) 11 tgθ111 + 14,6 tgθ200, где ∆.CG ( 2θhkl °) = (2θC.G. ° −2θmax °) hkl, значения 2θhkl ° соответствуют максимуму пика, 2θC.G. ° — центры тяжести профилей с точечным счетом, а 2θmax ° были определены из профили, записанные на диаграмме с использованием метода экстраполяции средней точки хорды ( 33 ). Расчетное значение β быстро нагретого образца составляет около 1.37%, то есть один близнец на каждые 73 (111) самолетов. Значение β для свежеприготовленного образца составляет около 0,15%, т.е. один двойник на каждые 667 (111) плоскостей. Такие результаты показывают, что плотность двойников в быстро нагретом образце заметно выше, чем в исходном образце.
Измерения нанотвердости
Испытания образцов на нанотвердость проводили на трибоинденторе Hysitron. Условия измерения включают предварительно установленную нагрузку 3000 мкН, скорость загрузки и разгрузки 600 мкН / с и время выдержки 2 с.Значения нанотвердости усреднялись не менее чем по 10 отпечаткам. Расстояние между двумя соседними выемками превышает 15 мкм, чтобы избежать эффекта перекрытия.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution-NonCommercial, которая разрешает использование, распространение и воспроизведение на любом носителе, при условии, что конечное использование будет , а не для коммерческих целей и при условии, что оригинальная работа правильно процитирована.
Благодарности: Финансирование: Мы благодарны за финансовую поддержку Министерству науки и технологий Китая (2017YFA0204401 и 2017YFA0700700), Национальному научному фонду Китая (грант №51231006) и Китайской академии наук (грант № zdyz201701). Вклад авторов: X.Y.L. и К. начал расследование. X.Y.L. и X.Z. подготовили образцы и провели эксперименты. X.Y.L., X.Z. и K.L. проанализировал данные и написал статью. Конкурирующие интересы: Авторы заявляют об отсутствии конкурирующих интересов. Доступность данных и материалов: Все данные, необходимые для оценки выводов в статье, представлены в документе и / или дополнительных материалах.Дополнительные данные, относящиеся к этой статье, могут быть запрошены у авторов.
- Copyright © 2020 Авторы, некоторые права защищены; эксклюзивный лицензиат Американской ассоциации содействия развитию науки. Нет претензий к оригинальным работам правительства США. Распространяется по некоммерческой лицензии Creative Commons Attribution 4.0 (CC BY-NC).
Почему и как мы используем медную трубку
Услуги медных трубопроводов
Медь — идеальный материал для водопроводных, отопительных, газовых и пожарных спринклерных систем.
Медь, вероятно, самый широко используемый в Европе сантехнический материал, обладает следующими преимуществами:
- Надежный и проверенный временем: Медь транспортирует воду на протяжении тысячелетий: первая известная установка была заложена в древнем египетском храме почти 5000 лет назад.
- Высокое сопротивление: Он может выдерживать экстремально высокие и низкие температуры и давления, а также может подвергаться воздействию ультрафиолетовых лучей, температуры и кислорода окружающей среды.
- Универсальность: Медная трубка используется во многих продуктах и услугах: питьевая вода, домашнее отопление (традиционное и лучистое), газ, медицинские газы, солнечные энергетические системы, пожарные спринклеры, системы кондиционирования воздуха. Он отвечает требованиям безопасности в непревзойденном широком диапазоне температур и давлений.
- Энергосбережение: Медные трубы благодаря своей превосходной теплопроводности являются лучшим материалом для теплообмена (или холодных жидкостей). Вот почему наиболее эффективные лучистые обогреватели имеют контуры в медных трубках.
- Вторичная переработка: В случае сноса или ремонта медная труба может быть на 100% переработана без потери рабочих характеристик; Таким образом, объем отходов на полигоне не увеличивается, а ресурсы рудника в дальнейшем не используются.
- Healthy: Сантехническая труба изготовлена из меди на 99,90%, и ее состав со временем не изменится; внутри нет никаких добавок, летучих органических соединений или пигментов. Кроме того, он является предпочтительным материалом для транспортировки медицинских газов, таких как чистый кислород, в больницах.
- Beautiful: Медная трубка может быть установлена снаружи стены и, благодаря своему привлекательному виду, может быть использована даже для изготовления красивых аксессуаров для кухни и ванных комнат, таких как настенные радиаторы.
- Универсальность: Медная труба и медные фитинги соответствуют международным стандартам. Они доступны на всех европейских рынках, а компоненты трубопроводной системы взаимозаменяемы, независимо от производителя.
Питьевая вода
Медная труба веками использовалась для транспортировки питьевой воды.Медная трубка может выделять в воду только ионы меди, которые необходимы для метаболизма нашего тела: вода, которую мы пьем и используем, не будет содержать добавок, пигментов, летучих органических соединений или других синтетических соединений.
Отопление
Медь является предпочтительным продуктом для трубопроводных систем отопления благодаря ее надежности и безопасности. Он плавится при 1083 ° C, поэтому горячая вода и пар не смягчают и не изменяют форму трубки; высокая температура не сокращает срок службы трубки и, следовательно, срок службы установки.Кроме того, медь обладает отличной теплопроводностью и по этой причине является наиболее эффективным материалом для систем, которые должны обмениваться теплом. Так обстоит дело, например, с лучистым отоплением под полом или под стенами: системы, сделанные из меди, имеют более короткие пути трубопроводов по сравнению с пластиковыми системами, что означает меньшие потери тепла и меньшее потребление энергии для циркуляционных насосов.
Газовый транспорт
Медная труба для газа может быть размещена практически везде: внутри и снаружи, встраиваемая, в землю и пол или в специальные конструкции, поскольку она соответствует требованиям безопасности для такого типа установки.Красный металл непроницаем для газов и воздуха, поэтому утечки или загрязнения извне невозможны; кислород, ультрафиолетовые лучи и температура не снижают его механических свойств. Во всей Европе медные трубы разрешены стандартами; проектировщики и установщики полагаются на него, зная, что он не горит и не распространяет огонь (класс A1 по реакции на огонь) и обеспечивает газонепроницаемые соединения и фитинги.
Сохранение тепловой окраски меди при прозрачном покрытии
Образование, Алоха и большинство
весело вы можете получить в отделке
Интернет-ресурс №1 в мире с 1989 года
——Самые свежие публикации:
14 декабря 2020 г. А.Сегодня я накрасил свой фонарик прозрачным слоем, окрашенным в медь, и он работает!
Это было на моей полке в моей мастерской. Кажется, я купил его в магазине, где продают серебро, цепи, находки и инструменты много лет назад. Не могу поверить, что у меня что-то было, так как рыба цвета факела и колибри потемнели от порошкового покрытия.
Название продукта — Protecta Clear от Everbrite, Inc.
Веб-сайт: www.everbritecoatings.com/ProtectaClear.htm
Телефон № 916-852-0200
Надеюсь, это кому-то поможет.Я потратил много времени на чтение этого сайта, многому научился, но у меня был свой ответ! Лол
Ким Бейтс— Сан-Сити, Аризона
| Декабрь 2020 г. A. Спасибо, Ким! Сегодня все, у кого есть телефон, страдают от роботизированных звонков, и каждый, у кого есть веб-сайт общественного обсуждения, переносит сотни роботизированных сообщений о спаме в комментариях. По этой и другим причинам мы стараемся поддерживать технические обсуждения и не публикуем предложения брендов или источники. Но Everbrite поддерживает этот сайт, поэтому мы, безусловно, рады предложить ваше сообщение в качестве рекламного ролика 🙂 Удачи и С уважением, Тед Муни, П.E. RET Алоха — идея, которую стоит распространять finish.com — Pine Beach, New Jersey |
Предыдущие вопросы и ответы по теме, начиная с:
1999 г.Я испробовал все формы тепла (оксиацетилен, электрическая духовка и газ для домашней плиты), чтобы произвести эффект, наблюдаемый на этом орнаменте холодильника в виде бабочки, но не смог воспроизвести яркие цвета.
Предоставлено Мелом Оуэном
Поскольку у меня их 2, я предполагаю, что их можно продублировать.Добавлен ли еще один ингредиент (масло?) Или это вопрос постоянной температуры?
Мел Оуэн— Техас
2000 г.
A. Раскраска бабочки может быть выполнена с помощью тепла. Вам не нужно обмазывать свою работу вредными химическими веществами, чтобы получить отличный цвет. Вы должны экспериментировать, как никогда раньше, работать с теплом от любого факела и «раскрасить» медь пламенем. Вы также можете попробовать работать с маслами. Однажды я отжигал в печи немного латуни и слишком рано достал ее для отжига, но заводское масло, должно быть, все еще было на нем, потому что оно давало удивительные цвета и узоры.(Кусочки металла были обрамлены и вывешены в галерее «Out of Hand Gallery» в Луненбурге, Новая Шотландия!) С смазкой может быть легче работать, чем с маслом. Вы должны много играть с фонариком, потому что металл легко нагреть слишком сильно, и цвет станет неприятно-коричневым. Также попробуйте поработать со складыванием детали и отжигом. Когда вы открываете работу, вы получаете интересные цветовые узоры из-за количества кислорода, попадающего на металл в складках.
Уловка заключается в том, чтобы играть! Удачи и ВСЕГДА НАДЕВАЙТЕ НАДЕЖНУЮ СРЕДНЮЮ БЕЗОПАСНОСТЬ! ЗАЩИЩАЙТЕ СЕБЯ И ОКРУЖАЮЩУЮ СРЕДУ!
М.Jardine— Фармингтон, Новая Шотландия, Канада
Кажется, что все прозрачные покрытия удаляют цвета пламени
2002 г.В. У МЕНЯ НЕТ ПРОБЛЕМ ПОЛУЧЕНИЕ МЕДИ, ЧТОБЫ ИЗМЕНИТЬ ПОЧТИ ЛЮБОЙ ЦВЕТ. Это котел после его нагрева.
Моя проблема заключается в потере всех синих, красных и пурпурных цветов. Когда я использую какой-либо продукт, чтобы медь не потускнела. Другая фотография — после нанесения продукта.
Я применил большое количество разнообразных продуктов, и ни один из них не дал мне удовлетворительного результата.Буду очень рад любому совету, который вы дадите.
СОННИ ГРАЭМ— ОЗОНА, ФЛОРИДА
2003
В. Да, у меня такая же ситуация, как и у Сонни. Я пробовал распылять на медь, окрашенную в тепло, прозрачным Krylon или лаком, но кажется, что под поверхностью прозрачного герметика она окисляется (примерно через 6 месяцев). Как сохранить цвета, полученные при нагревании, без окисления? У меня также часто бывает шероховатая отшлифованная поверхность, поэтому я не уверен, что можно использовать воск.
Джон Уотерс— Феникс, Аризона
А.К сожалению, у меня нет хороших новостей для вас, Сонни и Джон 🙁
Некоторая часть красивой окраски происходит от дифракционных картин, таких как радужный блеск капли масла на воде, а не от пигментации. Масло на самом деле не радужно окрашено, это то, как очень тонкий слой отражает свет. Когда вы наносите на изделие прозрачный слой, это все равно, что пытаться положить лист стекла на масляную радугу, чтобы сохранить ее. Цвета, которые «действительно присутствуют» в виде пигментов, будут сохранены, но дифракционные цвета исчезнут.
Тед Муни, P.E.
Стремление к жизни Алоха
Finish.com — Пайн-Бич, Нью-Джерси
2003 г.
A. Попробуйте использовать полиуретан на основе МАСЛА вместо лака. Или другой продукт на масляной основе.
Проблема с продуктами на водной основе и многими кислотными лаками заключается в том, что медь создает еще одну патину, не обязательно ту, которую вы хотите.
Я не пробовал использовать его с такими цветами, как ваш, но я использовал его как для чистой матовой меди, так и для сернокислой меди с патиной (в основном темные цвета), и он сохраняет большую часть цвета.
У меня есть медный обеденный сервиз, который я сделал около 7 лет назад, и он все еще почти того же цвета (это изображение, когда ему около 4 лет).
Я просто экспериментировал с несколькими брендами, и цена, похоже, не имеет значения. Самый дешевый сработал так же. Полиуретан также имеет то преимущество, что он эластичен, в отличие от лака, который через некоторое время будет иметь микротрещины из-за температурного расширения и усадки меди и потеряет свою защиту.
Я протестировал его, согнув кусок с покрытием вперед и назад и оставив его в соленой воде на месяц без видимого потускнения, пока кусок лака почернел.
Алик Перах— Сан-Диего, Калифорния
2004 г.
В. Я увлекаюсь изготовлением медных колокольчиков. Я сжигаю медные колокольчики пропановой горелкой, чтобы выделить разные цвета в трубке. Когда я наношу отделку на трубу, цвета блекнут, а некоторые цвета, например фиолетовый, полностью исчезают, превращаясь в оранжевый. Я использовал лак, продукты Rustoleum, шеллак и различные прозрачные лаки на водной основе (акрил), используемые для хобби и купленные в магазинах для хобби, и все с одинаковыми результатами.Кто-нибудь знает какую-либо отделку кистью или распылителем, которая не изменит окисление трубы.
Тони Райтлюбитель — Хантингтон-Бич, Калифорния
2005
Q. Hi
Я пытаюсь сохранить цвет на меди с патинированным ТЕПЛОМ. Я пробовала Incralac на водной основе, пасту-воск, аэрозольный лак, Крылон 1301 [аффил. ссылка на информацию / продукт на Amazon] . Лучшие результаты показал Крылон. Однако он все еще меняет цвет. Как вы думаете, Incralac на основе растворителя лучше сохранит цвет? Спасибо за ваш вклад.
Брюс Маккимми— Мосс-Бич, Калифорния
2006 г.
А. Привет. Я делаю свистульки из меди и раскрашиваю их теплом. Мне очень повезло отделать их латунным лаком. Он разработан для латуни и меди и хорошо работает. Это несколько дорого, но работает. Поищите на ebay, иногда удастся найти выгодную сделку.
Рик Хинк— Холиок Колорадо
2005 г.
Я пробовал много вещей, чтобы мои медные фонтаны оставались красивыми и блестящими, воск и акриловая отделка.Но, к сожалению, худшее, что я обнаружил, — это нанесение на них лаковой отделки. Будь то сочетание внешних элементов или воды, или того и другого, я не знаю, но через пару месяцев он начинает обесцвечиваться, и финиш становится действительно тусклым.
Я экспериментирую с компанией в Великобритании, которая работает с прозрачным порошковым покрытием, и я пытаюсь получить что-то, что можно было бы использовать на открытом воздухе с водой в течение длительного периода времени. Возможно, пройдет некоторое время, прежде чем я получу достойный результат, но если он сработает, я опубликую информацию позже в этом году.
Крейг Хамфрис— Лондон, Великобритания
2004 г.
A. Я имел большой успех, сохраняя синий, пурпурный и красный цвета в моей обработанной пламенем меди. Я работал с местной порошковой краской и обнаружил, что прозрачная отделка, запеченная за половину обычно необходимого времени, делает свое дело. Это позволяет порошку расплавиться до прозрачной глазури и придать меди глубину, которую не позволяет распыление при обработке, но, оставив ее на половину времени, медь не нагревается слишком сильно, чтобы изменить цвет.
Эмили Льюис— Берлингтон, Северная Каролина
2007 г.
А.Я понимаю проблемы потери цвета после теплового окрашивания. Делаю стальную окраску. Лучше всего использовать холоднокатаную сталь. После получения желаемого эффекта оставьте его на ночь или дольше и дайте ему остыть. Затем я использую спрей под названием EnviroTex high gloss =>
Держите баллончик на расстоянии не менее 18 дюймов от обрабатываемой детали и распылите легкий слой. Дайте ему высохнуть, а затем повторите то же самое. Делайте это несколько раз, но НЕ СЛИШКОМ БЛИЖАЙТЕ. Вы можете потерять немного более светлого синего, но глубокий синий и фиолетовый останутся.Также прозрачное порошковое покрытие подействует вдвое быстрее, чем время выпекания. Когда порошок начинает тускнеть, я выключаю огонь и вытаскиваю изделие из духовки. Появляется новое низкотемпературное прозрачное порошковое покрытие. Пока нет информации об этом.
Сварка Mike LeMaster— Delta Colorado
24 января 2008 г.
A. Эй, я много раскрашиваю все виды металлов, лучшее, что я нашел, это «Микрокристаллический воск эпохи Возрождения» [аффил. ссылка на информацию / продукт на Amazon] это полироль на основе микрокристаллического воска.Это немного дороговато, но лучшее, что я нашел, оставляет естественную поверхность (не блестящую). Он немного «смягчает» цвета (в зависимости от того, как / когда вы наносите), но если все сделано правильно, цвет НЕ теряется.
Фрэнк Бахманн— Глен Берни, Мэриленд
25 января 2008 г.
Как мы все знаем, если вы нанесете каплю масла в лужу с водой, то увидите красочный радужный блеск. Цвета радуги — это не цвет масла, это картина интерференции / дифракции, эффект призмы, который возникает, когда свет встречается с очень тонкой пленкой прозрачного материала.
Некоторые из ваших теплых красок представляют собой настоящие пигменты и патины. Но некоторые цвета, особенно более тонкие, таковыми не являются: это дифракционные картины, вызванные очень тонкими пленками масла или прозрачных оксидов на поверхности. Прозрачное покрытие удаляет эти цвета не в результате химической реакции, пожелтения (отдельно) или фильтрации, а просто в результате присутствия. Если вы изучаете тему карнавального стекла (которое также получает цвета от дифракционных картин, а не пигментов), вы можете найти кое-что полезное о толщине пленки и т. Д., что поможет сохранить тепловую окраску. Просто мысль, чего бы это ни стоило, от человека, который не занимается этим искусством, но считает, что, исходя из этого, воск — лучший выбор 🙂
Тед Муни, P.E.
Стремление к жизни Алоха
Finish.com — Пайн-Бич, Нью-Джерси
Окрашивание пламенем для выделения цветов
2004 г.В. Скажите, пожалуйста, где я могу найти помощь. Я хочу нагреть медный лист 110 калибра 0,032 .. Я хочу выделить участки оранжевого, желтого, красного и т. Д.Какой обычный инструмент я могу использовать и насколько он должен быть горячим? Вы можете порекомендовать какой-нибудь веб-сайт, статью или книгу? СПАСИБО ПУЧКАМ
Дотти Сезариолюбитель Тампа, Флорида
2005
В. Меня интересует, что вы обнаружили при окрашивании меди при различных температурах. Но по другой причине. Моя медная раковина переднего фартука была повреждена, и на ней была красивая отделка «Огонь и лед». При ремонте его пришлось отполировать, и я хотел бы воспроизвести все представленные цвета.(Я понимаю, что не могу точно воспроизвести это.) Спасибо за любую информацию!
Пегги Томас— Амарилло, Техас
2006
В. Я создаю металлическую скульптуру для террасы и у бассейна из листового металла 18 калибра. Я хотел бы добавить случайный цвет (синий или любой другой возможный оттенок) к скульптуре с помощью кислородно-ацетиленовой горелки. Как это достигается и какие настройки я использую на своих регуляторах? Искали книги по этой теме, но не нашли.
Полли Фискхудожник по металлу — Даллас, Техас
2006
В.Получение красного цвета из меди с помощью фонаря. Я новичок в кузнечном деле и пытаюсь добиться цвета своих листьев и бабочек, когда вырезаю их с помощью факела. Кто-нибудь знает как это сделать? Это в настройках регулятора что ли? Я все перепробовал.
Джереми Уитмир,, медник — Медная страна, штат Мичиган.
2004 г.
A. Мне удалось получить широкий спектр оттенков меди с помощью обычной пропановой горелки. Хитрость заключается в том, чтобы нагреть медь до высокой температуры, а затем использовать горелку, как малярную кисть.Нагрейте одну часть изделия, пока не начнет проявляться цвет, а затем поэкспериментируйте. Долгое время под факелом у самого сердца пламя дает бледно-зеленый, серебряный и золотой. Быстрый удар краем пламени дает голубизну. Более длительное время на краю пламени дает красный и розовый оттенки.
Джо Николас— Канзас-Сити, Миссури
2007
A. Когда я делаю небольшие проекты на меди, я обычно получаю хороший эффект масштаба огня, «окрашивая» детали, которые я хочу раскрасить, флюсом (флюс для твердого припоя), давая ему высохнуть, затем переворачивая деталь и нагревая его со спины.
Я обычно нагреваю его очень горячим, чтобы получить красивый красный цвет, но держите пламя подальше, иначе он сожжет флюс и приобретет необычный цвет. Слегка используйте флюс …
— Санта-Крус, Калифорния
2007
A. Если вы хотите, чтобы медь стала красной, нагрейте ее настолько сильно, насколько это возможно, но не плавите, затем окуните или опрыскайте водой. Когда я делаю розу из меди, получается очень яркая красная роза.
Кузнец Лайл Винн— Флоууд, Миссисипи
Использование солей бромида или поташа для красок
2004 г.В.Мы пытаемся создать сцену тропического заката из листовой меди и хотели бы украсить работу преимущественно синими и красными оттенками. Металлург упомянул нанесение бромидных солей на металл перед нагреванием пропановой горелкой. У кого-нибудь был успех с этим методом? Есть другие рекомендации?
Спасибо!
Боб Йеманс— Колумбус, Огайо
2004
В. Я хотел бы знать, какой процесс мне нужно использовать, чтобы обесцветить медь или латунь. Я считаю, что хочу протравить металл, но не знаю, какие химические вещества использовать или, возможно, как нагреть его для этого.Я работаю над логотипом, который будет большим, и я хочу использовать обесцвеченный и / или потрепанный металл. Мы будем благодарны за любую помощь, которую вы можете предложить.
Спасибо
Пол
Пол Ле Пейнхудожник — Данидин, Флорида
2005
В. Я хотел бы знать, как лучше всего выделить цвет латуни с помощью паяльной лампы. Стоит ли использовать что-то помимо тепла. Кроме того, как лучше всего сохранить цвета? Стоит ли его использовать полиуретан? Я хочу создавать предметы искусства из меди и получать красивые пурпурные и золотые тона от жары.
Линн Шмуклюбитель — Хиллсборо, Нью-Джерси
2006
В. Как использовать калий для окрашивания медных изделий? Я хочу узнать, что это за приложение и как и с чем смешать калий?
Росс Д. ЛэрдPrimal Iron Originals — Сан-Диего, Калифорния
Каков химический состав теплового окрашивания?
2006 г.В. Я пытался сформировать оксидную пленку на меди путем термического окисления при 350 ° C в окружающей атмосфере. Через 10 минут на меди образовалась серая пленка, которую я предположил, это CuO.Примерно через час при температуре 350 ° C поверхность стала разноцветной с пятнами розового, фиолетового и серо-черного цветов! Какие возможные соединения вызывают эти цвета?
Нандини ВенкатараманСтудент-исследователь — Тусон, Аризона
30 апреля 2008 г.
В. Я новичок в работе с медью. Я использую не листовую медь, а тяжелую медную проволоку методом холодной штамповки. Я экспериментирую с различными способами патинирования и окрашивания, и мне очень нравится тепловое окрашивание. Я поэкспериментировал, используя жаровню в своей духовке, и добился великолепного ярко-розового / фиолетового цвета.Однако, как только медь остыла, она быстро потускнела до оранжевого … очень красивого ярко-оранжевого цвета, но НЕ того цвета, который я хотел. Есть ли способ сохранить этот прекрасный розовый цвет? Я не видел этого раньше ни в одной законченной работе с медью, поэтому мне очень любопытно, является ли это просто цветом, который проявляется, когда медь горячая, или можно ли сохранить этот конкретный оттенок. Любая помощь будет очень признательна!
Женевьев Ланкастерлюбитель, дизайнер — Атланта, Джорджия
—-
Ed. примечание: 6 вопросов подряд 🙁
Нет бесплатных экспертов по отделке, которые ходят за кулисами и ждут, чтобы наброситься и ответить на ваши вопросы, ребята.Этот форум взаимопомощи будет продолжать работать только в том случае, если вы потратите время на помощь другим, а не просто зададите свои вопросы 🙂
10 июня 2008 г.
A. Я работаю с медью около 13 лет и получил красивую радужную патину с печенью серы. [аффил. ссылка на информацию / товар на Amazon]. Это безвредное вещество, доступное в кристаллической форме из любого химического центра или в жидкой форме из любого садового центра — это оранжевая жидкая часть спрея из спящего масла, которая используется для опрыскивания фруктовых деревьев поздней весной и дешевле, чем кристаллы.Сера в печени — это вещество, которое пахнет тухлыми яйцами (помните бомбы-вонючки?), Так что будьте осторожны при использовании.
Его следует смешивать с водой, и он дает налет от очень светло-коричневого до черного, в зависимости от соотношения воды и серы. Меньше воды = более темный цвет. Когда я наношу кистью, я получаю самый красивый переливающийся оттенок. Поэкспериментируйте с разными пропорциями лома, пока не добьетесь желаемого эффекта. Эффект мгновенный, и если он вам не нравится, очистите медь и попробуйте еще раз.Патина нестабильна, поэтому после достижения желаемого эффекта ее необходимо покрыть лаком. Кроме того, водная смесь довольно быстро теряет жизнеспособность, поэтому смешивайте только то, что вы будете использовать, через несколько -30 минут, максимум.
Надеюсь, кому-нибудь это пригодится.
Ура!
Кэтлин Дональдсон— Кингстон, Онтарио, Канада
4 мая 2009 г.
A. В настоящее время я учусь по специальности слесарь. Я много экспериментировал с тепловыми патинами и узнал о некоторых вещах, о которых я не видел в этой ветке.Я использую пропановую горелку с самым широким наконечником, который я могу найти, тепло должно быть очень общим и не слишком сфокусированным. На более крупных предметах я даже использую кончик бутона розы. Для получения ровного цвета медь нужно нагревать равномерно и очень небольшими порциями. Окончательный цвет проявится только после того, как медь остынет, поэтому уберите фонарик и просто наблюдайте за изделием. Цвет будет развиваться по мере охлаждения меди. Если изделие нагревали неравномерно, он будет иметь неоднородный цвет. Трюк, которому я научился и который добился огромного успеха, заключается в том, чтобы как можно быстрее охладить на воздухе (НЕ ТУШЕНИЕ! Погружение в воду приведет к отслаиванию цвета).Я делаю это, выбегая зимой на улицу и раскачивая изделие в холодном воздухе. Вы также можете положить его в морозильную камеру, когда увидите, что цвет, который вам нравится, проявляется. Не ставьте изделие на решетку в морозильной камере, это может привести к неравномерному цвету в тех местах, где металл соприкасается с решеткой. Использование воздушного компрессора и обдув детали тоже довольно эффективно, сжатый воздух довольно холодный. Мне потребовалось много экспериментов и много неудач, но я могу точно определить любой цвет в цветовом спектре, нагревая медленно и равномерно, удаляя тепло и наблюдая, а также охлаждая воздух как можно быстрее.Несмотря на то, что я считаю себя достаточно опытным в нанесении тепловой патины, я все же марину большинство кусочков и начинаю несколько раз, чтобы определить точный цвет, который я ищу, каждый кусок будет немного отличаться в зависимости от его размера, несоответствий в толщине и, иногда, , форма. Что касается запечатывания цвета, я не нашел ничего, что могло бы быть эффективным, лично мне нравится идея постоянно меняющегося предмета, если вы действительно хотите, вы всегда можете очистить его и повторно нанести патину после ее потери.
Коди Пиннов— Меномони, Висконсин
21 декабря 2009 г.
А.Я делаю колокольчики из медных трубок цвета пламени. Кажется, я получаю лучшие цвета, нагревая трубки фонариком до тех пор, пока цвета не начнут проявляться, затем я даю ему «отдохнуть» и остыть всего на пару минут, затем снова ударяю по нему фонариком и действительно заставляю цвета выходить . Я также нашел продукт, который действительно работает и не тускнеет. Это лак X-I-M 900. Он предназначен для защиты полированных цветных металлов. Я очень хорошо держусь даже на улице, и цвета не тускнеют.Я нашел его в моей местной профессиональной компании по поставке автомобильной краски. Это сделано XIM Products; они продают это в Интернете. ИСПОЛЬЗУЙТЕ 3 ИЛИ 4 ЛЕГКИХ СЛОЯ. Сначала он выглядит немного морозным, но быстро сохнет. Удачи.
Dale Firm— Кантон, Огайо
В. Почему цвет чистой меди, которая используется в Циклотерне, меняется на цвет радуги при нагревании горелкой? Могу ли я сделать точную копию? deba prasad dashсотрудник — Калькутта, Вестбангал, Индия 12 января 2010 г. А.Привет, Деба. Я бы предположил, что окраска радуги — это оксиды меди, как описано на этой странице. Я думаю, что создание дубликата — это больше связано с художественным мастерством и опытом, чем с научным пониманием технологии. Другими словами, я сомневаюсь, что смогу сделать дубликат, но верю, что опытный художник по металлу может 🙂 Удачи с этим. С уважением, Тед Муни, P.E. Стремление к жизни Алоха Finish.com — Пайн-Бич, Нью-Джерси |
23 октября 2010 г.
А.Всем привет.
Я много работаю с патинированием из ниобия и титана, поэтому у меня есть некоторая информация, которая может помочь.
Цвета радуги — это дифракция света, вызванная прозрачными оксидами. Цвет зависит от толщины оксида.
С научной точки зрения отношение толщины оксида к длине волны света определяет конечный цвет, который вы видите.
Поэтому ответ — протереть пламя и поэкспериментировать. Невозможно точно сказать, сколько.
Помогла бы атмосфера с высоким содержанием кислорода.Лучше всего подойдет кислородно-ацетиленовая горелка с высоким содержанием кислорода.
Райан Дидерих— Уилбрахам, Массачусетс, США
27 февраля 2011 г.
A. Медь можно окрасить теплом и сохранить цвета. Занимаюсь этим с начала 90-х. Цвета, которые я могу достичь, — медный, коричневый, фиолетовый, синий, зеленый, желтый, оранжевый, розовый и черный. Однако на это уходит много-много часов проб и ошибок.
Веррел Мартин— Фултон, штат Миссури
4 апреля 2011 г.
А.Я не очень много работал с медью, и я использовал только серебро на уроке, похоже, никто не упоминал об использовании теплового пистолета, это похоже на супер горячий фен, очевидно используемый для отслаивания краски, во всяком случае, один день, когда я был в подвале, там была тепловая пушка и кусок меди, поэтому я включил ее и применил на меди, она работала очень хорошо, медь прошла все стадии окрашивания по мере того, как она постепенно становилась все горячее. мне тоже казалось, что я очень контролирую. Просто подумал, что выложу это там!
Logan Swift— Монмут, Нью-Джерси, США
19 мая 2011 г.
А.Рекомендую использовать лак на масляной основе. Несколько слоев — это все, что вам действительно нужно. Если вам нужна дополнительная защита, можно нанести один слой лака, а затем самовыравнивающуюся эпоксидную смолу, которую можно вылить на поверхность. Комбинация этих двух свойств делает медь действительно «популярной». Плюс эпоксидной смолы в том, что вы можете отшлифовать ее и залить новым слоем поверх после нескольких лет носки, и она снова будет выглядеть совершенно новой. Надеюсь, это поможет.
Дон АнджелоСпринг-Хилл, Теннесси
10 декабря 2011
А.Другая причина, по которой тепловая патина может не длиться долго или выглядеть так же, как раньше, — это природа самой патины. Если изделие будет находиться на открытом воздухе, металл со временем нагреется и изменит цвет. Я убедился в этом на собственном опыте. У меня такое случилось с одной из моих вещей, которая летом ненадолго осталась в машине. Потом он выглядел размытым. Кроме того, что он был в машине, к нему ничего не прикасалось, даже прямые солнечные лучи.
У меня есть еще одна деталь, которую я сижу внутри, которую я сделал, я не накрывал ее каким-либо прозрачным слоем, и это нормально.Тепловая патина будет держаться долго, но это ни в коем случае не полностью стойкая окраска, в конечном итоге она потускнеет и потускнеет или потускнеет.
— Лаббок, Техас, США
(вы на 1-й странице ветки) Следующая страница>
нареч.
этот текст заменяется на bannerText
Заявление об ограничении ответственности: на этих страницах невозможно полностью диагностировать проблему отделки или опасности операции.Вся представленная информация предназначена для общего ознакомления и не отражает профессионального мнения или политики работодателя автора. Интернет в основном анонимный и непроверенный; некоторые имена могут быть вымышленными, а некоторые рекомендации могут быть вредными.
Если вы ищете продукт или услугу, связанную с отделкой металлов, посетите эти каталоги:
О нас / Контакты — Политика конфиденциальности — © 1995-2021 finish.

 Когда изделие остынет, промойте его водой и насухо вытрите мягкой тряпкой
Когда изделие остынет, промойте его водой и насухо вытрите мягкой тряпкой

 ) + 2 NO 3 — (водн.) -> [Cu (H 2 O) 6 ] 2+ (водн.) + 2 NO 2 (г)
) + 2 NO 3 — (водн.) -> [Cu (H 2 O) 6 ] 2+ (водн.) + 2 NO 2 (г) )
) )
) ) В Cu (OH) 2 (s)
) В Cu (OH) 2 (s)
 ) Обратно в Cu (s)
) Обратно в Cu (s)