Плавление — Википедия

Плавле́ние — это процесс перехода тела из кристаллического твёрдого состояния в жидкое, то есть переход вещества из одного агрегатного состояния в другое. Плавление происходит с поглощением теплоты плавления и является фазовым переходом первого рода, которое сопровождается скачкообразным изменением теплоёмкости в конкретной для каждого вещества температурной точке превращения — температура плавления.
Способность плавиться относится к физическим свойствам вещества[1]
При нормальном давлении, наибольшей температурой плавления среди металлов обладает вольфрам (3422 °C), среди простых веществ — углерод (по разным данным 3500 — 4500 °C[2]) а среди произвольных веществ — карбид тантала-гафния Ta4HfC5 (3942 °C). Можно считать, что самой низкой температурой плавления обладает гелий: при нормальном давлении он остаётся жидким при сколь угодно низких температурах.
Многие вещества при нормальном давлении не имеют жидкой фазы. При нагревании они путём сублимации сразу переходят в газообразное состояние.
Плавление смесей и твёрдых растворов[править | править код]
У сплавов, как правило, нет определённой температуры плавления; процесс их плавления происходит в конечном диапазоне температур. На диаграммах состояния «температура — относительная концентрация» имеется конечная область сосуществования жидкого и твёрдого состояния, ограниченная кривыми ликвидуса и солидуса. Аналогичная ситуация имеет место и в случае многих твёрдых растворов.
Фиксированной температуры плавления нет также у аморфных тел; они переходят в жидкое состояние постепенно, размягчаясь при повышении температуры.

Технически плавление вещества осуществляется с помощью подвода тепловой энергии снаружи образца (внешний нагрев, например, в термической печи) или непосредственно во всём его объёме (внутренний нагрев, например, резистивный нагрев при пропускании тока через образец, или индукционный нагрев в высокочастотном электромагнитном поле). Способ плавления не влияет на основные характеристики процесса — температуру и скрытую теплоту плавления, но определяет внешнюю картину плавления, например, появление квази-жидкого слоя на поверхности образца при внешнем нагреве.
Считается, что плавление характеризуется потерей дальнего ориентационного межатомного порядка в кристалле с переходом к «жидкоподобному» или «газоплотному» беспорядку.
Природа плавления[править | править код]
Поясним вначале, почему при некоторой температуре тело предпочитает разорвать часть межатомных связей и из упорядоченного состояния (кристалл) перейти в неупорядоченное (жидкость).
Как известно из термодинамики, при фиксированной температуре тело стремится минимизировать свободную энергию F=E−TS{\displaystyle F=E-TS}. При низких температурах второе слагаемое (произведение температуры и энтропии) несущественно, и в результате всё сводится к минимизации обычной энергии E{\displaystyle E}. Состояние с минимальной энергией — это кристаллическое твёрдое тело. При повышении температуры, второе слагаемое становится всё важнее, и при некоторой температуре оказывается выгоднее разорвать некоторые связи. При этом обычная энергия E{\displaystyle E} слегка повысится, но при этом сильно возрастет и энтропия, что в результате приведёт к понижению свободной энергии.
Динамика плавления[править | править код]
Тепловые колебания атомов в решетке кристалла: точки — атомы, соединяющие линейные отрезки — межатомные связи Поведение атомов жидкости после перехода кристалла через точку плавления, как в среднем постоянные для заданной температуры разрывы и восстановления межкластерных и внутрикластерных межатомных связей (короткие утолщенные отрезки — разорванные связи)[3]Изначально, в умозрительном, то есть не количественном, представлении считалось, что в динамике плавление происходит следующим образом. При повышении температуры тела увеличивается амплитуда тепловых колебаний его молекул, и время от времени возникают структурные дефекты решётки в виде перескоков атомов, роста дислокаций и других нарушений кристаллической решетки [4]. Каждый такой дефект, возникновение и перемещение дислокаций требуют определённого количества энергии, поскольку сопровождается разрывом некоторых межатомных связей. Стадия рождения и накопления дефектов называется стадией предплавления. Кроме того, на этой стадии, как правило, при внешнем нагреве возникает квази-жидкий слой на поверхности тела. Считается, что при некоторой температуре концентрация дефектов становится столь большой, что приводит к потере ориентационного порядка в образце, то есть плавлению.
Однако, в связи с тем, что механизм термодеструкции кристалла за счёт образования дефектов и роста дислокаций, протекающей в широком диапазоне температур, не приводит к фазовому превращению 1-го рода, то есть к скачку термодинамических характеристик вещества в конкретной, фиксированной для каждого вещества температурной точке, то Линдеман
Теоретические исследования В. Андреева[10][11] показали, что динамика плавления кристаллического тела, как фазового превращения 1-го рода, определяется (в отличие от модели накопления дефектов и дислокаций и модели Линдемана) «катастрофичеким» (crash — [крэш]) конформационным преобразованием (инвертированием) структуры группы атомов при их тепловых колебаниях с амплитудами, меньшими межатомных расстояний в решетке, сопровождаемым разрушением межатомной связи при преодолении потенциального барьера инвертирования в фиксированной температурной точке с затратой постоянной величины энергии, ниже энергии атомизации решетки, и равной удельной теплоте плавления. Этот механизм приводит к подтверждаемой экспериментально кластерной структуре связанного (конденсированного) жидкого состояния с постоянным (для заданной температуры) средним числом разрывающихся и восстанавливающихся межкластерных и внутрикластерных межатомных связей, обеспечивающих сохранение объёма и определяющих подвижность (текучесть) и химическую активность жидкости. С ростом температуры количество атомов в кластерах уменьшается за счет увеличения разорванных связей. Образующиеся свободные атомы (молекулы) испаряются с поверхности жидкости или остаются в межкластерном пространстве в качестве растворённого газа (пара). При температуре кипения вещество переходит в моноатомное (мономолекулярное) газообразное (парообразное) состояние.
Плавление в двумерных системах[править | править код]
В двумерных или квази-двумерных системах кристалл является гораздо более шатким объектом, чем в трёхмерном случае, а именно у двумерного кристалла нет дальнего позиционного порядка. Для сравнения, в одномерном случае кристалл при конечной температуре вообще не может быть стабильным.
Как выяснилось, это приводит к тому, что плавление двумерного кристалла происходит в два этапа. Вначале кристалл переходит в так называемую гексатическую фазу, в которой теряется ближний позиционный порядок, но сохраняется ориентационный, а затем происходит потеря и ориентационного порядка и тело становится жидким.
- ↑ С. Т. Жуков Химия 8-9 класс, Глава 1. Основные представления и понятия химии
- ↑ Разброс экспериментальных данных связан, по видимому, с фазовым переходом графит-карбин и различной скоростью нагрева при измерениях. Климовский И. И., Марковец В. В. Влияние фазового перехода графит-карбин на излучательную способность графитовых образцов при их нагревании до температур 3000 K и более // International Scientific Journal for Alternative Energy and Ecology. — 2007. — № 6 (50). — С. 50—59. Архивировано 26 октября 2015 года.
- ↑ Андреев В. Д. Избранные проблемы теоретической физики.. — Киев: Аванпост-Прим,. — 2012.
- ↑ Мейер К. Физико-химическая кристаллография, М., «Металлография», 1972
- ↑ Lindemann F. A. // Phys.Z., 1910, v.11, p.609
- ↑ Wood W. W., Jacobson J. D. Preliminary Results from a Recalculation of the Monte Carlo Equation of State of Hard Spheres // J. Chem. Phys.. — 1957. — № 27. — С. 1207. — doi:10.1063/1.1743956.
- ↑ Alder B. J., Wainwright T. E. Phase Transition in Elastic Disks // Phys. Rev.. — 1962. — № 127. — С. 359. — doi:10.1103/PhysRev.127.359.
- ↑ Hoover W. G., Gray S. G., Johnson K. W. Thermodynamic Properties of the Fluid and Solid Phases for Inverse Power Potentials // J. Chem. Phys.. — 1971. — № 55. — С. 1128. — doi:10.1063/1.1676196.
- ↑ Пайнс Д. Элементарные возбуждения в твёрдых телах. М., Мир, 1965.
- ↑ Андреев В. Д. Крэш (crash)-конформационная кинематика ковалентной решетки алмаза при плавлении. // Журнал структурной химии. — 2001. — № 3. — С. 486—495.
- ↑ Андреев В. Д. «Фактор плавления» при межатомных взаимодействиях в алмазной решетке. // Химическая физика. — 2002. — № 8,т.21. — С. 35—40.
Температура плавления цветных и черных металлов
В металлургической промышленности одним из основных направлений считается литье металлов и их сплавов по причине дешевизны и относительной простоты процесса. Отливаться могут формы с любыми очертаниями различных габаритов, от мелких до крупных; это подходит как для массового, так и для индивидуального производства.

Литье является одним из древнейших направлений работы с металлами, и начинается примерно с бронзового века: 7−3 тысячелетия до н. э. С тех пор было открыто множество материалов, что приводило к развитию технологии и повышению требований к литейной промышленности.
В наши дни существует много направлений и видов литья, различающихся по технологическому процессу. Одно остается неизменным — физическое свойство металлов переходить из твердого состояния в жидкое, и важно знать то, при какой температуре начинается плавление разных видов металлов и их сплавов.
Процесс плавления металла
 Данный процесс обозначает собой переход вещества из твердого состояния в жидкое. При достижении точки плавления металл может находиться как в твердом, так и в жидком состоянии, дальнейшее возрастание приведет к полному переходу материала в жидкость.
Данный процесс обозначает собой переход вещества из твердого состояния в жидкое. При достижении точки плавления металл может находиться как в твердом, так и в жидком состоянии, дальнейшее возрастание приведет к полному переходу материала в жидкость.
То же самое происходит и при застывании — при достижении границы плавления вещество начнет переходить из жидкого состояния в твердое, и температура не изменится до полной кристаллизации.
При этом следует помнить, что данное правило применимо только для чистого металла. Сплавы не имеют четкой границы температур и совершают переход состояний в некотором диапазоне:
- Солидус — линия температуры, при которой начинает плавиться самый легкоплавкий компонент сплава.
- Ликвидус — окончательная точка плавления всех компонентов, ниже которой начинают появляться первые кристаллы сплава.
Точно измерить температуру плавления таких веществ невозможно, точкой перехода состояний указывается числовой промежуток.
В зависимости от температуры, при которой начинается плавление металлов, их принято разделять на:
- Легкоплавкие, до 600 °C. К ним относятся олово, цинк, свинец и другие.
- Среднеплавкие, до 1600 °C. Большинство распространенных сплавов, и такие металлы как золото, серебро, медь, железо, алюминий.
- Тугоплавкие, свыше 1600 °C. Титан, молибден, вольфрам, хром.
Также существует и температура кипения — точка, при достижении которой расплавленный металл начнет переход в газообразное состояние. Это очень высокая температура, как правило, в 2 раза превышающая точку расплава.
Влияние давления
 Температура плавления и равная ей температура затвердевания зависят от давления, возрастая с его повышением. Это обусловлено тем, что при повышении давления атомы сближаются между собой, а для разрушения кристаллической решетки их нужно отдалить. При повышенном давлении требуется большая энергия теплового движения и соответствующая ей температура плавления увеличивается.
Температура плавления и равная ей температура затвердевания зависят от давления, возрастая с его повышением. Это обусловлено тем, что при повышении давления атомы сближаются между собой, а для разрушения кристаллической решетки их нужно отдалить. При повышенном давлении требуется большая энергия теплового движения и соответствующая ей температура плавления увеличивается.
Существуют исключения, когда температура, необходимая для перехода в жидкое состояние, при повышенном давлении уменьшается. К таким веществам относят лёд, висмут, германий и сурьма.
Таблица температур плавления
Любому человеку, связанному с металлургической промышленностью, будь то сварщик, литейщик, плавильщик или ювелир, важно знать температуры, при которых происходит расплав материалов, с которыми он работает. В нижеприведенной таблице указаны точки плавления наиболее распространенных веществ.
Таблица температур плавления металлов и сплавов
| Название | T пл, °C |
|---|---|
| Алюминий | 660,4 |
| Медь | 1084,5 |
| Олово | 231,9 |
| Цинк | 419,5 |
| Вольфрам | 3420 |
| Никель | 1455 |
| Серебро | 960 |
| Золото | 1064,4 |
| Платина | 1768 |
| Титан | 1668 |
| Дюралюминий | 650 |
| Углеродистая сталь | 1100−1500 |
| Чугун | 1110−1400 |
| Железо | 1539 |
| Ртуть | -38,9 |
| Мельхиор | 1170 |
| Цирконий | 3530 |
| Кремний | 1414 |
| Нихром | 1400 |
| Висмут | 271,4 |
| Германий | 938,2 |
| Жесть | 1300−1500 |
| Бронза | 930−1140 |
| Кобальт | 1494 |
| Калий | 63 |
| Натрий | 93,8 |
| Латунь | 1000 |
| Магний | 650 |
| Марганец | 1246 |
| Хром | 2130 |
| Молибден | 2890 |
| Свинец | 327,4 |
| Бериллий | 1287 |
| Победит | 3150 |
| Фехраль | 1460 |
| Сурьма | 630,6 |
| карбид титана | 3150 |
| карбид циркония | 3530 |
| Галлий | 29,76 |
Помимо таблицы плавления, существует много других вспомогательных материалов. Например, ответ на вопрос, какова температура кипения железа лежит в таблице кипения веществ. Помимо кипения, у металлов есть ряд других физических свойств, как прочность.
Прочность металлов
 Помимо способности перехода из твердого в жидкое состояние, одним из важных свойств материала является его прочность — возможность твердого тела сопротивлению разрушению и необратимым изменениям формы. Основным показателем прочности считается сопротивление возникающее при разрыве заготовки, предварительно отожженной. Понятие прочности не применимо к ртути, поскольку она находится в жидком состоянии. Обозначение прочности принято в МПа — Мега Паскалях.
Помимо способности перехода из твердого в жидкое состояние, одним из важных свойств материала является его прочность — возможность твердого тела сопротивлению разрушению и необратимым изменениям формы. Основным показателем прочности считается сопротивление возникающее при разрыве заготовки, предварительно отожженной. Понятие прочности не применимо к ртути, поскольку она находится в жидком состоянии. Обозначение прочности принято в МПа — Мега Паскалях.
Существуют следующие группы прочности металлов:
- Непрочные. Их сопротивление не превышает 50МПа. К ним относят олово, свинец, мягкощелочные металлы
- Прочные, 50−500МПа. Медь, алюминий, железо, титан. Материалы этой группы являются основой многих конструкционных сплавов.
- Высокопрочные, свыше 500МПа. Например, молибден и вольфрам.
Таблица прочности металлов
| Металл | Сопротивление, МПа |
|---|---|
| Медь | 200−250 |
| Серебро | 150 |
| Олово | 27 |
| Золото | 120 |
| Свинец | 18 |
| Цинк | 120−140 |
| Магний | 120−200 |
| Железо | 200−300 |
| Алюминий | 120 |
| Титан | 580 |
Наиболее распространенные в быту сплавы
 Как видно из таблицы, точки плавления элементов сильно разнятся даже у часто встречающихся в быту материалов.
Как видно из таблицы, точки плавления элементов сильно разнятся даже у часто встречающихся в быту материалов.
Так, минимальная температура плавления у ртути -38,9 °C, поэтому в условиях комнатной температуры она уже в жидком состоянии. Именно этим объясняется то, что бытовые термометры имеют нижнюю отметку в -39 градусов Цельсия: ниже этого показателя ртуть переходит в твердое состояние.
Припои, наиболее распространенные в бытовом применении, имеют в своем составе значительный процент содержания олова, имеющего точку плавления 231.9 °C, поэтому большая часть припоев плавится при рабочей температуре паяльника 250−400°C.
Помимо этого, существуют легкоплавкие припои с более низкой границей расплава, до 30 °C и применяются тогда, когда опасен перегрев спаиваемых материалов. Для этих целей существуют припои с висмутом, и плавка данных материалов лежит в интервале от 29,7 — 120 °C.
Расплавление высокоуглеродистых материалов в зависимости от легирующих компонентов лежит в границах от 1100 до 1500 °C.
Точки плавления металлов и их сплавов находятся в очень широком температурном диапазоне, от очень низких температур (ртуть) до границы в несколько тысяч градусов. Знание этих показателей, а так же других физических свойств очень важно для людей, которые работают в металлургической сфере. Например, знание того, при какой температуре плавится золото и другие металлы пригодятся ювелирам, литейщикам и плавильщикам.
| Полиолефины (полиэтилен, полипропилен) | |||||
|---|---|---|---|---|---|
| Полиэтилен высокого давления (низкой плотности) ГОСТ 16337 | 900-939 | 105-108 | 80-90 | -70 | -50…70 |
| Полиэтилен низкого давления (высокой плотности) ГОСТ 16338 | 948-959 | 125-135 | 128-134 | -60 | -60…100 |
| Высокопрочный полиэтилен низкого давления (ТУ 6-05-1721-75) | 942-957 | 125-135 | 125-140 | -140 | — |
| Высокомолекулярный полиэтилен низкого давления (ТУ 6-05-50-76) | 935 | — | 140 | -150 | — |
| Модифицированный полиэтилен низкого давления (ТУ 6-05-55-76) | 937-943 | — | 120-125 | — | — |
| Полипропилен (ТУ 6-05-11-05-73) | 900-910 | 164-170 | 95-100 | -15…-8 | — |
| Блоксополимер пропилена с этиленом (ТУ 6-05-1756-76) | 910 | 164-170 | 140-145 | — | — |
| Сополимер этилена с пропиленом низкого давления (ТУ 6-05-529-76) | 907-913 | — | — | -140 | — |
| Сэвилин — сополимер этилена с винилацетатом (ТУ 6-05-1636-73) | 920-959 | — | 30-95 | -75…-60* | — |
| Кабельный полиэтилен (ТУ 6-05-475-73) | 921 | — | 105-120 | -60 | — |
| Композиция самозатухающая на основе полиэтилена (ТУ 6-05-1445-72) | 1000 | — | 80 | -50 | — |
| Композиции полиэтилена низкой плотности с наполнителями (ТУ 6-05-1409-74) | 940-1100 | — | 80-92 | -60…-30 | — |
| Композиции на основе поли-4-метил-1-пентена (темплена) (ТУ 6-05-589-77) | 830-834 | 190-210 | 150-180 | -60* | — |
| Термостойкие окрашенные композиции на основе темплена (ТУ 6-05-637-77) | — | 200-210 | 170-180 | -60* | — |
| Композиция темплена с повышенной диэлектрической проницаемостью (ТУ 6-05-583-75) | 1800-2000 | — | 220 | -40* | — |
| Полипропиленовая пленка (ТУ 6-05-360-72, ТУ 6-05-469-77, ТУ 38-10524-73) | 890-910 | — | — | — | -50…120 |
| Полистирол и пластмассы на его основе | |||||
| Полистиролы общего назначения | 1050-1100 | — | 82-95 | -40* | до 65 |
| Полистирол ударопрочный (ОСТ 6-05-406-75) | 1060 | — | 85-95 | -40 | — |
| Полистирол вспенивающийся (ОСТ 6-05-202-73) | 20-30 | — | — | -65…-60* | до 70 |
| АБС-пластики (ТУ 6-05-1587-74) | 1030-1050 | — | 95-117 | -60…-40 | — |
| АБС-пластик СНП (ГОСТ 13077) | 1140 | — | 103 | — | -40…70 |
| Полистирол оптический и светотехнический (ТУ 6-05-1728-75) | 1050-1080 | — | 82-100 | — | -40…65 |
| Сополимеры стирола САН (ТУ 6-05-1580-75) | 1000-1040 | — | 96-108 | -60 | до 75 |
| Сополимер стирола САМ-Э | 1050-1170 | — | — | -60 | до 90 |
| Сополимеры стирола МС и МСН (ГОСТ 12271) | 1120-1140 | — | 86-88 | — | -40…70 |
| Сополимер стирола ударопрочный МСП (ТУ 6-05-626-76) | 1100 | — | 95-105 | — | — |
| Ударопрочные полистирольные пластики СНК и УПМ (ТУ 6-05-041-528-74) | 1050-1080 | — | 70-80 | — | до 70 |
| Пресс-материал 390 (ТУ 84-89-75) 46 и 46а (ТУ 84-142-70) | 1100-1300 | — | — | — | -60…60 |
| Материал АТ-1 (МРТУ 6-05-1197-69) и АТ-2 | 1150-1300 | — | 100-102 | — | -40…70 |
| Композиция стилон (ТУ 6-05-478-73) | 1100 | — | 125-130 | — | — |
| Пленка полистирольная (ГОСТ 12998) | 1050 | — | 95-100 | — | -50…70 |
| Высокочастотный диэлектрик стиролинк | 1200 | — | — | — | -60…100 |
| Фольгированный материал СА-3,8Ф (ТУ 16-503-108-72) | 1800 | — | 120 | — | -60…90 |
| Листовой самозатухающий материал АБС-090ЗС (ТУ 6-05-572-75) | — | — | 80 | -60* | — |
| Пенопласт полистирольный ПС-1 (ТУ 6-05-1178-75) | 70-600 | — | — | — | -60…65 |
| Пенопласт полистирольный ПС-4 (ТУ 6-05-1178-75) | 40-65 | — | — | — | -65…70 |
| Фторопласты | |||||
| Фторопласт-3 (ГОСТ 13744) | 2090-2160 | 210-215 | — | — | -195…130 |
| Фторопласт-4 (ПТФЭ или тефлон ГОСТ 10007) | 2190-2200 | 327 | 100-110 | — | -269…260 |
| Фторопласт-4Д (ГОСТ 14906) | 2210 | 327 | — | — | -269…260 |
| Фторопласт-4ДПТ (ТУ 6-05-372-77) | 2200-2230 | — | — | — | -269…260 |
| Фторопласт-4МБ (ОСТ 6-05-400-74) | 2140-2170 | 270-290 | 100-120 | — | -190…205 |
| Фторопласт-4НА (ТУ 6-05-373-77) | 2000-2100 | 210-230 | 90-120 | — | -200…200 |
| Фторопласт-23 (ТУ 6-05-1706-74) | 1740 | 130 | — | — | -60…200 |
| Фторопласт-26 (ТУ 6-05-1706-74) | 1790 | — | — | — | -60…250 |
| Фторопласт-30П, 30А (ТУ 6-05-1706-74) | 1670 | 215-235 | — | — | -198…170 |
| Фторопласт-32Л (ТУ 6-05-1620-73) | 1920-1950 | 105 | — | — | -60…200 |
| Фторопласт-40 (ОСТ 6-05-402-74) | 1650-1700 | 260-275 | 140-143 | — | -100…200 |
| Фторопласт-40Д и 40ДП (ТУ 6-05-1706-74) | 1650-1700 | 265 | — | — | -100…200 |
| Фторопласт-40Б (ТУ 6-05-501-74) | 1650-1700 | 260-265 | — | — | -60…200 |
| Фторопласт-40ШБ (ТУ 6-05-383-72) | 1650 | — | 140 | — | -60…200 |
| Фторопласт-2 (ТУ 6-05-646-77) | 1700-1800 | 170-180 | 140-160 | — | -60…150 |
| Фторопласт-2М (ТУ 6-05-1781-76) | 1750-1800 | 155-165 | 120-145 | — | -60…145 |
| Фторопласт-45 (ТУ 6-05-1442-71) | 1910-2000 | 150-160 | 97-105 | — | -60…120 |
| Фторопласт-1 (ТУ 6-05-559-74) | 1380-1400 | 196-204 | 120 | — | -80…200 |
| Фторопласт-10Б и 100Б | 2100 | — | — | — | -100…150 |
| Фторопласт-400 | 1700 | — | — | — | -60…150 |
| Композиция Ф40С15 (ТУ 6-05-606-75) | — | 265-275 | — | — | — |
| Композиция Ф4К20 (ТУ 6-05-1412-76) | 2100-2120 | — | — | — | -60…250 |
| Композиция Ф4С15 (ТУ 6-05-1412-76) | 2170-2180 | — | — | — | -60…250 |
| Композиция Ф4К15М5 (ТУ 6-05-1412-76) и Ф4С15М5 | 2190 | — | — | — | -60…250 |
| Композиция Ф4М15 | 2250 | — | — | — | -60…260 |
| Композиция Ф4Г21М7 | 2100-2300 | — | — | — | -100…250 |
| Антифрикционный материал Ф40Г40 | 1700-1800 | — | — | — | -60…200 |
| Антифрикционный материал Ф40С15М1,5 | 1800 | — | — | — | -100…210 |
| Антифрикционный графитофторопластовый материал 7В-2А | 1900-200 | — | — | — | до 250 |
| Антифрикционный графитофторопластовый материал АФГМ | 2100-2300 | — | — | — | до 180 |
| Антифрикционный графитофторопластовый материал АФГ-80ВС и 80ФГ | 2050-2100 | — | — | — | до 200 |
| Антифрикционный графитофторопластовый материал ГФ-5М | 2100-2200 | — | — | — | до 180 |
| Пленка из фторопласта-10 (ТУ 6-05-538-77) | 2100 | — | — | — | -100…100 |
| Пленка фторопластовая Ф-4 | 2200-2300 | — | — | — | -60…200 |
| Пленка фторопластовая Ф-4ЭО, Ф-4ИО, Ф-4ИН и Ф-4ЭН | 2100-2200 | — | — | — | -60…250 |
| Поливинилхлорид (ПВХ) и пластмассы на его основе | |||||
| Винипласт листовой (ГОСТ 9639) | 1380 | — | 70-85 | -75 | — |
| Изоляционные пластикаты И40-13, И50-13, И60-12, ИТ-105 (ГОСТ 5960) | 1180-1340 | — | 170-190 | -60…-40 | — |
| Винипроз и эстепроз (ТУ 6-05-1222-75) | 1350-1400 | — | — | — | -35…60 |
| Пенопласт ПВХ-1, ПВХ-2 | 70-300 | — | — | — | -60…60 |
| Пенопласт ПВХ-1, ПВХ-2 | 50-400 | — | — | — | -70…70 |
| Пенопласт ПВХ-Э | 100-270 | — | — | — | -10…40 |
| Пеноэласт | 80-300 | — | — | — | -20…70 |
| Винипор С, Д, М | 90-180 | — | — | — | -10…55 |
| Вибропоглощающий материал ВМЛ-25 (ТУ 6-05-980-75) | 1500-1600 | — | — | — | -10…50 |
| Пленка винипластовая (ГОСТ 16389, ГОСТ 15976) | 1370-1450 | — | — | — | -50…60 |
| Поливинилацетат | 1190 | — | 44-50 | -5* | — |
| Поливинилформаль (ГОСТ 10758) | 1240 | — | 115-120 | — | — |
| Поливинилбутираль (ГОСТ 9439) | 1100 | — | 60-75 | — | — |
| Поливинилэтилаль (ТУ 6-05-564-74) | 1350 | — | 118-120 | — | — |
| Поливинилформальэтилаль (ГОСТ 10400) | 1200 | — | 120 | — | — |
| Поливинилбутиральфурфураль (ТУ 6-05-1102-74) | 1055 | — | 70-85 | — | — |
| Поливинилкеталь | 1180 | — | 105-115 | — | — |
| Пленка ПВС-Э, ПВС | 1200-1300 | — | — | — | -5…130 |
| Поливинилбутиральные пленки А-17, Б-Н, Б-10, Б-17, Б-17-О (ГОСТ 9438) | 1050-1100 | — | — | — | -60…150 |
| Полиакрилаты | |||||
| Полиметилметакрилат литьевой ЛПТ (ТУ 6-05-952-74) | 1180-1200 | — | 120-125 | -50* | -60…60 |
| Дакрил-2М ( ТУ 6-01-707-72) | 1190 | — | 110 | — | — |
| Компаунд МБК-1 (ТУ 6-05-1602-71) | 1600 | — | — | — | -60…105 |
| Герметики ДН-1 и Анатерм-1, 2, 4, 5, 6, 7 | 1050-1200 | — | — | — | до 150 |
| Герметик Унигерм | 1050-1200 | — | — | — | -185…200 |
| Стекло органическое СОЛ (ГОСТ 15809) | 1180 | — | 90 | — | -60…60 |
| Оргстекло СТ-1 (ГОСТ 15809) | 1180 | — | 110 | — | -60…80 |
| Оргстекло 2-55 (ГОСТ 15809) | 1190 | — | 133 | — | -60…100 |
| Стекло органическое ТОСП (ГОСТ 17622) | 1180 | — | 90 | — | — |
| Оргстекло ТОСН (ГОСТ 17622) | 1180 | — | 105-110 | — | — |
| Оргстекло ТОСС (ГОСТ 17622) | 1180 | — | 125-130 | — | — |
| Полиарилаты | |||||
| Полиарилаты Д-3, Д-4, Д-3Э ( ТУ 6-05-211-834-72) | 1150-1190 | 260-285 | 210 | -100* | до 180 |
| Полиарилат Д-4С (ТУ 6-05-818-72) | 1210 | 255-280 | 210 | -100* | до 180 |
| Полиарилат Ф1 | 1110-1260 | 300-310 | 268 | -100* | до 200 |
| Полиарилат Ф2 | 1100-1170 | 320-340 | 280 | -100* | до 250 |
| Антифрикционный пластик Аман-1 | 3600 | — | — | — | до 220 |
| Антифрикционный пластик Аман-2 | 3700 | — | — | — | до 180 |
| Антифрикционный пластик Аман-7 | 2500 | — | — | — | до 120 |
| Антифрикционный пластик Аман-10 | 2500 | — | — | — | до 200 |
| Антифрикционный пластик Аман-12 | 3000 | — | — | — | до 300 |
| Антифрикционный пластик Аман-22 | 3700 | — | — | — | до 250 |
| Антифрикционный пластик Аман-24 | 3200 | — | — | — | до 250 |
| Полиарилатная пленка Д-4П (ТУ 6-05-823-72) | — | — | — | — | -60…180 |
| Полиарилатная пленка ДФ-55П и Ф-2П (ТУ 6-05-823-72) | — | — | — | — | -60…250 |
| Полиарилатная пленка Д-3Э (ТУ 6-05-834-72) | — | — | — | — | -60…155 |
| Фенопласты | |||||
| Фенопласт О6-010-02 (ГОСТ 5689) и К-18-2 (ТУ 6-05-480-72) | 1400 | — | — | — | -60…60 |
| Фенопласт О7-010-02 (ГОСТ 5689) | 1450 | — | — | — | -50…110 |
| Фенопласты СП1-342-02, СП2-342-02 (ГОСТ 5689) | 1400 | — | — | — | -60…60 |
| Фенопласты Э1-340-02, Э2-330-02 (ГОСТ 5689) | 1400 | — | — | — | -60…100 |
| Фенопласт Э3-340-65, Э3-340-61 (ГОСТ 5689) | 1950 | — | — | — | -60…115 |
| Фенопласт Э6-014-30 (ГОСТ 5689) | 1850 | — | — | — | -60…220 |
| Фенопласт В-4-70 (ГОСТ 5.1958) | 2000 | — | — | — | -60…150 |
| Фенопласт влагохимстойкий ВХ-090-34 (ГОСТ 5689) | 1600 | — | — | — | -40…110 |
| Фенопласт влагохимстойкий ВХ4-080-34 (ГОСТ 5689) | 1750 | — | — | — | -60…200 |
| Фенопласты ударопрочные У1-301-07, У2-301-07, У3-301-07 (ГОСТ 5689) | 1450 | — | — | — | -40…110 |
| Фенопласты ударопрочные У5-301-41, У6-301-41 | 1950 | — | — | — | -40…130 |
| Фенопласты жаростойкие Ж1-010-40, Ж2-040-60, Ж3-010-62, Ж4-010-62 | 1750-1900 | — | — | — | -40…120 |
| Фенопласт жаростойкий Ж2-010-60 (ГОСТ 5689) | 1750 | — | — | — | -40…130 |
| Антифрикционный пластик АФ-3Т ( ТУ 26-01-55-1-73) | 1760-1800 | — | — | — | -70…250 |
| Пресс-материал АТМ-1 (антегмит) | 1800-1850 | — | — | — | до 115** |
| Пресс-материал АТМ-1К (антегмит) | 1800-1850 | — | — | — | до 300** |
| Изодин (ТУ 16-503-013-74) | 1350-1450 | — | — | — | до 120** |
| Пластик ПГТ (ТУ 16-503-023-75) | 1300-1450 | — | — | — | -60…105 |
| Текстолит конструкционный ПТК, ПТ, ПТМ-1 (ГОСТ 5-72) | 1300-1400 | — | — | — | до 130** |
| Текстолит электротехнический листовой А, Б, Г, ВЧ (ГОСТ 2910) | 1300-1450 | — | — | — | -65…105 |
| Текстолит электротехнический листовой ЛЧ (ГОСТ 2910) | 1250-1350 | — | — | — | -65…120 |
| Текстолит электротехнический листовой влагостойкий ЛТ (ТУ 16-503.149-75) | 1200-1350 | — | — | — | -65…65 |
| Пенофенопласт ФФ (МРТУ 6-05-1302-70) | 190-230 | — | — | — | -50…150 |
| Пенофенопласт ФК-20 (МРТУ 6-05-1302-70) | 190-230 | — | — | — | -60…120 |
| Звуконепроницаемая теплоизоляция ФС-7-2 (ТУ 6-05-958-73) | 70-100 | — | — | — | -55…100 |
| Пенофенопласт ФК-20-А-20 (ТУ 6-05-1303-70) | 140-200 | — | — | — | до 250 |
| Пенопласт Резопен (ТУ В-302-71), Виларес-1, Виларес-5 | 30-80 | — | — | — | -150…150 |
| Пенопласт ФРП-2М (ТУ 6-05-304-74) | 100 | — | — | — | -180…200 |
| Пенопласт ФЛ-1, ФЛ-2 | 40-60 | — | — | — | -60…120 |
| Карбамидные пресс-материалы (композиты и аминопласты) | |||||
| Аминопласты А1 и А2 (ГОСТ 9359) | 1400-1500 | — | — | — | -60…60 |
| Аминопласт В1 (ГОСТ 9359) | 1600-1800 | — | — | — | -60…120 |
| Аминопласт В5 (ГОСТ 9359) | 1600-1850 | — | — | — | -60…60 |
| Пресс-материал П-1-1 | 1480 | — | — | — | -60…100 |
| Пенопласты мочевиноформальдегидные МФП-1 и МФП-2 (ТУ 6-05-206-73) | 10-30 | — | — | — | -60…100 |
| Пресс-материалы на основе кремнийорганических смол | |||||
| Пресс-материалы КФ-9 и КФ-10 (ТУ 6-05-1471-71) | 1500-1650 | — | — | — | -60…250 |
| Пресс-материалы КЭП-1 и КЭП-2 | 1500-1800 | — | — | — | -60…200 |
| Антифрикционный пластик АМС-1 (ТУ 48-20-45-74) | 1740-1760 | — | — | — | -60…210 |
| Антифрикционный пластик АМС-3 (ТУ 48-20-45-74) | 1780-1800 | — | — | — | -200…210 |
| Органосиликатный материал Группа А марка 1 и 4 | — | — | — | — | -60…500 |
| Органосиликатный материал Группа Т марка 11 | — | — | — | — | -60…700 |
| Пенопласт К-40 | 200-400 | — | — | — | до 250 |
| Полиэфиры | |||||
| Полиэтилентерефталат (ПЭТ, лавсан, майлар) (ТУ 6-05-830-76) | 1320 | — | 160-180 | — | — |
| Лавсан ЛС-1 | 1530 | — | 190 | — | — |
| Пленка полиэтилентерефталатная (ПЭТФ) аморфная (ТУ 6-05-1454-71) | 1330-1340 | 260-264 | — | — | до 60 |
| Пленка ПЭТФ общего назначения (ТУ 6-05-1065-76) | 1380 | 260 | — | — | -60…155 |
| Пленка ПЭТФ электроизоляционная (ТУ 6-05-1794-76) | 1380 | 260-264 | — | — | -150…156 |
| Пленка ПЭТФ конденсаторная (ТУ 6-05-1099-76) | 1380-1400 | 250 | — | -60* | -60…125 |
| Пленка ПЭТФ для металлизации (ТУ 6-05-1108-76) | 1380 | 260-264 | — | — | — |
| Эпоксидные смолы и компаунды | |||||
| Заливочный компаунд ЭЗК-1 и ЭЗК-4 | 1800-1850 | — | — | — | -60…120 |
| Эпоксидный заливочный компаунд ЭЗК-6 | 1220 | — | — | — | -60…80 |
| Заливочный компаунд ЭЗК-5 | 1520 | — | — | — | -50…70 |
| Заливочный компаунд ЭЗК-11 | 1100 | — | — | — | -60…120 |
| Заливочный компаунд ЭЗК-12 | 1500 | — | — | — | -60…100 |
| Заливочный компаунд ЭЗК-7 | 1600 | — | — | — | -60…80 |
| Заливочный компаунд ЭЗК-8 | 1450 | — | — | — | -60…70 |
| Компаунд ЭК-20 | 1160-1200 | — | — | — | -60…150 |
| Пропиточный компаунд ЭПК-1 и ЭПК-4 | 1230 | — | — | — | -60…120 |
| Компаунд УП-5-186 (ТУ 6-05-87-74) | — | — | 190-210 | — | -60…100 |
| Компаунд УП-5-187 (ТУ 6-05-87-74) | — | — | 200-230 | — | -60…100 |
| Пастообразный компаунд УП-5-190 (ТУ 6-05-95-75) | 2700-2900 | — | — | — | -50…180 |
| Компаунд ЭНТ-2 | 2200 | — | 250-300 | — | — |
| Компаунд ЭНКП-2 | 1800 | — | 150-180 | — | — |
| Компаунд ЭНГ-30 | 1290 | — | 125-135 | — | — |
| Компаунд ЭНМ-25 | 1320 | — | 125-135 | — | — |
| Пресс-материал УП-264С (ТУ 6-05-22-73) | 1650 | — | 155-165 | — | -60…150 |
| Пресс-материал УП-264П (ТУ 6-05-22-73) | 1900-2200 | — | 160-165 | — | -60…150 |
| Пресс-материал УП-284С (ТУ 6-05-70-73) | 1670-1710 | — | 180-200 | — | -60…180 |
| Пресс-материал УП-2198 (ТУ 6-05-94-75) | — | — | — | — | -60…105 |
| Пресс-материал УП-2197 | 1700-1900 | — | — | — | -60…230 |
| Премиксы ЭФП-60, ЭФП-61, ЭФП-62 | 1700-1800 | — | — | — | -60…155 |
| Премиксы ЭФП-64, ЭФП-65 | 1800-2300 | — | — | — | -60…155 |
| Пенопласт ПЭ-2 (ТУ В-172-70) | 90-450 | — | — | — | -60…140 |
| Пенопласт ПЭ-5 (ТУ 6-05-215-71) | 100-300 | — | — | — | -60…120 |
| Пенопласт ПЭ-6 (ТУ 6-05-215-71) | 20-50 | — | — | — | -60…100 |
| Пенопласт ПЭ-7 (ТУ 6-05-289-73) | 23-60 | — | — | — | -60…100 |
| Пенопласт ПЭ-8 (ТУ В-171-70) | 150-500 | — | — | — | -60…120 |
| Пенопласт ПЭ-9 (ТУ В-173-70) | 100-500 | — | — | — | -60…90 |
| Полиамиды | |||||
| Полиамид-6 (капролон) ОСТ 6-06-С9-76 | 1130 | 215 | 190-200 | — | — |
| Смола капроновая литьевая (ТУ 6-06-390-70) | 1130 | 215 | — | — | — |
| Полиамид 610 литьевой (ГОСТ 10589) | 1090-1110 | 215-221 | 200-220 | — | -60…100 |
| Полиамид П-66 литьевой (анид) (ОСТ 6-06-369-74) | 1140 | 252-260 | 210-220 | — | — |
| Полиамид литьевой П-12Л (ТУ 6-05-1309-72) | 1020 | 178-181 | 140 | -55…-50 | — |
| Полиамид П-12Б (ТУ 6-05-145-72) | 1020 | 170 | 140 | -50 | — |
| Полиамид экструзионный П-12Э (ТУ 6-05-147-72) | 1020 | 178-182 | 140 | -60 | — |
| Капролон В (ТУ 6-05-983-73) | 1150-1160 | 220-225 | 190-220 | — | -60…60 |
| Капролит РМ | 1200 | — | 220 | — | — |
| Литьевой сополимер полиамида АК-93/7 (ГОСТ 19459) | 1140 | 238-243 | 220-230 | — | — |
| Литьевой сополимер полиамида АК-85/15 (ГОСТ 19459) | 1130 | 224-230 | 210-220 | — | — |
| Литьевой сополимер полиамида АК-80/20 (ГОСТ 19459) | 1130 | 212-218 | 200-210 | — | — |
| Смола полиамидная П-54 и П-54/10 (ТУ 6-05-1032-73) | 1120 | 160-165 | 115-135 | -40* | — |
| Смола полиамидная П-548 (ТУ 6-05-1032-73) | 1120 | 150 | 85 | -50* | — |
| Материал АТМ-2 (ТУ 6-05-502-74) | 1390 | 218-220 | — | — | -50…60 |
| Антифрикционный материал ЛАМ-1 (ТУ 26-404-74) | — | 235 | — | — | -60…165 |
| Полиуретаны | |||||
| Пенополиуретан ППУ-ЭМ-1 (ТУ 6-05-1473-76) | 30-50 | — | — | — | -50…100 |
| Пенополиуретан ППУ-202-1 (ТУ 6-05-234-72) | 55-85 | — | — | — | до 100 |
| Пенополиуретан ППУ-ЭФ-1, ППУ-ЭФ-2, ППУ-ЭФ-3 | 19-38 | — | — | — | -40…100 |
| Пенополиуретан ППУ-305А (ТУ 6-05-121-74) | 35-500 | — | 120 | — | — |
| Пенополиуретан ППУ-307 (ТУ 6-05-251-72) | 35-220 | — | 130-150 | — | — |
| Пенополиуретан ППУ-311 (ТУ 6-05-221-72) | 30-60 | — | 150 | — | — |
| Пенополиуретан ППУ-313-2, ППУ-312-3 | 35-45 | — | 120-150 | — | — |
| Пенополиуретан ППУ-314 (ТУ 6-05-279-73) | 20-300 | — | 80-100 | — | — |
| Пенополиуретан ППУ-403 (ТУ 6-05-252-72) | 75-200 | — | 120 | — | — |
| Пенополиуретан ППУ-202-1 (ТУ 6-05-234-72) | 200-250 | — | — | — | -60…100 |
| Пенополиуретан ППУ-202-2 (ТУ 6-05-229-72) | 130-250 | — | — | — | -60…100 |
| Пенополиуретан ППУ-3Н, ППУ-9Н | 50-80 | — | 70-75 | — | — |
| Пенополиуретан ППУ-304Н | 30-200 | — | 120 | — | — |
| Пенополиуретан ППУ-308Н | 40-200 | — | 150 | — | — |
| Этролы | |||||
| Этролы ацетилцеллюлозные АЦЭ-43А, АЦЭ-55А (ТУ 6-05-1528-72) | 1270-1340 | — | 65-85 | — | — |
| Этрол ацетилцеллюлозный АЦЭ-47ТВ (ТУ 6-05-268-73) | 1270-1340 | — | 65-85 | — | — |
| Этрол ацетилцеллюлозный АЦЭ-55АМ (ТУ 6-05-1528-72) | 1270-1340 | — | 70 | — | — |
| Этролы АЦЭ-55У, АЦЭ-50У, АЦЭ-50-20У, АЦЭ-50-5У (ТУ 6-05-268-73) | 1270-1340 | — | 90 | — | — |
| Этрол ацетобутиратцеллюлозный АБЦЭ-15АТ (ТУ 6-05-255-72) | 1160-1250 | — | 85 | — | — |
| Этрол ацетобутиратцеллюлозный АБЦЭ-7,5-5, АБЦЭ-10, АБЦЭ-15ДСМ-В | 1160-1250 | — | 80 | — | — |
| Этрол ацетобутиратцеллюлозный АБЦЭ-15 | 1160-1250 | — | 75-80 | — | — |
| Пленка электроизоляционная триацетатная (ТУ 6-17-499-73) | 1260 | — | — | — | -60…100 |
| Стеклопластики | |||||
| Стеклопластик АГ-4С-6 (ТУ 84-359-73) | 1900-2000 | — | — | — | -60…200 |
| Стеклопластик АГ-4В-10 (ТУ 84-438-74) | 1700-1900 | — | — | — | -60…130 |
| Термопласт стеклонаполненный САН-С (ТУ 6-05-369-76) | 1280-1320 | — | 115-120 | — | -40…120 |
| Полиамид П-6 стеклонаполненный ПА6ВС, ПА6ВС-У (ТУ 6-05-953-74) | 1350 | 212-216 | — | — | — |
| Смола капроновая стеклонаполненная КС-30а | 1360 | 214-221 | — | — | — |
| Полиамид стеклонаполненный КПС-30 и КВС-30 (ГОСТ 17648) | 1350-1380 | 214-221 | — | — | — |
| Дифлон СТН (ТУ 6-05-937-74) | 1400 | — | 170-172 | -100* | — |
| Стеклопластик ДАФ-С-2 | 2000-2150 | — | — | — | -60…180 |
| Стеклопластик ДАИФ-С1 и ДАИФ-С2 | 2200 | — | — | — | -60…250 |
| Стеклотекстолит листовой СТЭФ-НТ (ТУ 16-503.146-75) | 1600-1900 | — | — | — | -60…55 |
| Стеклотекстолит листовой СТ-НТ (ТУ 16-503.147-75) | 1600-1850 | — | — | — | -65…130 |
| Диэлектрик фольгированный ФДГ-1 и ФДГ-2 | — | — | — | — | -60…150 |
| Фольгированные травящиеся диэлектрики ФДМТ (ТУ 16-503.113-72) | 3000-4500 | — | — | — | -60…100 |
| Фольгированный диэлектрик ФДМ-1 | 2800-3400 | — | — | — | -60…100 |
| Фольгированный диэлектрик ФДМ-2 | 3500-4000 | — | — | — | -60…100 |
| Фольгированные диэлектрики ФДМЭ-1 и ФДМЭ-1-ОС | 2800-5100 | — | — | — | -60…105 |
| Пластики на основе формальдегида и диоксолана | |||||
| Сополимеры формальдегида с диоксоланом СФД (ТУ 6-05-1543-72) | 1390-1410 | 160-165 | 150-155 | — | -60…120 |
| Пентапласт | |||||
| Пентапласт (ТУ 6-05-1422-74) | 1400 | 180 | 155-165 | — | до 120 |
| Пентапласт кабельный И3 (ТУ 6-05-1693-74) | 1320-1330 | 170-172 | 123-127 | — | -25…125 |
| Пентапласт модифицированный | 1320 | 176 | 125 | -20 | — |
| Пентапласт футеровочный (ТУ 6-05-5-74) | 1350-1400 | — | 155-165 | — | — |
| Пленка пентапластовая (ТУ 6-05-453-73) | 1400 | — | — | — | -50…130 |
| Поликарбонаты | |||||
| Поликарбонат дифлон (ТУ 6-05-1668-74) | 1200 | — | 150-160 | — | -100…135 |
| Поликарбонат модифицированный ДАК-8 и ДАК-12-3BN (ОСТ 6-05-5018-73) | 1200 | — | 156-160 | — | — |
| Дифсан (ТУ 6-05-852-72) | 1320 | — | 155-160 | — | -100…120 |
| Поликарбонатная пленка ПКО (ТУ 6-05-865-73) | 1210 | — | — | — | -60…150 |
| Полиимиды | |||||
| Полиимид ПМ-67 | 1390-1460 | — | 280 | — | до 250 |
| Полиимид ПМ-69 | 1380-1470 | — | 280 | — | до 250 |
| Пленки ПМФ-351 и ПМФ-352 (ТУ 6-05-1754-76) | 1390-1420 | — | — | — | -60…200 |
| Полисульфон | |||||
| Полисульфон | 1250 | — | 180 | — | — |
| Пенопласты изолан | |||||
| Пенопласт изолан-1 | 35-400 | — | 200-250 | — | -60…200 |
| Пенопласт изолан-2 | 30-50 | — | 170 | — | -50…180 |
| Пресс-материал фенилон П и С1 (ТУ 6-05-101-71) | 1350 | — | 260-270 | — | — |
| Пресс-материал фенилон С2 (ТУ 6-05-226-72) | 1350 | — | 300 | — | — |
| Арилокс | |||||
| Арилокс-2101 (ТУ 6-05-416-76), 2102 (ТУ 6-05-415-76) | — | — | 180 | — | — |
| Арилокс-2103 (ТУ 6-05-417-76), 2104 (ТУ 6-05-421-76), 2105 (ТУ 6-05-423-77) | — | — | 130 | — | — |
| Арилокс-1Н (ТУ 6-05-402-75) | — | — | — | — | -60…150 |
| Фольгированный арилокс-1Н (ТУ 6-05-404-74) | — | — | — | — | -60…150 |
| Диэлектрик фольгированный флан (ТУ 16-503.148-75) | 1200-2600 | — | 190-200 | — | — |
| Ниплон | |||||
| Термостойкий пластик ниплон-1 (ТУ 6-05-998-75) | 1340 | — | 330-340 | — | до 300 |
| Термостойкий пластик ниплон-2 (ТУ 6-05-1001-75) | 1300 | — | — | — | до 300 |
| Стеклопластик ниплон-1 и ниплон-2 | 1800 | — | — | — | до 300 |
| Углепластик ниплон-1 и ниплон-2 | 1300 | — | — | — | до 300 |
таблица в градусах в зависимости от пробы, характеристики и свойства сплава, как расплавить дома
Платина — , считающийся драгоценным и податливым для обработки. Его название пришло из испанского языка, дословно переводится как мелкое серебро. В таблице Менделеева фигурирует под обозначением Pt. Элемент , различных сплавах и соединениях.
Температура плавления платины, тяжелый вес, твердость и устойчивость в условиях агрессивной среды делают металл незаменимым в различных областях жизни.
Характеристики и свойства платины
Платина обладает очень высокой плотностью. она занимает особое место и в весе уступает только не менее редким иридию и осмию.
В сравнении с золотом и серебром, имеет большую твердость. Именно это свойство позволяет платине быть устойчивой к механическим воздействиям.
Металл способен поглощать газы — водород и кислород. В некоторых состояниях эта способность усиливается. Особенно хорошо кислород абсорбируется платиновой чернью, которая получается в результате реакции солевых растворов на восстановители.
Характеристики:
- металл белого (иногда с оттенками серого) цвета, блестящий;
- кристаллическая решетка при 20 °C, нм а = 0,392;
- твердость равна МПа 390-420;
- удельное электросопротивление при 0 °C, мкОм•см 9,85;
- температура плавления, °С — 1773,5;
- температура кипения, °С — 4410;
- радиус атома, нм — 0,138;
- удельная теплоемкость, Дж/(моль/К) — 25,9;
- модуль упругости, ГПа — 173;
- теплопроводность при 25 °C, Вт/(м•К) — 74,1;
- плотность при 20 °C, кг/дм3 — 21,45.
Как происходит переработка платинового сырья
Металл очищается механически от инородных веществ. Затем наступает этап химической очистки, которая направлена на качественное улучшение и повышает свойства металла методом химической очистки от примесей.
На данном этапе очистки самородки нагреваются в крупных фарфоровых емкостях, куда добавляется царская водка. Этот процесс позволяет отделить неблагородные металлы, которые растворяются. Но выделяется также и неподдающийся растворению осадок с содержанием других элементов.
Осадки подвергаются фильтрации с последующей повторной обработкой царской водкой. Осмий и иридий, полученные в ходе этого процесса, в дальнейшем используются в промышленности, поэтому извлекаются из котлов.
В результате этих действий платина остается в двух комплексах:
Во второй комплекс вводится элемент под названием HCl. Именно он переводит (NO) 2[PtCl6] в первый комплекс. Так получается единый комплекс, в который входят палладий, осмий и иридий, относящиеся к благородным металлам. Их необходимо перевести в соединения (Ir3+, Pd2+), на которые не может влиять хлористый аммоний, чтобы элементы не выпали в осадок. Далее раствор изменяется прогревом с серной и щавелевой кислотами.
После ввода хлор-аммония платина попадает в осадок в виде гранул золотого цвета. Платина при этом остается в растворе. Извлеченный металл затем очищается нашатырем и просушивается.


Только после такого длительного процесса очистки платина готова к плавке.
При какой температуре плавится
Температурой плавления платины считается °С — 1773,5, однако существуют рекомендации плавки отдельных видов:
| Сплавы | Температура плавления | Пластичность | Удельный вес | Прочность |
| Pt850/ Ir | 1800—1820 °C | 15% | 21,5 | 160 HV |
| Pt900/ Ir | 1780—1800 °C | 20% | 21,5 | 110 HV |
| Pt950/ Ir | 1780—1790 °C | 30% | 21,45 | 80 HV |
| Pt 900/ Co30/ Pd70 | 1730°C – 1740 °C | 22% | 20,4 | 120 HV |
| Pt850/ Pd | 1730—1750 °C | 76 HV | ||
| Pt900/ Pd | 1740—1755 °C | 22% | 19,8 | 72 HV |
| Pt950/ Pd | 1755—1765 °C | 22% | 19,8 | 68 HV |
| Pt950/ Co | 1780—1765 °C | 20% | 20,8 | 135 HV |
| Pt960/ Cu | 1725—1745 °C | 29% | 20,0 | 108 HV |
| Pt950/ Co/ Cu | 1750—1760 °C | 22% | 20,1 | 120 HV |
| Pt950/ 15In/ 30Ga | 1550—1625 °C | 26% | 20,22 | 200 HV |
| Pt950/ Ru | 1780—1795 °C | 34% | 20,7 |
Какие металлы используются в платиновых сплавах, как они меняют температуру плавления
К платине часто добавляют другие металлы:
- вольфрам;
- иридий;
- кобальт;
- медь;
- галлий;
- палладий;
- рутений.
Они способные повысить его физические свойства, а также химические особенности. Это позволяет применять сплавы в более широких областях промышленности и науки.
Легирующие компоненты добавляются в платину в температурном диапазоне 1850—1901в градусах Цельсия.
Способы плавления и температура процесса
Для плавки платины используются тигли с футеровкой из оксида циркония, оксида кальция или магнезита. Как раскислитель нужны силикокальций или алюминий.
Иногда плавка ведется в печах из оксида тория. Такая необходимость возникает, когда требуется получить изделия без примесей кальция или магнезита.
Заливку платины ведут с незначительным перегревом расплава и заливают в известковые формы.
От состава сплава зависит и температура процесса (см. таблицу).
Можно ли расплавить платину в домашних условиях
Интересно, есть ли возможность плавки платины в домашних условиях — сразу оговорюсь, что приступать к таким действиям следует в том случае, если вы разбираетесь в теме! Методы самостоятельного плавления кустарны и порой небезопасны.
Получить чистый продукт без примесей в таких условиях практически невозможно, все способы плавки не идеальны. Лучше обратиться за помощью к специалисту.
Необходимое оборудование и материалы
Некоторые любители плавят платину с помощью собранных своими руками газовых горелок с использованием кислородных баллонов, кто-то делает это сварочным аппаратом. Необходим также фарфоровый тигель (горшочек для нагрева).
Подготовка шихты
В целом процесс подготовки не отличается от промышленного, разумеется, в рамках ваших возможностей, которые в условиях дома крайне ограничены.


Процесс плавки
Сплав помещается в тигель и накаляется газовой горелкой, сварочным инвертором или другими самодельными приспособлениями до достижения необходимой температуры.


Получение отливок
Отлитый металл бывает разного вида в зависимости от созданной формочки. Тут играют роль ваши предпочтения. Главное — дать платине остыть и пользоваться инструментами предосторожности.


Как удалить примеси в домашних условиях
Как правило, в домашних условиях сделать это почти невозможно. Напротив, у любителей получается множество примесей в связи с отсутствием опыта и профессионального оборудования.
Необходимо иметь хорошие знания в химии, чтобы суметь отделить нужный металл с помощью растворов.
На этом на сегодня все. Подписывайтесь на обновления в соцсетях и до встречи!
При какой температуре плавится алюминий
Инструкция по плавке алюминия в бытовых условиях
Алюминий используется в быту и промышленности на протяжении многих лет. Свойства материала позволяют создавать разнообразные изделия. Плавка алюминия может выполняться в домашних условиях, поскольку для этого не требуется высокая температура. Свойства металла нужно знать, чтобы правильно провести такую процедуру.
Характеристики
Чистота материалов определяет температуру их плавления. Алюминий пригоден для проведения разных технологических процедур, благодаря небольшому весу и хорошей пластичности. При высокой температуре происходит взаимодействие с кислородом. На поверхности металла возникает оксидная пленка, которая защищает его от коррозии и окисления. Плавление алюминия способствует изменению структуры вещества, поэтому защитное покрытие полезно для него. Усадка и дополнительное внутреннее напряжение появляется при резком охлаждении.
Особенности технологического процесса
Тигель — это тугоплавкая емкость для разогрева металла. Используются изделия из таких материалов:
В бытовых условиях применяется готовый тигель или емкость из широкой железной трубы. Чтобы изготовить ее, потребуется болгарка и сварочное оборудование. Объем тигля выбирается индивидуально, емкость прогревается равномерно, измельченный металл плавится в результате теплопередачи.
Перед термообработкой нужно уменьшить температуру плавления, чтобы состояние металла менялось быстрее. Для этого алюминий дробят на мелкие фрагменты. Воспламенение или окисление происходит часто после такого измельчения. Состояние образовавшегося оксида алюминия меняется при более высоких температурах. Это вещество удаляется вместе с другими шлаками после переплавки основного металла.

В процессе термообработки придется избегать попадания жидкости в тигель. Резкое испарение воды становится причиной взрыва. При погружении металла в емкость необходимо убедиться в том, что на нем отсутствует влага. Чаще всего плавят алюминиевую проволоку. Сначала материал делится на фрагменты ножницами, затем сдавливается пассатижами. Такой способ позволяет предотвратить воздействие кислорода на металл. Если нет необходимости в получении деталей высокого качества, измельчать сырье не нужно.
Технологию литья придется смоделировать самостоятельно при необходимости получить расплавленный алюминий в бытовых условиях. Материал предварительно очищается от грязи, примесей, шлаков. Крупные заготовки делятся на несколько малых фрагментов. Метод отливки требует соблюдения инструкции: для плавки металла используется самый удобный способ. Шлак удаляется с поверхности текучего вещества. Жидкий алюминий наливают в форму, которая разбивается после затвердевания.
Какой источник тепла использовать?
Для переплавки алюминия в бытовых условиях применяются:
- Муфельная печь, которую можно изготовить самостоятельно. Это эффективный метод, позволяющий быстро расплавить алюминий.
- Паяльная лампа может расплавить алюминий в малых количествах.
- Иногда используется газовый резак.
Из кирпичей сооружается очаг, каркас изготавливается из металлической емкости. Сбоку сверлится отверстие для подачи кислорода. К металлической трубке присоединяется пылесос, фен или другой прибор, нагнетающий воздух. После разведения огня тигель помещают в очаг.
Чтобы добиться лучшей термообработки, по бокам тоже выкладываются угли. Чтобы избежать потери тепла, можно соорудить крышку, оставить отверстия для выхода дыма. Если металл нужно расплавить один раз, нет необходимости оборудовать печь. Простая газовая плита поможет раскалить алюминий до нужной температуры. Небольшие куски металла плавятся примерно за полчаса.
Обычно жестяная банка применяется в качестве тигля. Чтобы добиться равномерного распределения температуры, емкость с алюминием помещают в другую банку таким образом, чтобы зазор между стенками равнялся 1 см. Чтобы обеспечить доступ пламени, нужно проделать в большой банке несколько отверстий по 3-4 см в диаметре. Рассекатель на конфорке удалять необязательно. Так можно добиться равномерного обогрева банки с металлом. Большую жестянку накрывают крышкой, чтобы тепло не выходило.
Как сделать форму для отливки
Создание простого материала для припоя не требует изготовления специальной формы. Можно вылить металл на стальной лист.
Для создания формы используются такие материалы:
- Гипс.
- Песок.
- Глина.
- Каменноугольный пепел.
- Жидкое стекло.
Сплав заливается в форму разными способами:
Открытый метод отличается простотой. Расплавленный металл переливается в обычную емкость, консервную банку, чашку и т. д. Когда вещество застывает, болванку извлекают из емкости. Если форма металлического предмета неважна, можно оставить алюминий на прочной поверхности.
Сложная отливка требует соответствия изделия указанным параметрам, для этого используются формировочные элементы. Кремнезем – это распространенное вещество, которое часто применяется при открытой заливке. Изделие состоит из двух емкостей, в которые засыпается и трамбуется земля. Элементы кремнезема сжимаются, между ними закладывается макет для отливки. Так можно получить точный отпечаток необходимой детали. Макет удаляется, в форму помещают раскаленный алюминий. Для закрытого способа отливки применяется речной песок, смешанный с жидким стеклом.

Гипс можно использовать для одноразового литья. Из парафина или пенопласта изготавливаются макеты. Применение таких материалов требует выполнения работ на открытом пространстве с хорошим доступом воздуха. Пенопласт не удаляется из твердого гипса, заливается раскаленным алюминием. Продукты горения этого вещества вредны для здоровья.
Распространенные ошибки и как их избежать
Гипсовые формы отличаются удобством и высокой чувствительностью к влаге. Простая сушка не позволяет удалить жидкость, поэтому качество отливки ухудшается. Придется ждать несколько дней, добиться полного высыхания гипсовой формы. Алюминий нужно держать на огне до самой заливки, чтобы успеть распределить его по всей форме.
Нежелательно использовать воду для охлаждения детали. Внутренняя структура вещества при этом нарушается, появляются трещины.
Меры безопасности
Требуется использование индивидуальной защиты при плавке алюминия. Руки, лицо, открытые участки тела должны быть защищены. Рекомендуется использовать перчатки сварщика, которые выдерживают температуру больше 600 градусов. Это главное средство защиты, поскольку шансы попадания жидкого алюминия на руки самые высокие. Очки и маска предотвращают попадание раскаленных элементов в глаза. Чтобы защититься полностью, можно проводить плавильные работы в костюме металлурга с высокой огнестойкостью. Химический респиратор применяется при очистке алюминия сварочным флюсом.
Плавка алюминия в бытовых условиях не представляет сложности. Металл разогревается в заранее подготовленной емкости. С поверхности жидкого вещества удаляются шлаки, затем чистый алюминий заливают в форму. Конструкция печи и температура определяют время плавки. При использовании газовой горелки тепло должно воздействовать на металл сверху.
Как в домашних условиях плавить алюминий
Алюминий часто используется для изготовления деталей. Иногда плавят кусочки алюминия, чтобы заделать дефект, делают отливки. Плавить можно обломки дюраля, ненужные радиодетали. В обзоре представлены способы, как в домашних условиях расплавить алюминий, что для этого потребуется. Специалисты поделятся опытом, расскажут, какие свойства легкого металла необходимо учитывать, чтобы плавить металл самостоятельно.

Характеристики алюминия
Чтобы правильно плавить металл, необходимо учитывать температуру плавки алюминия. Чистый сплав легко плавится уже при +660°С, а оксидная пленка только при +2300°С. Опасно самостоятельно плавить порошок, он способен воспламениться. Кусочки алюминия плавят сухими, вода в расплаве способна спровоцировать взрыв.
Технология плавления алюминия в домашних условиях
Суть плавления состоит из нескольких этапов:
- Подготовка лома. В качестве исходного сырья используют профиль из алюминия, проволоку (ее предварительно уминают пассатижами), отслужившие детали. Кусочки должны быть небольшими. Краску, вкрапления других металлов из них не достают, все это будет в составе шлака.
- Подбор емкости, в которой можно плавить алюминий. Подойдет прочная посудина из стали (температура плавления 1300°С) или чугунок (1100°С), используют готовые огнеупорные тигли.
- Подготовка формы для расплава. В домашних условиях их делают самостоятельно. Процедура изготовления представлена ниже.
- Плавление лома. Предварительно определяют источник тепла.
- Снятие шлака, изготовление отливки. Самый простой способ плавки – аккуратно слить жидкий алюминий в подготовленную емкость или форму, шлак остается на стенках плавильной посудины. Чтобы он не прилип, требуется быстро ее охладить.
В принципе, технология промышленного и кустарного литья ничем не отличается. Лом плавят до состояния текучести. После этого отделяют расплав от шлака, сливают в заготовленные формы. Их после охлаждения отливки разбивают. Важно определить, что в результате должно получиться из жидкого алюминия. Даже если плавить металл решили ради эксперимента, емкость или форму для литья все равно необходимо приготовить. Тогда можно будет рассмотреть получившийся слиток, проверить его на пористость, чистоту, однородность структуры.
Оборудование и способы плавки
Прежде, чем плавить алюминий, выбирают место и способ разогрева металла. Два часто используемых варианта:
- В гаражах или домовладениях плавят алюминий, сооружается плавильня, ее составляют из кирпича без использования связующего раствора. В качестве опоры удобен металлический каркас, в нем должно быть отверстие для нагнетания воздуха, для этого используют пылесос или фен. Самодельная печь обкладывается углем. Емкость для плавления с ломом помещают внутрь. Для лучшего сохранения тепла кирпичи сверху накрывают листом металла.
- В домашних условиях для разогрева небольшого количества лома пользуются:
— газовой плитой, можно плавить небольшое количество лома, но выход расплава будет невысокий.
Литье плавят в стальной посуде. Для повышения скорости нагрева используют конструкцию из двух емкостей, их вставляют одна в другую с зазором 1 см. Дно большой посудины перфорируется, оно выполняет функцию пламярассекателя. Когда есть газовая горелка, совмещают нижний нагрев с верхним. Плавить металл можно быстрее.
Дополнительное оборудование
Для небольших порций лома иногда используют жестяные банки. Но эта тара ненадежная, не исключено прогорание жести. Надежнее использовать керамический или металлический огнеупорный тигель для муфельных печей. Хороший вариант – обрезанный стакан огнетушителя. Для удобства делают желоб, по которому будет стекать расплавленный алюминий. При работе используют длинные щипцы. Понадобится ложка на длинной ручке для сбора шлака.
Как сделать форму для отливки
Перед тем, как расплавить алюминий, готовят болванку для отливки. Существует несколько способов заливки жидкого расплава. Чаще используют открытый и закрытый метод. О каждом стоит рассказать подробнее.
Открытая форма
Когда плавят алюминий по открытой методике, после плавления расплав выливают в подготовленную емкость, например, жестяную банку. Алюминиевую отливку вынимают из банки в горячем виде, когда горячий расплав немного схватится сверху. Достаточно несильно постучать по емкости. Если не нужен слиток заданной геометрии, расплавленный металл выливают на любую ровную огнеупорную поверхность, он хорошо держится, не растекается, внешне напоминает ртуть.
Закрытая форма
Сложные по геометрии отливки получают в специально приготовленных формах. Она должна соответствовать параметрам детали, обычно делается разъемной. Для изготовления формы используют деталь-макет, по которому делают отливку. В качестве формующего материала используют кремнезем, он хорошо трамбуется, его несложно найти. Кремнезем заменяют:
- смесью речного песка и жидкого стекла;
- смесь песка, цемента, вместо воды добавляют тормозную жидкость;
- гипс, он удобен для сложных макетов.
Из гипса делают сплошные бесшовные формы, они одноразовые, их после застывания алюминия разбивают. Деталь-макет изготавливают из воска или пенопласта. Его помещают внутрь емкости, используемой для формы, затем заливают пустоты. Получаются ровные детали, не требующие дополнительной обработки. Когда используется гипс, его сушат в течение пары дней. Гипс боится влаги, разбухает. Он склонен к растрескиванию при высыхании. При контакте с парафином или пенопластом гипс сохраняет свою структуру, не образуется рытвин, раковин.
Полезные советы
- Расплав должен быть горячим, чтобы форма заполнялась равномерно. Его заливают, когда он приобретает консистенцию ртути.
- Сложные по конфигурации отливки делают быстро, стараются сразу залить формы, чтобы металл не успел схватиться, не образовалось перегородок и пустот.
- В гипс металл можно заливать по воску или пенопласту, от высокой температуры воск и пенопласт выгорают. Поверхность отливки будет ровной.
- Для охлаждения отливку не опускают в воду, литье потрескается.
- При расплавлении чистого алюминия применяется технология использования защитных флюсов, они предохраняют металл от окисления.
Необходимо соблюдать противопожарную безопасность, процесс литья связан с использованием открытого пламени. Важно использовать индивидуальные средства защиты: перчатки, очки.
Какая температура плавления алюминия по Цельсию
 Такой металл, как алюминий, очень распространен в мире. Немалое его количество содержится в организме человека, а уж в окружающем мире его еще больше. Среди материалов, из которых построены дома, а также в конструкции любого автомобиля есть некая доля алюминия.
Такой металл, как алюминий, очень распространен в мире. Немалое его количество содержится в организме человека, а уж в окружающем мире его еще больше. Среди материалов, из которых построены дома, а также в конструкции любого автомобиля есть некая доля алюминия.
Нередко из этого вещества изготавливаются детали мебели. И если вдруг что-то из этого сломается, то можно либо приобрести новый товар в соответствующем магазине, либо заняться самостоятельным ремонтом изделия. В последнем случае придется плавить металл в домашних условиях, а для этого уже нужно знать о некоторых свойствах этого металла.
Для изготовления какой-либо алюминиевой конструкции вовсе не обязательно подробно изучать все характеристики вещества, но на основные моменты следует обратить свое внимание, включая знание, при какой температуре плавится алюминий.
О температуре плавления
Необходимо помнить: алюминий очень легко поддается литью и начинает превращаться в жидкую субстанцию уже при температуре в 660 градусов. Для того чтобы понять, что этот показатель довольно низкий, достаточно сравнить его с температурами плавления других металлов, которые также нередко используются для изготовления тех или иных, нужных в обиходе предметов.
Например:
- сталь начинает плавиться лишь при температуре в 1300 градусов;
- чугун — при 1100 градусах.
Но все же, хоть температура плавления алюминия по Цельсию и не слишком высока по сравнению со многими другими металлами, достичь 600 градусов в домашних условиях с использованием обыкновенной газовой или электрической плиты довольно трудно.
Уменьшение температуры
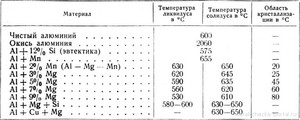 Прежде чем подвергать металл плавлению, можно специальными методами уменьшить его температуру плавления, например, использовать в виде порошка. В этом случае он начнет плавиться чуть быстрее. Но при этом он становится опасным, так как взаимодействуя с атмосферным кислородом, может окислиться или воспламениться. А в результате окисления, как мы помним из школьного курса химии, образуется оксид алюминия; и температура, при которой начинает плавиться это вещество, уже превышает две тысячи градусов.
Прежде чем подвергать металл плавлению, можно специальными методами уменьшить его температуру плавления, например, использовать в виде порошка. В этом случае он начнет плавиться чуть быстрее. Но при этом он становится опасным, так как взаимодействуя с атмосферным кислородом, может окислиться или воспламениться. А в результате окисления, как мы помним из школьного курса химии, образуется оксид алюминия; и температура, при которой начинает плавиться это вещество, уже превышает две тысячи градусов.
Вообще избежать образования оксида не получится, если заниматься плавлением алюминия, но уменьшить количество лишнего вещества вполне возможно. При плавлении алюминия нужно не допускать попадания в вещество воды. Ведь если это случится, то произойдет взрыв.
Перед началом процесса нужно убедиться в том, что сырье является абсолютно сухим. Чаще всего в качестве исходного материала применяется алюминиевая проволока. Предварительно ее нужно с помощью ножниц разделить на множество мелких по длине кусочков. А для того, чтобы уменьшить площадь контакта с содержащимся в атмосфере кислородом, эти кусочки прессуются пассатижами.
Не всегда есть необходимость создать алюминиевое изделие высокого качества, поэтому вовсе не обязательно всегда использовать порошок или мелко нарезанную и плотно сдавленную проволоку. Можно взять любой предмет, который уже был использован, например, банку, в которой хранились консервы. Но перед плавкой нужно лишить ее нижнего шва или обрезать профиль. Полученное сырье может быть окрашено или испачкано. Не нужно об этом беспокоиться. Все, что имеется лишнее на поверхности, быстро отходит в виде шлаков.
Процесс плавления в домашних условиях
Плавление — это довольно опасный процесс. Предварительно необходимо обязательно побеспокоиться о средствах защиты от различных ядовитых веществ, которые будут образовываться, а также подготовить литейную форму.
Средства защиты
 Не обойтись без специальных перчаток даже в том случае, если расплавить алюминий необходимо лишь единожды. Это, пожалуй, основное средство защиты, так как расплавленная масса с большой долей вероятности может попасть на руки, и тогда неминуемо на коже появится ожог, поскольку температура жидкого металла превышает 600 градусов.
Не обойтись без специальных перчаток даже в том случае, если расплавить алюминий необходимо лишь единожды. Это, пожалуй, основное средство защиты, так как расплавленная масса с большой долей вероятности может попасть на руки, и тогда неминуемо на коже появится ожог, поскольку температура жидкого металла превышает 600 градусов.- Следующая часть тела, которую также необходимо защитить от попадания горячего алюминия — глаза. При частой плавке не обойтись без специальной защитной маски, ну или хотя бы очков. Но лучше всего работать в костюме, который устойчив к воздействию высокой температуры в несколько сотен градусов.
- Если необходимо получить чистый алюминий, потребуется рафинирующий флюс. И тогда работать нужно в химическом респираторе.
Выбор формы для литья
 Для того, чтобы отлить алюминий, необязательно запасаться литейной формой. Достаточно лишь приобрести лист из более тугоплавкого металла — из стали, вылить на него расплавленный алюминий и подождать, пока последний затвердеет. Но для получения какой-либо детали из алюминия обязательно придется приобретать форму для литья.
Для того, чтобы отлить алюминий, необязательно запасаться литейной формой. Достаточно лишь приобрести лист из более тугоплавкого металла — из стали, вылить на него расплавленный алюминий и подождать, пока последний затвердеет. Но для получения какой-либо детали из алюминия обязательно придется приобретать форму для литья.
Ее можно изготовить самостоятельно в домашних условиях. Для этой цели обычно используется скульптурный гипс. Он заливается в форму, затем какое-то время охлаждается. После этого в него вставляют модель и сверху кладут вторую емкость с гипсом. При этом важно не забыть проделать отверстие в гипсе с помощью какого-нибудь предмета цилиндрической формы. Через это отверстие и будет заливаться горячий алюминий.
При плавлении алюминия не обойтись без так называемого тигеля: то есть емкости из тугоплавкого металла. Она может быть выполнена из фарфора, кварца, стали, чугуна. Впрочем, изготавливать тигель самостоятельно вовсе не обязательно, ведь его можно просто купить в специальном магазине. Объем тигеля зависит от того, какое количество металла требуется получить.
Кратко о процессе
 Плавка алюминия в домашних условиях — это не такой уж трудный процесс, которым он может показаться поначалу. Кусочки металла нагреваются до нужной температуры плавки алюминия в специальной емкости.
Плавка алюминия в домашних условиях — это не такой уж трудный процесс, которым он может показаться поначалу. Кусочки металла нагреваются до нужной температуры плавки алюминия в специальной емкости.
Некоторое время полученный расплав необходимо выдерживать в разогретом состоянии и периодически удалять с его поверхности образующийся шлак. После этого чистый жидкий металл наливается в специальную форму, в которой он некоторое время будет остывать.
Время, которое уйдет на плавку, зависит от самой печи, а точнее от той температуры, которую она может обеспечить. Если же вместо печи используется газовая горелка, то она должна нагревать металл сверху.
Удельный вес, теплопроводность и температура плавления алюминия
 Алюминий — всем известный из школьного курса химии элемент из таблицы Менделеева. В большей части соединений он проявляет трехвалентность, но в условиях высоких температур достигает некоторой степени окисления. Одним из самых важных его соединений является оксид алюминия.
Алюминий — всем известный из школьного курса химии элемент из таблицы Менделеева. В большей части соединений он проявляет трехвалентность, но в условиях высоких температур достигает некоторой степени окисления. Одним из самых важных его соединений является оксид алюминия.
Основные характеристики алюминия
 Алюминий — серебристый металл с удельным весом 2,7*10 3 кг/м 3 и плотностью 2,7 г/см 3 . Легкий и пластичный, хорош, как проводник электроэнергии, благодаря тому, что теплопроводность алюминия довольно высока — 180 ккал/м*час*град (указан коэффициент теплопроводности). Теплопроводность алюминия превышает аналогичный показатель чугуна в пять раз и железа в три раза.
Алюминий — серебристый металл с удельным весом 2,7*10 3 кг/м 3 и плотностью 2,7 г/см 3 . Легкий и пластичный, хорош, как проводник электроэнергии, благодаря тому, что теплопроводность алюминия довольно высока — 180 ккал/м*час*град (указан коэффициент теплопроводности). Теплопроводность алюминия превышает аналогичный показатель чугуна в пять раз и железа в три раза.
Благодаря своему составу, этот металл можно легко раскатать в тонкий лист или вытянуть в проволоку. При соприкосновении с воздухом на его поверхности образуется оксидная пленка (оксид алюминия), которая является защитой от окисления и обеспечивает его высокие антикоррозионные свойства. Тонкий алюминий, например, фольга или порошок этого металла мгновенно сгорают, если их нагреть до высоких температур и становятся оксидом алюминия.
Металл не особенно устойчив к агрессивным кислотам. К примеру, его можно растворить в серной или соляной кислотах даже, если они разбавленны, особенно, если их нагреть. Однако он не растворяется ни в разбавленной ни в концентрированной и при этом холодной азотной кислоте, благодаря оксидной пленке. Определенное воздействие на металл имеют водные растворы щелочей — оксидный слой растворяется и образуются соли, содержащие этот металл в составе аниона — алюминаты.
Известно, что алюминий является самым часто встречающимся металлом в природе, но впервые в чистом виде его смог получить ученый-физик из Дании Х. Эрстед еще в 1925 году XIX века. Этот металл занимает третье место по распространенности в природе среди элементов и является лидером среди металлов. 8,8% алюминия содержит земная кора. Его выявили в составе слюд, полевых шпатов, глин и минералов.
Производство и применение алюминия
 Процесс производства очень энергоемкий и поэтому первый большой завод в нашей стране был построен и запущен в XX веке. Основным сырьем для получения этого металла является оксид алюминия. Чтобы его получить, необходимо минералы, содержащие алюминий или бокситы, очистить от примесей. Далее электролитическим способом расплавляют естественный или полученный искусственным путем криолит при температуре чуть ниже 1000 ºС . Затем начинают понемногу добавлять оксид алюминия и сопутствующие вещества, необходимые для улучшения качества металла. В процессе оксид начинает разлагаться и выделяется алюминий. Чистота получаемого металла 99,7% и выше.
Процесс производства очень энергоемкий и поэтому первый большой завод в нашей стране был построен и запущен в XX веке. Основным сырьем для получения этого металла является оксид алюминия. Чтобы его получить, необходимо минералы, содержащие алюминий или бокситы, очистить от примесей. Далее электролитическим способом расплавляют естественный или полученный искусственным путем криолит при температуре чуть ниже 1000 ºС . Затем начинают понемногу добавлять оксид алюминия и сопутствующие вещества, необходимые для улучшения качества металла. В процессе оксид начинает разлагаться и выделяется алюминий. Чистота получаемого металла 99,7% и выше.
Этот элемент нашел свое применение в пищевом производстве в качестве фольги и столовых приборов, в строительстве используют его сплавы с другими металлами, в авиации, электротехнике в качестве заменителя меди для кабелей, как легирующая добавка в металлургии, алюмотермии и других отраслях.
Что такое температура плавки металлов?
 Температура плавки металлов – значение температуры нагревания металла, при которой начинается процесс перехода из исходного состояния в другое, то есть процесс противоположный кристаллизации (отвердевания), но неразрывно связаный с ней.
Температура плавки металлов – значение температуры нагревания металла, при которой начинается процесс перехода из исходного состояния в другое, то есть процесс противоположный кристаллизации (отвердевания), но неразрывно связаный с ней.
Итак, для расплавления металл нагревают извне до температуры плавки и продолжают нагревать для преодоления границы фазового перехода. Суть в том, что показатель температуры плавки означает температуру, при которой металл находится в фазовом равновесии, то есть между жидким и твердым телом. Другими словами существует одновременно, как в том, так и в другом состоянии. А для плавления нужно нагреть его больше пограничной температуры, чтобы процесс пошел в нужную сторону.
Стоит сказать о том, что только для чистых составов температура плавки постоянна. Если в составе металла находятся примеси, то это сместит границу фазового перехода, а, соответственно, и температура плавления будет другой. Это объясняется тем, что состав с примесями имеет иную кристаллическую структуру, в которой атомы взаимодейстуют между собой по-другому. Исходя из этого принципа, металлы можно разделить на:
- легкого плавления, такие как ртуть и галлий, например, (температура плавки до 600°С)
- среднеплавкие — это алюминий и медь (600-1600°С)
- тугоплавкие — молибден , вольфрам (больше 1600°С).
Знание показателя температуры плавления необходимо, как при производстве сплавов для правильного расчета их параметров, так и при эксплуатации изделий из них, поскольку этот показатель определяет ограничения их использования. Уже давным давно для удобства ученые физики свели эти данные в одну таблицу. Существуют таблицы температур плавки как металлов, так и их сплавов.
Температура плавления алюминия
 Плавление — процесс перерабатывания металлов обычно в специальных печах для получения сплава нужного качества в жидком состоянии . Как уже говорилось выше, алюминий относится к среднеплавким металлам и плавится при нагреве до 660ºС. При изготовлении изделий из металла температура плавления влияет на выбор плавильной печи или агрегата и, соответственно, используемых для отливки огнеупорных форм.
Плавление — процесс перерабатывания металлов обычно в специальных печах для получения сплава нужного качества в жидком состоянии . Как уже говорилось выше, алюминий относится к среднеплавким металлам и плавится при нагреве до 660ºС. При изготовлении изделий из металла температура плавления влияет на выбор плавильной печи или агрегата и, соответственно, используемых для отливки огнеупорных форм.
Указанная температура относится к процессу расплавки чистого алюминия. Так как в чистом виде он применяется реже, а введение в его состав примесей меняет температуру плавления. Сплавы алюминия изготавливаются для того, чтобы изменить какие-либо его свойства, увеличить прочность, например, или жароустойчивость. В качестве добавок применяют:
- цинк
- медь
- магний
- кремний
- марганец.
Добавление примесей влечет за собой снижение электропроводности, ухудшение или улучшение коррозионных свойств, повышение относительной плотности.
Обычно добавление других элементов в металл приводит к тому, что температура плавления сплава понижается, но не всегда. К примеру, добавление меди в объеме 5,7% приводит к понижению температуры плавления до 548ºС. Полученный сплав называют дюралюминием, его подвергают дальнейшей термической закалке. А алюминиево-магниевые составы плавятся при температуре 700 — 750ºС.
Во время процесса плавления необходим строгий контроль температуры расплава, а также присутствия газов в составе, которые выявляют через технологические пробы или способом вакуумной экстракции. На заключительной стадии производства сплавов алюминия проводят их модифицирование.
При какой температуре плавится железо
При какой температуре плавится железо

 |  |  | 1.3 Основные физические свойства железа |
Температура плавления химически чистого железа составляет 1539 о С. Технически чистое железо, полученное в результате окислительного рафинирования, содержит некоторое количество растворенного в металле кислорода. По этой причине температура его плавления понижается до 1530 о С.
Температура плавления стали всегда ниже температуры плавления железа в связи с наличием в ней примесей. Растворенные в железе металлы (Mn, Cr, Ni. Co, Mo, V и др.) понижают температуру плавления металла на 1 – 3 о С на 1% введенного элемента, а элементы из группы металлоидов (C, O, S, P и др.) на 30 – 80 о С.
На протяжении большей части общей продолжительности плавки температура плавления металла изменяется главным образом в результате изменения содержания углерода. При концентрации углерода 0,1 – 1,2%, которая характерна для доводки плавки в сталеплавильных агрегатах, температуру плавления металла с достаточной для практических целей точностью можно оценить из уравнения

Теплота плавления железа составляет 15200 Дж/моль или 271,7 кДж/кг.
Температура кипения железа в изданиях последних лет приводится равной 2735 о С. Однако, опубликованы результаты исследований, согласно которым температура кипения железа значительно выше (до 3230 о С).
Теплота испарения железа составляет 352,5 кДж/моль или 6300 кДж/кг.
Давление насыщенного пара железа (PFe, Па) можно оценить при помощи уравнения

где Т – температура металла, К.
Результаты расчета давления насыщенного пара железа при различных температурах, а также содержания пыли в окислительной газовой фазе над металлом (X, г/м 3 ) представлены в таблице 1.1.
Таблица 1.1 – Давление насыщенного пара железа и запыленность газов при разных температурах

Согласно существующим санитарным нормам содержание пыли в газах, которые выбрасываются в атмосферу, не должно превышать 0,1 г/м 3 . Из данных таблицы 1.1 видно, что при 1600 о С запыленность газов над открытой поверхностью металла выше допустимых значений. Поэтому обязательно требуется очистка газов от пыли, состоящей в основном из оксидов железа.
Динамическая вязкость. Коэффициент динамической вязкости жидкости ( ) определяется из соотношения
) определяется из соотношения

где F – сила взаимодействия двух движущихся слоев, Н;
S – площадь соприкосновения слоев, м 2 ;
 – градиент скорости слоев жидкости по нормали к направлению потока, с -1 .
– градиент скорости слоев жидкости по нормали к направлению потока, с -1 .
Динамическая вязкость сплавов железа обычно изменяется в пределах 0,001 – 0,005 Па•с. Ее величина зависит от температуры и содержания примесей, главным образом углерода. При перегреве металла над температурой плавления выше 25 – 30 о С влияние температуры не существенно.
Кинематическая вязкость жидкости представляет собой скорость передачи импульса в потоке единичной массы. Ее величина определяется из уравнения

где – плотность жидкости, кг/м 3 .
Величина динамической вязкости жидкого железа близка к 6•10 -7 м 2 /с.
Плотность железа при 1550 – 1650 о С равна 6700 – 6800 кг/м 3 . При температуре кристаллизации плотность жидкого металла близка к 6850 кг/м 3 . Плотность твердого железа при температуре кристаллизации равна 7450 кг/м 3 , при комнатной температуре – 7800 кг/м 3 .
Из обычных примесей наибольшее влияние на плотность расплавов железа оказывают углерод и кремний, понижая ее. Поэтому обычного состава жидкий чугун имеет плотность 6200 – 6400 кг/м 3 , твердый при комнатной температуре – 7000 – 7200 кг/м 3 .
Плотность жидкой и твердой стали занимает промежуточное положение между плотностями железа и чугуна и составляет соответственно 6500 – 6600 и 7500 – 7600 кг/м 3 .
Удельная теплоемкость жидкого металла практически не зависит от температуры. В оценочных расчетах величину ее можно принимать равной 0,88 кДж/(кг•К) для чугуна и 0,84 кДж/(кг•К) для стали.
Поверхностное натяжение железа имеет максимальное значение при температуре около 1550 о С. В области более высоких и низких температур величина его уменьшается. Это отличает железо от большинства металлов, для которых характерно понижение поверхностного натяжения при повышении температуры.
Поверхностное натяжение жидких сплавов железа существенно меняется в зависимости от химического состава и температуры. Обычно оно изменяется в пределах 1000 – 1800 мДж/м 2 (рисунок 1.1).

Рисунок 1.1 – Влияние примесей на величину поверхностного натяжения сплавов железа
Растворимость. Весьма ограниченную растворимость в жидком и твердом железе имеют щелочные (Li, Na, K, Rb, Cs) и щелочноземельные (Mg, Ca, Ba, Sr) металлы. Кроме того практически нерастворимыми являются Ag, Cd и Bi.
К числу металлов, имеющих неограниченную растворимость в железе, относятся Mn, Ni, Co, Cu, Al, Sb, Ce и все редкоземельные металлы.
Ограниченной растворимостью в железе обладают Cr, V, Mo, W, Ti, Zr, Pb, Sn, Pt и др. Но при высоких температурах все металлы этой группы, кроме Pb и Sn, растворяются в расплавах железа в неограниченных количествах.
Железо: химические свойства и температура плавления
 Металлы плавятся, как правило, при очень высокой температуре, которая может достигать более 3 тыс. градусов. Хотя некоторые из них можно расплавить в домашних условиях, например, свинец или олово. А вот ртуть плавят при температуре минус 39 градусов. В домашних условиях этого добиться не удастся. Температура плавления — это один из важных показателей производства не только самого металла, но и его сплавов. Выплавляя сырье, специалисты учитывают и другие физические и химические свойства руды и металла.
Металлы плавятся, как правило, при очень высокой температуре, которая может достигать более 3 тыс. градусов. Хотя некоторые из них можно расплавить в домашних условиях, например, свинец или олово. А вот ртуть плавят при температуре минус 39 градусов. В домашних условиях этого добиться не удастся. Температура плавления — это один из важных показателей производства не только самого металла, но и его сплавов. Выплавляя сырье, специалисты учитывают и другие физические и химические свойства руды и металла.
Железо и его свойства
Железо — это химический элемент, который в таблице Менделеева находится под номером 26. Это один из самых распространенных элементов во всей Солнечной системе. Согласно материалам исследований, в составе ядра Земли находится примерно 79−85% этого вещества. В земной коре его тоже присутствует большое количество, но оно уступает алюминию.
В чистом виде металл имеет белый цвет с чуть серебристым оттенком. Он пластичен, но имеющиеся в нем примеси могут определять его физические свойства. Реагирует на магнит.
 Железо присутствует в воде. В речных водах его концентрация равна примерно 2 мг/л металла. В морской воде его содержание может быть ниже в сто или даже тысячу раз.
Железо присутствует в воде. В речных водах его концентрация равна примерно 2 мг/л металла. В морской воде его содержание может быть ниже в сто или даже тысячу раз.
Оксид железа — это основная форма, добыча которой осуществляется и которая находится в природе. Оксидное железо может располагаться в самой верхней части земной коры и быть составляющей осадочных образований.
Элемент, находящийся на двадцать шестом месте в таблице Менделеева, может иметь несколько степеней окисления. Именно они определяют его геохимическую особенность нахождения в определенной среде. В ядре Земли металл присутствует в нейтральной форме.
Добыча полезных ископаемых
Руд, в которых присутствует железо, существует несколько. Однако, в качестве сырья для производства железа в промышленности используют в основном следующие:
- магнезитовую руду;
- гетитовую руду;
- гематитовую руду.
А также часто встречаются такие разновидности руды:
 леллингит;
леллингит;- сидерит;
- марказит;
- ильменит;
- ярозит.
Существует еще минерал под названием мелантерит. Его используют преимущественно в фармацевтической промышленности. Из себя он представляет зелёного цвета хрупкие кристаллы, в которых присутствует стеклянный блеск. Из него производят лекарственные препараты, в составе которых имеется ферум.
Основным месторождением этого металла является Южная Америка, а именно Бразилия.
Плавление железа и необходимая температура
Точкой плавления металла называют такую минимальную температуру, при которой он переходит из твердого состояния в жидкое. При этом в объеме он практически остается неизменным.
 Металл могут производить из руды различными способами, но самый основной из них — это доменный. Помимо доменного, используют еще выплавку железа при помощи обжига измельченной руды с примесью глины. Из полученной смеси формируют окатыши, которые обрабатываются в печи с последующим восстановлением водородом. Далее плавление железа осуществляется в электрической печи.
Металл могут производить из руды различными способами, но самый основной из них — это доменный. Помимо доменного, используют еще выплавку железа при помощи обжига измельченной руды с примесью глины. Из полученной смеси формируют окатыши, которые обрабатываются в печи с последующим восстановлением водородом. Далее плавление железа осуществляется в электрической печи.
Температура плавления железа весьма высока. Для технически чистого элемента она составляет +1539 °C. В этом веществе присутствует примесь — Сера, которую можно извлечь лишь в жидком виде. Без примесей чистый материал получают при электролизе солей металла.
Классификация металлов по температуре плавления
Разные металлы могут переходить в жидкое состояние при разной температуре. Вследствие этого выделяют определённую классификацию. Их делят следующим образом:
- Легкоплавкие — те элементы, которые могут становиться жидкими уже при температуре ниже 600 градусов. К ним относят цинк, олово, свинец и пр. Их можно расплавить даже в домашних условиях — просто нужно разогреть при помощи плиты или паяльника. Такие виды нашли применение в технике и электронике. Они используются для соединения элементов из металла и движения электрического тока. Олово плавится при 232 градусах, а цинк — при 419 градусах.
- Среднеплавкие — элементы, которые начинают расплавляться при температуре от шестисот до тысячи шестисот градусов. Эти элементы используют по большей части для строительных элементов и металлоконструкций, то есть при создании арматур, плит и строительных блоков. В эту группу входят: железо, медь, алюминий. Температура плавления алюминия сравнительно низка и составляет 660 градусов. А вот железо начинает переходить в жидкое состояние лишь при температуре 1539 градусов. Это один из самых распространенных металлов, используемых в промышленности, особенно в автомобильной. Однако железо подвержено коррозии, то есть ржавчине, поэтому ему требуется специальная поверхностная обработка. Его необходимо покрывать краской или олифой, и не допускать попадание влаги.
- Тугоплавкие — это такие материалы, которые расплавляются и становятся жидкими при температуре выше 1600 градусов. В эту группу относят вольфрам, титан, платину, хром и т. п. Они используются в ядерной промышленности и для некоторых машинных деталей. Они могут применяться для расплавки других металлов, изготовления высоковольтных проводов или проволоки. Платину можно расплавить при 1769 градусах, а вольфрам — при 3420 °C.
Единственный элемент, который при обычных условиях находится в жидком состоянии — это ртуть. Температура его плавления составляет минус 39 градусов и его пары являются ядовитыми, поэтому его используют только в лабораториях и закрытых ёмкостях.
Сплавы железа и температура их плавления.
Температура плавления железа является важным показателем технологии производства металла и его сплавов. При выплавке сырья учитываются физические и химические свойства руды и металла.

Физические и химические свойства железа
- Химический элемент № 26 является самым распространенным в Солнечной системе. По данным исследований содержание железа в ядре Земли составляет 79–85,5%. По распространенности в коре планеты оно уступает только алюминию.
- Металл в чистом виде имеет белый цвет с серебристым оттенком, отличается пластичностью. Наличие примесей определяет его физические параметры. Железу свойственно реагировать на магнит.
- Для этого химического элемента характерен полиморфизм, который имеет место при нагревании. Повышенная концентрация металла наблюдается в местах извержения пород. Промышленные месторождения формируются в результате внешних и внутренних процессов, происходящих в земной коре.
- В речной воде содержится приблизительно 2 мг/л металла, а показатель для морской воды меньше в 100–1000 раз.
- Железо имеет несколько степеней окисления, определяющих его геохимическую особенность нахождения в определенной среде. В нейтральной форме металл находится в ядре Земли.
- Оксид железа является основной формой нахождения в природе, а оксидное железо размещается в самой верхней части земной коры в составе осадочных образований.
- Содержание химического элемента № 26 в минералах с нестабильным составом увеличивается с уменьшением температурного градиента. Кипение происходит при нагревании до + 2861 °C. Удельная теплота плавления составляет 247,1 КДж/кг.
Добыча металла
Среди руд, содержащих железо, сырьем для промышленного производства являются:
Гетит и гидрогетит формируют образования в коре выветривания, размером сотни метров. В зоне шельфа и озерах коллоидные растворы минералов в результате осаждения образуют оолиты (бобовые железные руды).
Пирит и пирротин, широко распространенные в природе минералы железа, используются в качестве сырья для производства серной кислоты.
К часто встречающимся минералам железа относятся также:
Минерал мелантерит, представляющий собой хрупкие зеленые кристаллы со стеклянным блеском, используется в фармацевтической промышленности для производства железосодержащих препаратов.
Основное месторождение этого металла находится в Бразилии. В последнее время внимание сосредоточивается на разработке конкреций, присутствующих на морском дне, в которых содержатся железо и марганец.
Плавление железа
От чего зависит температура плавления железа?
Производство металла предусматривает различные технологии его извлечения из рудного сырья. Наиболее распространена выплавка железа доменным способом.
Перед тем как выплавлять металл, его восстанавливают в печи при температуре +2000 °C. Для извлечения примесей добавляется флюс, разлагающийся при нагревании до оксида с последующим соединением с диоксидом кремния и образованием шлака.
Кроме доменного способа выплавка железа производится путем обжига измельченной руды с глиной. Из смеси формируются окатыши и обрабатываются в печи с восстановлением водородом. Дальнейшая плавка железа производится в электрических печах.

Свойства металла зависят от чистоты материала. Для технически чистого железа температура плавления составляет +1539 °C. Сера является вредной примесью. Извлечь ее можно только из жидкого раствора. Химически чистый материал получают в результате электролиза солей металла.
Сплавы металла
В чистом виде этот материал мягкий, поэтому для повышения прочности в состав вводят углерод.
В металлургии сплавы железа называют черными металлами.
В зависимости от компонентов лигатуры меняются свойства материалов. Температура плавления железа также меняется при наличии лигатурных компонентов.
Удельная теплота плавления стали равна 84 кДж. Этот показатель обозначает, что при температуре плавления стали для перевода 1 кг сплава из кристаллического в жидкое состояние необходимо 84 кДж энергии.
Соединения из различных металлов образуют сплавы. Удельная теплота плавления чугуна составляет 96–140 кДж. Чугун содержит до 4% углерода, 1,5% марганца, до 4,5% кремния и примеси в виде серы и фосфора. Различают белый и серый сплавы.
В белом часть углерода находится в соединении карбида железа. Такой сплав отличается хрупкостью и твердостью. Он предназначается для изготовления конструкций и деталей.
Серый сплав, содержащий углерод в виде графита, легко поддается обработке. Чугун выплавляют из железной руды в доменных печах. Плавление руды сопровождается восстановительной реакцией железа из оксидов углеродом.
Большинство веществ может плавиться с увеличением объема при нагревании. Для чугуна объемом 1000 см³ этот показатель составляет 988–994 см³.
Чугун является сырьем для производства стали, отличающейся содержанием углерода (не выше 2,14%).
По химическому составу различают сталь:
Углеродистая сталь содержит примеси серы, фосфора и кремния. Она отличается низкими электротехническими свойствами, низкой прочностью, легко поддается процессу коррозии.
Наличие лигатурных добавок придает стали новые технические свойства. В качестве дополнительных компонентов используют:
В состав высоколегированной стали входит не более 10% добавок. Сплав отличается прочностью. Технология производства стали из чугуна позволяет получить высококачественный материал для производства:
- металлических конструкций;
- резервуаров;
- посуды;
- армирующих деталей;
- электрооборудования.

В качестве сырья сталь используется в разных отраслях промышленности. Без нее невозможно представить авиастроение, кораблестроение, автомобильную отрасль и многие другие производственные сферы.
Температура кипения и плавления металлов. Температура плавления стали
Температура кипения и плавления металлов
В таблице представлена температура плавления металлов tпл, их температура кипения tк при атмосферном давлении, плотность металлов ρ при 25°С и теплопроводность λ при 27°С.
Температура плавления металлов, а также их плотность и теплопроводность приведены в таблице для следующих металлов: актиний Ac, серебро Ag, алюминий Al, золото Au, барий Ba, берилий Be, висмут Bi, кальций Ca, кадмий Cd, кобальт Co, хром Cr, цезий Cs, медь Cu, железо Fe, галлий Ga, гафний Hf, ртуть Hg, индий In, иридий Ir, калий K, литий Li, магний Mg, марганец Mn, молибден Mo, натрий Na, ниобий Nb, никель Ni, нептуний Np, осмий Os, протактиний Pa, свинец Pb, палладий Pd, полоний Po, платина Pt, плутоний Pu, радий Ra, рубидий Pb, рений Re, родий Rh, рутений Ru, сурьма Sb, олово Sn, стронций Sr, тантал Ta, технеций Tc, торий Th, титан Ti, таллий Tl, уран U, ванадий V, вольфрам W, цинк Zn, цирконий Zr.
По данным таблицы видно, что температура плавления металлов изменяется в широком диапазоне (от -38,83°С у ртути до 3422°С у вольфрама). Низкой положительной температурой плавления обладают такие металлы, как литий (18,05°С), цезий (28,44°С), рубидий (39,3°С) и другие щелочные металлы.
Наиболее тугоплавкими являются следующие металлы: гафний, иридий, молибден, ниобий, осмий, рений, рутений, тантал, технеций, вольфрам. Температура плавления этих металлов выше 2000°С.
Приведем примеры температуры плавления металлов, широко применяемых в промышленности и в быту:
- температура плавления алюминия 660,32 °С;
- температура плавления меди 1084,62 °С;
- температура плавления свинца 327,46 °С;
- температура плавления золота 1064,18 °С;
- температура плавления олова 231,93 °С;
- температура плавления серебра 961,78 °С;
- температура плавления ртути -38,83°С.
Максимальной температурой кипения из металлов, представленных в таблице, обладает рений Re — она составляет 5596°С. Также высокими температурами кипения обладают металлы, относящиеся к группе с высокой температурой плавления.
Плотность металлов в таблице находится в диапазоне от 0,534 до 22,59 г/см 3 , то есть самым легким металлом является литий, а самым тяжелым металлом осмий. Следует отметить, что осмий имеет плотность большую, чем плотность урана и даже плутония при комнатной температуре.
Теплопроводность металлов в таблице изменяется от 6,3 до 427 Вт/(м·град), таким образом хуже всего проводит тепло такой металл, как нептуний, а лучшим теплопроводящим металлом является серебро.
Температура плавления стали
Представлена таблица значений температуры плавления стали распространенных марок. Рассмотрены стали для отливок, конструкционные, жаропрочные, углеродистые и другие классы сталей.
Температура плавления стали находится в диапазоне от 1350 до 1535°С. Стали в таблице расположены в порядке возрастания их температуры плавления.
| Сталь | tпл, °С | Сталь | tпл, °С |
|---|---|---|---|
| Стали для отливок Х28Л и Х34Л | 1350 | Коррозионно-стойкая жаропрочная 12Х18Н9Т | 1425 |
| Сталь конструкционная 12Х18Н10Т | 1400 | Жаропрочная высоколегированная 20Х23Н13 | 1440 |
| Жаропрочная высоколегированная 20Х20Н14С2 | 1400 | Жаропрочная высоколегированная 40Х10С2М | 1480 |
| Жаропрочная высоколегированная 20Х25Н20С2 | 1400 | Сталь коррозионно-стойкая Х25С3Н (ЭИ261) | 1480 |
| Сталь конструкционная 12Х18Н10 | 1410 | Жаропрочная высоколегированная 40Х9С2 (ЭСХ8) | 1480 |
| Коррозионно-стойкая жаропрочная 12Х18Н9 | 1410 | Коррозионно-стойкие обыкновенные 95Х18…15Х28 | 1500 |
| Сталь жаропрочная Х20Н35 | 1410 | Коррозионно-стойкая жаропрочная 15Х25Т (ЭИ439) | 1500 |
| Жаропрочная высоколегированная 20Х23Н18 (ЭИ417) | 1415 | Углеродистые стали | 1535 |
- Волков А. И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
- Казанцев Е. И. Промышленные печи. Справочное руководство для расчетов и проектирования.
- Физические величины. Справочник. А. П. Бабичев, Н. А. Бабушкина, А. М. Братковский и др.; Под ред. И. С. Григорьева, Е. З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с.
При какой температуре плавится дюраль
Дюралюминий
Для производства различных деталей и вещей может использоваться дюралюминий. Данный материал получил свое название от города, в котором он был создан. Отличия дюрали от алюминия заключаются в химическом составе, который оказывает влияние на основные эксплуатационные качества. Рассмотрим особенности данного сплава подробнее.

Химический состав
Появление дюралюминия связывают с немецкой компанией, которая расположена в городе Дюрен. Специалисты этой компании занимались разработкой нового сплава, и ошибочно провели смешивание ранее не используемых компонентов. После проведения предварительных тестов они были удивлены тем, какого смогли добиться результата, но изначально посчитали их ошибочными. Спустя некоторое время они повторили свой эксперимент и добились еще более высоких результатов.
Алюминий и дюралюмин, в первую очередь, отличаются друг от друга химическим составом. Дюралюминий обладает следующим составом:
- 4-5% меди;
- 93% алюминия;
- 2-3% других легирующих элементов, которые добавляются для придания сплаву особых качеств.

Состав различных марок дюрали
Долгое время дюралюмин изготавливался при обычных условиях, что определяло некачественное соединение элементов. Начавшаяся война сделала данный металл стратегически важным, что привело к поиску более эффективных методов соединения всех компонентов. Результатом данных исследований стали следующие технологические особенности процесса:
- Нагрев проводится при температуре до 500 градусов Цельсия.
- На разогрев уходит около 3-х часов.
- Проводится быстрое охлаждение водой или селитрой для повышения прочности.
Состав дюралюминия может существенно меняться — все зависит от особенностей применяемой технологии производства.
Наиболее распространенная марка Д16 имеет следующий химический состав:
- Основная часть дюралюминия во всех случая представлена алюминием, на который приходится 90-94% от общей массы.
- В состав добавляется достаточно большое количество меди (3,8-4,9%).
- Обязательным условием можно назвать добавление в равных частях кремния и железа, примерно по 0,5%.
- В состав входит цинк (не более 2,5%).
- Добавляется фиксированное значение магния — 1,8%.
Остальные компоненты представлены хромом, марганцем, титаном, которые берутся примерно по 1%.
Получаемый дюралюминий при подобном химическом составе обладает достаточно высоким показателем мягкости. Именно поэтому Д16 зачастую применяется в качестве полуфабрикатов при производстве штамповок.
Не только состав сплава дюрали оказывает влияние на основные технологические свойства. Вместе со специфической подборкой компонентов применяются технология искусственного старения, которая заключается в закалке.Для повышения прочности и твердости поверхности сплав подвергается термической обработке с охлаждением.
Технологические свойства дюрали
В зависимости от химического состава и применяемого метода изготовления технологические свойства дюрали могут существенно отличаться. ГОСТа именно для этого металла пока нет.
Сразу после появления дюралюминия его назвали самым подходящим материалом для строительства дирижаблей и самолетов.
Среди технологических свойств следует отметить нижеприведенные моменты:
- Низкая стоимость, которая обуславливается простой технологией производства. Тот момент, что компоненты не нужно разогревать до экстремально высоких температур определяет существенное удешевление материала. Также на стоимости благоприятно отражается возможность проведения производства в обычной среде.
- Небольшой вес. Рассматривая химический состав можно отметить, что большая часть состава представлена алюминием. Этот металл известен своей легкостью.
- Высокие показатели температуры плавления позволили использовать сплав дюраль при производстве различных элементов самолетов и другой техники. Температура плавления дюралюминия около 650 градусов Цельсия. При этом обычный алюминий плавится уже при более низких температурах, что приводит к изменению основных технологических качеств и деформации изделий.
- Плотность дюралюминия составляет 2,5 грамма на кубический сантиметр (у стали на каждый кубический сантиметр приходится 8 грамм). Именно этот показатель определяет существенно снижение веса изготавливаемых деталей. Данный показатель может варьироваться в относительно небольшом диапазоне, достигать значения 2,8 грамм на кубический сантиметр.
- Статическая прочность дюралюминия достаточно высока, что определяет устойчивость к разовой нагрузке. Именно поэтому сплав применяется при изготовлении различных ответственных деталей. Проведенные исследования указывают на то, что разрушить подобный материал довольно сложно.
Однако есть и один недостаток – относительно невысокая устойчивость к воздействию повышенной влажности. Разрушение сплава блокируют путем нанесения защитного покрытия, что несколько повышает стоимость сплава.

Детали из дюрали
Дюралюминий Д16 получил достаточно широкое распространение. Отличные эксплуатационные качества он демонстрирует при температуре не выше 250 градусов Цельсия. Стоит учитывать, что уже при температуре 80 градусов Цельсия появляются признаки образования межкристаллической коррозии.
В последнее время в чистом виде дюралюминий практически не применяется. Это связано не только с высокой вероятностью появления коррозии, но и другими недостатками алюминиевого сплава. Для повышения эксплуатационных качеств сегодня выполняют следующее улучшение:
- Закалку в естественных условиях. При маркировке указывается буква «Т».
- Выполняют процедуру искусственного старения, что также отражается на маркировке «Т1».
- Анодирование и покрытие поверхности специальными лаками (в маркировке указывают букву «А»).
Снижение коррозионной стойкости происходит не только по причине повышения температуры, но и механического воздействия. Именно поэтому уделяется внимание дополнительным процедурам увеличения эксплуатационных качеств.
Более высокими эксплуатационными качествами обладает сплав под названием ВД95. Кроме этого, данная разновидность сплава проходит процедуру старения, за счет чего существенно повышается потенциал этой разновидности дюралюминия.
Область применения
Тугоплавкость дуралюмина марки ВД95 определяет его широкое применение не только в сфере авиастроения, но и изготовления скоростных поездов, которые постепенно становятся самым распространенным транспортным средством в Европе и Азии. Это связано с тем, что при движении на большой скорости из-за возникающего трения поверхность может сильно нагреваться. Слишком высокая пластичность из-за перестроения кристаллической решетки становится причиной деформации поверхности при механическом воздействии. Также применение дюралюминия представлено производством прутков, заклепок, болтов и других крепежных материалов.
Несмотря на тугоплавкость, есть возможность проводить сварочные работы с помощью аргона. Данный процесс настолько прост, что его можно провести в собственном гараже. В различных отраслях машиностроения дюралюминий применяется для получения изоляционных материалов. Примером можно назвать появление фольги толщиной около 0,2 миллиметров, которая применяется в качестве отражающего слоя при производстве изоляции.
В пищевой промышленности фольга из дюралюминия встречается довольно часто — ее используют для оборачивания конфет.
Сплав получил широкое применение и в буровой отрасли. Это связано с уникальным сочетанием нижеприведенных качеств:
- Легкость.
- Прочность.
- Стойкость к повышенным температурам и влажности.
Изготавливаемые буры из дюралюминия отлично справляются с гашением вибрации.
В заключение отметим, что широкая область применения определена особыми эксплуатационными качествами и относительно невысокой стоимостью материала. Кроме этого отметим, что сегодня алюминий в чистом виде стали использовать намного реже.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
Дюралюминий: состав, свойства и применение
Дюралюминий — сплав, состоящий из основы в виде алюминия с медью и добавками других металлов. Открытие технологии его изготовления произошло в самом начале девятнадцатого века работником немецкого металлургического завода. После многочисленных экспериментов он установил, что при добавлении к алюминию меди в соотношении 96% на 4% получается сплав, который при выдержке в помещении с комнатной температурой сохраняет пластичность основного элемента с повышением показателей прочности.

Дюралюминий: особенности
Само наименование сплава пошло от торговой марки Dural, под которой был начат его выпуск. В русский язык оно пришло в начале двадцатого века и обозначает целую группу сплавов с алюминием в основе. Могут встречаться различные формы, например «дуралюминий» и «дюраль».
Области применения дюралюминия
 Формула успеха дюралюминия была проста. Лёгкий вес и прочность нового продукта способствовали его быстрому распространению. Первым большим его применением стали конструкции каркаса дирижабля. Показал он себя отлично, и со временем ему находили место во всё больших отраслях машиностроения.
Формула успеха дюралюминия была проста. Лёгкий вес и прочность нового продукта способствовали его быстрому распространению. Первым большим его применением стали конструкции каркаса дирижабля. Показал он себя отлично, и со временем ему находили место во всё больших отраслях машиностроения.
Авиастроители по достоинству оценили дюраль, и она быстро стала основой самолётостроения, а также в будущем основным конструкционным материалом в производстве космической техники.
Её применяют в производстве поездов. Дюралюминий в наши дни можно встретить даже на кухне в виде многочисленных бытовых предметов. А также активно используется дюралюминиевая фольга, в которой продают кондитерские изделия.
Активно используется сплав и в строительстве. Различные трубы, листы являются частями конструкций зданий.
Используется дюраль и в автомобилестроении, помогая инженерам уменьшить вес машины, улучшая технические показатели автомобиля. Благодаря устойчивости к высоким температурам, её можно использовать и для внутренних механизмов двигателя.
Дюралюминий лучше переносит вибрацию, чем сталь, что позволило применять его в буровых работах.
Можно заметить, что не все сплавы дюралюминия пригодны для сварки. Например, при строительстве самолётов для создания конструкций из деталей дюралюминия используются заклёпки. Они могут делаться из того же сплава дюралюминия, только пригодного для сварочных работ.
Дюраль: состав сплава
С течением времени состав сплава дюрали совершенствовался, появилось множество новых видов, их различия как в составе примесей, так и способе последующей обработки.
 Al+Cu+Mg. Этот тип называется дюралюмином. В зависимости от концентрации меди и марганца в сплавах меняются и его общие свойства и характеристики. Данный вид не имеет дополнительной защиты от коррозии, потому для его эксплуатации необходимо дополнительное покрытие для защиты от влаги.
Al+Cu+Mg. Этот тип называется дюралюмином. В зависимости от концентрации меди и марганца в сплавах меняются и его общие свойства и характеристики. Данный вид не имеет дополнительной защиты от коррозии, потому для его эксплуатации необходимо дополнительное покрытие для защиты от влаги.- Al+Mg+Si. Такой тип называется «авиаль». Добавление к алюминию частей магния и кремния повысило коррозионную стойкость сплава. Для получения своих свойств сплав проходит термообработку при температуре около пятисот градусов по Цельсию и охлаждается в воде с температурой двадцать градусов с естественным старением около суток. Такая обработка позволяет эксплуатировать сплав в условиях повышенной влажности и под напряжением.
- Al+Mg, Al+Mn. Этот сплав имеет название «магналии». При его производстве не используется термическая обработка. Основными его плюсами является повышенная устойчивость к коррозии и хорошая пригодность к сварочным и паяльным работам.
Состав дюралюминия в процентах можно рассмотреть на примере состава сплава дюралюминий д16:
 Al (Алюминий): 91 — 94.7%.
Al (Алюминий): 91 — 94.7%.- Cu (Медь): 3.7−4.9%.
- Fe (Железо): 0.5%.
- Si (Кремний): 0.5%.
- Zn (Цинк): 0.25%.
- Mg (Магний): 1.1 — 1.8%.
- Cr (Хром): 0.1%.
- Mn (Марганец): 0.4% – 0.9%.
- Ti (Титан): 0.15%.
Могут добавляться маркировки, зависящие от форм выпуска сплава:
- «Т» — закалка в естественных условиях.
- «Т1» — после процесса искусственного старения.
- «А» — после покрытия специальными лаками и анодирования.
Свойства дюралюминия
 Не смотря на попытки борьбы с коррозией путём добавления марганца и магния, дюралюминий все же ей подвержен и подвержен достаточно, чтобы на это обратить внимание. Потому, при эксплуатации необходимо защитить его при помощи какого-либо покрытия. Защита должна быть настолько тщательной, насколько это возможно.
Не смотря на попытки борьбы с коррозией путём добавления марганца и магния, дюралюминий все же ей подвержен и подвержен достаточно, чтобы на это обратить внимание. Потому, при эксплуатации необходимо защитить его при помощи какого-либо покрытия. Защита должна быть настолько тщательной, насколько это возможно.
Дюраль отличается небольшим весом при большой прочности. Благодаря этому её и используют как основной конструкционный материал в космонавтике и авиации. Используется также в авиастроении, при производстве скоростных поездов и различных других областях машиностроения.
Средняя плотность дюралюминия 2500−2800 килограмм на кубический метр.
Дюралюминиевый сплав, в отличие от алюминия чистого, хорошо подходит к сварочным работам.
Обладает высокой устойчивостью воздействиям среды и низкой уязвимостью к разрушению.
Появление такого лёгкого и прочного материала позволило поднять машиностроение на новый уровень и построить такие технические проекты, которые ранее казались неосуществимыми.
Какая температура плавления алюминия по Цельсию
 Такой металл, как алюминий, очень распространен в мире. Немалое его количество содержится в организме человека, а уж в окружающем мире его еще больше. Среди материалов, из которых построены дома, а также в конструкции любого автомобиля есть некая доля алюминия.
Такой металл, как алюминий, очень распространен в мире. Немалое его количество содержится в организме человека, а уж в окружающем мире его еще больше. Среди материалов, из которых построены дома, а также в конструкции любого автомобиля есть некая доля алюминия.
Нередко из этого вещества изготавливаются детали мебели. И если вдруг что-то из этого сломается, то можно либо приобрести новый товар в соответствующем магазине, либо заняться самостоятельным ремонтом изделия. В последнем случае придется плавить металл в домашних условиях, а для этого уже нужно знать о некоторых свойствах этого металла.
Для изготовления какой-либо алюминиевой конструкции вовсе не обязательно подробно изучать все характеристики вещества, но на основные моменты следует обратить свое внимание, включая знание, при какой температуре плавится алюминий.
О температуре плавления
Необходимо помнить: алюминий очень легко поддается литью и начинает превращаться в жидкую субстанцию уже при температуре в 660 градусов. Для того чтобы понять, что этот показатель довольно низкий, достаточно сравнить его с температурами плавления других металлов, которые также нередко используются для изготовления тех или иных, нужных в обиходе предметов.
Например:
- сталь начинает плавиться лишь при температуре в 1300 градусов;
- чугун — при 1100 градусах.
Но все же, хоть температура плавления алюминия по Цельсию и не слишком высока по сравнению со многими другими металлами, достичь 600 градусов в домашних условиях с использованием обыкновенной газовой или электрической плиты довольно трудно.
Уменьшение температуры
 Прежде чем подвергать металл плавлению, можно специальными методами уменьшить его температуру плавления, например, использовать в виде порошка. В этом случае он начнет плавиться чуть быстрее. Но при этом он становится опасным, так как взаимодействуя с атмосферным кислородом, может окислиться или воспламениться. А в результате окисления, как мы помним из школьного курса химии, образуется оксид алюминия; и температура, при которой начинает плавиться это вещество, уже превышает две тысячи градусов.
Прежде чем подвергать металл плавлению, можно специальными методами уменьшить его температуру плавления, например, использовать в виде порошка. В этом случае он начнет плавиться чуть быстрее. Но при этом он становится опасным, так как взаимодействуя с атмосферным кислородом, может окислиться или воспламениться. А в результате окисления, как мы помним из школьного курса химии, образуется оксид алюминия; и температура, при которой начинает плавиться это вещество, уже превышает две тысячи градусов.
Вообще избежать образования оксида не получится, если заниматься плавлением алюминия, но уменьшить количество лишнего вещества вполне возможно. При плавлении алюминия нужно не допускать попадания в вещество воды. Ведь если это случится, то произойдет взрыв.
Перед началом процесса нужно убедиться в том, что сырье является абсолютно сухим. Чаще всего в качестве исходного материала применяется алюминиевая проволока. Предварительно ее нужно с помощью ножниц разделить на множество мелких по длине кусочков. А для того, чтобы уменьшить площадь контакта с содержащимся в атмосфере кислородом, эти кусочки прессуются пассатижами.
Не всегда есть необходимость создать алюминиевое изделие высокого качества, поэтому вовсе не обязательно всегда использовать порошок или мелко нарезанную и плотно сдавленную проволоку. Можно взять любой предмет, который уже был использован, например, банку, в которой хранились консервы. Но перед плавкой нужно лишить ее нижнего шва или обрезать профиль. Полученное сырье может быть окрашено или испачкано. Не нужно об этом беспокоиться. Все, что имеется лишнее на поверхности, быстро отходит в виде шлаков.
Процесс плавления в домашних условиях
Плавление — это довольно опасный процесс. Предварительно необходимо обязательно побеспокоиться о средствах защиты от различных ядовитых веществ, которые будут образовываться, а также подготовить литейную форму.
Средства защиты
 Не обойтись без специальных перчаток даже в том случае, если расплавить алюминий необходимо лишь единожды. Это, пожалуй, основное средство защиты, так как расплавленная масса с большой долей вероятности может попасть на руки, и тогда неминуемо на коже появится ожог, поскольку температура жидкого металла превышает 600 градусов.
Не обойтись без специальных перчаток даже в том случае, если расплавить алюминий необходимо лишь единожды. Это, пожалуй, основное средство защиты, так как расплавленная масса с большой долей вероятности может попасть на руки, и тогда неминуемо на коже появится ожог, поскольку температура жидкого металла превышает 600 градусов.- Следующая часть тела, которую также необходимо защитить от попадания горячего алюминия — глаза. При частой плавке не обойтись без специальной защитной маски, ну или хотя бы очков. Но лучше всего работать в костюме, который устойчив к воздействию высокой температуры в несколько сотен градусов.
- Если необходимо получить чистый алюминий, потребуется рафинирующий флюс. И тогда работать нужно в химическом респираторе.
Выбор формы для литья
 Для того, чтобы отлить алюминий, необязательно запасаться литейной формой. Достаточно лишь приобрести лист из более тугоплавкого металла — из стали, вылить на него расплавленный алюминий и подождать, пока последний затвердеет. Но для получения какой-либо детали из алюминия обязательно придется приобретать форму для литья.
Для того, чтобы отлить алюминий, необязательно запасаться литейной формой. Достаточно лишь приобрести лист из более тугоплавкого металла — из стали, вылить на него расплавленный алюминий и подождать, пока последний затвердеет. Но для получения какой-либо детали из алюминия обязательно придется приобретать форму для литья.
Ее можно изготовить самостоятельно в домашних условиях. Для этой цели обычно используется скульптурный гипс. Он заливается в форму, затем какое-то время охлаждается. После этого в него вставляют модель и сверху кладут вторую емкость с гипсом. При этом важно не забыть проделать отверстие в гипсе с помощью какого-нибудь предмета цилиндрической формы. Через это отверстие и будет заливаться горячий алюминий.
При плавлении алюминия не обойтись без так называемого тигеля: то есть емкости из тугоплавкого металла. Она может быть выполнена из фарфора, кварца, стали, чугуна. Впрочем, изготавливать тигель самостоятельно вовсе не обязательно, ведь его можно просто купить в специальном магазине. Объем тигеля зависит от того, какое количество металла требуется получить.
Кратко о процессе
 Плавка алюминия в домашних условиях — это не такой уж трудный процесс, которым он может показаться поначалу. Кусочки металла нагреваются до нужной температуры плавки алюминия в специальной емкости.
Плавка алюминия в домашних условиях — это не такой уж трудный процесс, которым он может показаться поначалу. Кусочки металла нагреваются до нужной температуры плавки алюминия в специальной емкости.
Некоторое время полученный расплав необходимо выдерживать в разогретом состоянии и периодически удалять с его поверхности образующийся шлак. После этого чистый жидкий металл наливается в специальную форму, в которой он некоторое время будет остывать.
Время, которое уйдет на плавку, зависит от самой печи, а точнее от той температуры, которую она может обеспечить. Если же вместо печи используется газовая горелка, то она должна нагревать металл сверху.
Как в домашних условиях плавить алюминий
Алюминий часто используется для изготовления деталей. Иногда плавят кусочки алюминия, чтобы заделать дефект, делают отливки. Плавить можно обломки дюраля, ненужные радиодетали. В обзоре представлены способы, как в домашних условиях расплавить алюминий, что для этого потребуется. Специалисты поделятся опытом, расскажут, какие свойства легкого металла необходимо учитывать, чтобы плавить металл самостоятельно.

Характеристики алюминия
Чтобы правильно плавить металл, необходимо учитывать температуру плавки алюминия. Чистый сплав легко плавится уже при +660°С, а оксидная пленка только при +2300°С. Опасно самостоятельно плавить порошок, он способен воспламениться. Кусочки алюминия плавят сухими, вода в расплаве способна спровоцировать взрыв.
Технология плавления алюминия в домашних условиях
Суть плавления состоит из нескольких этапов:
- Подготовка лома. В качестве исходного сырья используют профиль из алюминия, проволоку (ее предварительно уминают пассатижами), отслужившие детали. Кусочки должны быть небольшими. Краску, вкрапления других металлов из них не достают, все это будет в составе шлака.
- Подбор емкости, в которой можно плавить алюминий. Подойдет прочная посудина из стали (температура плавления 1300°С) или чугунок (1100°С), используют готовые огнеупорные тигли.
- Подготовка формы для расплава. В домашних условиях их делают самостоятельно. Процедура изготовления представлена ниже.
- Плавление лома. Предварительно определяют источник тепла.
- Снятие шлака, изготовление отливки. Самый простой способ плавки – аккуратно слить жидкий алюминий в подготовленную емкость или форму, шлак остается на стенках плавильной посудины. Чтобы он не прилип, требуется быстро ее охладить.
В принципе, технология промышленного и кустарного литья ничем не отличается. Лом плавят до состояния текучести. После этого отделяют расплав от шлака, сливают в заготовленные формы. Их после охлаждения отливки разбивают. Важно определить, что в результате должно получиться из жидкого алюминия. Даже если плавить металл решили ради эксперимента, емкость или форму для литья все равно необходимо приготовить. Тогда можно будет рассмотреть получившийся слиток, проверить его на пористость, чистоту, однородность структуры.
Оборудование и способы плавки
Прежде, чем плавить алюминий, выбирают место и способ разогрева металла. Два часто используемых варианта:
- В гаражах или домовладениях плавят алюминий, сооружается плавильня, ее составляют из кирпича без использования связующего раствора. В качестве опоры удобен металлический каркас, в нем должно быть отверстие для нагнетания воздуха, для этого используют пылесос или фен. Самодельная печь обкладывается углем. Емкость для плавления с ломом помещают внутрь. Для лучшего сохранения тепла кирпичи сверху накрывают листом металла.
- В домашних условиях для разогрева небольшого количества лома пользуются:
— газовой плитой, можно плавить небольшое количество лома, но выход расплава будет невысокий.
Литье плавят в стальной посуде. Для повышения скорости нагрева используют конструкцию из двух емкостей, их вставляют одна в другую с зазором 1 см. Дно большой посудины перфорируется, оно выполняет функцию пламярассекателя. Когда есть газовая горелка, совмещают нижний нагрев с верхним. Плавить металл можно быстрее.
Дополнительное оборудование
Для небольших порций лома иногда используют жестяные банки. Но эта тара ненадежная, не исключено прогорание жести. Надежнее использовать керамический или металлический огнеупорный тигель для муфельных печей. Хороший вариант – обрезанный стакан огнетушителя. Для удобства делают желоб, по которому будет стекать расплавленный алюминий. При работе используют длинные щипцы. Понадобится ложка на длинной ручке для сбора шлака.
Как сделать форму для отливки
Перед тем, как расплавить алюминий, готовят болванку для отливки. Существует несколько способов заливки жидкого расплава. Чаще используют открытый и закрытый метод. О каждом стоит рассказать подробнее.
Открытая форма
Когда плавят алюминий по открытой методике, после плавления расплав выливают в подготовленную емкость, например, жестяную банку. Алюминиевую отливку вынимают из банки в горячем виде, когда горячий расплав немного схватится сверху. Достаточно несильно постучать по емкости. Если не нужен слиток заданной геометрии, расплавленный металл выливают на любую ровную огнеупорную поверхность, он хорошо держится, не растекается, внешне напоминает ртуть.
Закрытая форма
Сложные по геометрии отливки получают в специально приготовленных формах. Она должна соответствовать параметрам детали, обычно делается разъемной. Для изготовления формы используют деталь-макет, по которому делают отливку. В качестве формующего материала используют кремнезем, он хорошо трамбуется, его несложно найти. Кремнезем заменяют:
- смесью речного песка и жидкого стекла;
- смесь песка, цемента, вместо воды добавляют тормозную жидкость;
- гипс, он удобен для сложных макетов.
Из гипса делают сплошные бесшовные формы, они одноразовые, их после застывания алюминия разбивают. Деталь-макет изготавливают из воска или пенопласта. Его помещают внутрь емкости, используемой для формы, затем заливают пустоты. Получаются ровные детали, не требующие дополнительной обработки. Когда используется гипс, его сушат в течение пары дней. Гипс боится влаги, разбухает. Он склонен к растрескиванию при высыхании. При контакте с парафином или пенопластом гипс сохраняет свою структуру, не образуется рытвин, раковин.
Полезные советы
- Расплав должен быть горячим, чтобы форма заполнялась равномерно. Его заливают, когда он приобретает консистенцию ртути.
- Сложные по конфигурации отливки делают быстро, стараются сразу залить формы, чтобы металл не успел схватиться, не образовалось перегородок и пустот.
- В гипс металл можно заливать по воску или пенопласту, от высокой температуры воск и пенопласт выгорают. Поверхность отливки будет ровной.
- Для охлаждения отливку не опускают в воду, литье потрескается.
- При расплавлении чистого алюминия применяется технология использования защитных флюсов, они предохраняют металл от окисления.
Необходимо соблюдать противопожарную безопасность, процесс литья связан с использованием открытого пламени. Важно использовать индивидуальные средства защиты: перчатки, очки.

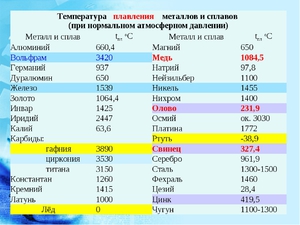 Не обойтись без специальных перчаток даже в том случае, если расплавить алюминий необходимо лишь единожды. Это, пожалуй, основное средство защиты, так как расплавленная масса с большой долей вероятности может попасть на руки, и тогда неминуемо на коже появится ожог, поскольку температура жидкого металла превышает 600 градусов.
Не обойтись без специальных перчаток даже в том случае, если расплавить алюминий необходимо лишь единожды. Это, пожалуй, основное средство защиты, так как расплавленная масса с большой долей вероятности может попасть на руки, и тогда неминуемо на коже появится ожог, поскольку температура жидкого металла превышает 600 градусов. леллингит;
леллингит; Al+Cu+Mg. Этот тип называется дюралюмином. В зависимости от концентрации меди и марганца в сплавах меняются и его общие свойства и характеристики. Данный вид не имеет дополнительной защиты от коррозии, потому для его эксплуатации необходимо дополнительное покрытие для защиты от влаги.
Al+Cu+Mg. Этот тип называется дюралюмином. В зависимости от концентрации меди и марганца в сплавах меняются и его общие свойства и характеристики. Данный вид не имеет дополнительной защиты от коррозии, потому для его эксплуатации необходимо дополнительное покрытие для защиты от влаги. Al (Алюминий): 91 — 94.7%.
Al (Алюминий): 91 — 94.7%.