Температура плавления металлов и сплавов таблица. Физические характеристики, состав и особенности металла железа
Каждый металл и сплав имеет собственный уникальный набор физических и химических свойств, среди которых не последнее место занимает температура плавления. Сам процесс означает переход тела из одного агрегатного состояния в другое, в данном случае, из твердого кристаллического состояния в жидкое. Чтобы расплавить металл, необходимо подводить к нему тепло до достижения температуры плавления. При ней он все еще может оставаться в твердом состоянии, но при дальнейшем воздействии и повышении тепла металл начинает плавиться. Если температуру понизить, то есть отвести часть тепла, элемент затвердеет.
Самая высокая температура плавления среди металлов принадлежит вольфраму : она составляет 3422С о, самая низкая — у ртути: элемент плавится уже при — 39С о. Определить точное значение для сплавов, как правило, не представляет возможности: оно может значительно колебаться в зависимости от процентного соотношения компонентов. Их обычно записывают в виде числового промежутка.
Их обычно записывают в виде числового промежутка.
Как происходит
Плавление всех металлов происходит примерно одинаково — при помощи внешнего или внутреннего нагревания. Первый осуществляется в термической печи, для второго используют резистивный нагрев при пропускании электрического тока или индукционный нагрев в высокочастотном электромагнитном поле. Оба варианта воздействуют на металл примерно одинаково.
При увеличении температуры увеличивается и амплитуда тепловых колебаний молекул , возникают структурные дефекты решетки, выражающиеся в росте дислокаций, перескоке атомов и других нарушениях. Это сопровождается разрывом межатомных связей и требует определенного количества энергии. В это же время происходит образование квази-жидкого слоя на поверхности тела. Период разрушения решетки и накопления дефектов называется плавлением.
В зависимости от температуры плавления металлы делятся на:
В зависимости от температуры плавления выбирают и плавильный аппарат .
Еще одной немаловажной величиной является температура кипения. Это величина, при которой начинается процесс кипения жидкостей, она соответствует температуре насыщенного пара, который образуется над плоской поверхностью кипящей жидкости. Обычно она почти в два раза больше, чем температура плавления.
Обе величины принято приводить при нормальном давлении. Между собой они прямопропорциональны .
- Увеличивается давление — увеличится величина плавления.
- Уменьшается давление — уменьшается величина плавления.
Таблица легкоплавких металлов и сплавов (до 600С о)
Таблица среднеплавких металлов и сплавов (от 600С о до 1600С о)
Таблица тугоплавких металлов и сплавов (свыше 1600С о)
Температура плавления химически чистого железа составляет 1539 о С. Технически чистое железо, полученное в результате окислительного рафинирования, содержит некоторое количество растворенного в металле кислорода.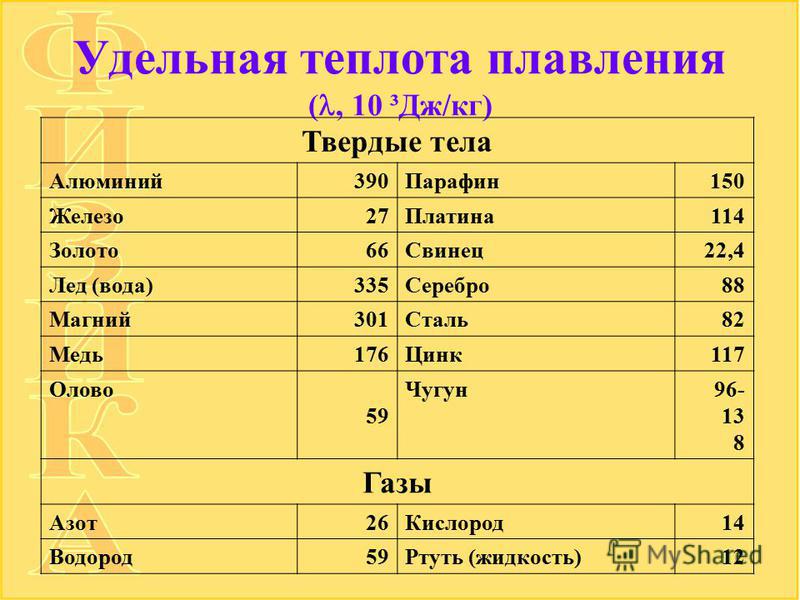
Температура плавления стали всегда ниже температуры плавления железа в связи с наличием в ней примесей. Растворенные в железе металлы (Mn, Cr, Ni. Co, Mo, V и др.) понижают температуру плавления металла на 1 – 3 о С на 1% введенного элемента, а элементы из группы металлоидов (C, O, S, P и др.) на 30 – 80 о С.
На протяжении большей части общей продолжительности плавки температура плавления металла изменяется главным образом в результате изменения содержания углерода. При концентрации углерода 0,1 – 1,2%, которая характерна для доводки плавки в сталеплавильных агрегатах, температуру плавления металла с достаточной для практических целей точностью можно оценить из уравнения
Теплота плавления железа составляет 15200 Дж/моль или 271,7 кДж/кг.
Температура кипения железа в изданиях последних лет приводится равной 2735 о С. Однако, опубликованы результаты исследований, согласно которым температура кипения железа значительно выше (до 3230 о С).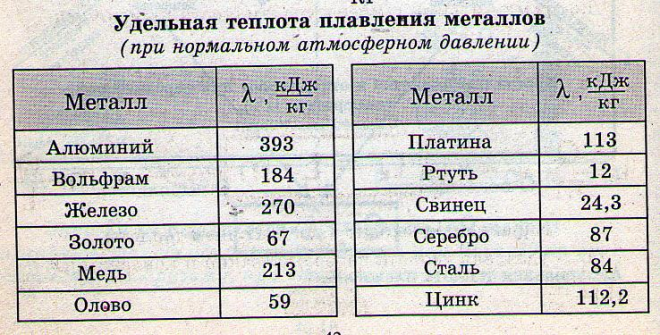
Теплота испарения железа составляет 352,5 кДж/моль или 6300 кДж/кг.
Давление насыщенного пара железа (P Fe , Па) можно оценить при помощи уравнения
где Т – температура металла, К.
Результаты расчета давления насыщенного пара железа при различных температурах, а также содержания пыли в окислительной газовой фазе над металлом (X , г/м 3) представлены в таблице 1.1.
Таблица 1.1 – Давление насыщенного пара железа и запыленность газов при разных температурах
Согласно существующим санитарным нормам содержание пыли в газах, которые выбрасываются в атмосферу, не должно превышать 0,1 г/м 3 . Из данных таблицы 1.1 видно, что при 1600 о С запыленность газов над открытой поверхностью металла выше допустимых значений. Поэтому обязательно требуется очистка газов от пыли, состоящей в основном из оксидов железа.
Динамическая вязкость . Коэффициент динамической вязкости жидкости () определяется из соотношения
где F – сила взаимодействия двух движущихся слоев, Н;
S – площадь соприкосновения слоев, м 2 ;
– градиент скорости слоев жидкости по нормали к направлению потока, с -1 .
Динамическая вязкость сплавов железа обычно изменяется в пределах 0,001 – 0,005 Па с. Ее величина зависит от температуры и содержания примесей, главным образом углерода. При перегреве металла над температурой плавления выше 25 – 30 о С влияние температуры не существенно.
Кинематическая вязкость жидкости представляет собой скорость передачи импульса в потоке единичной массы. Ее величина определяется из уравнения
где – плотность жидкости, кг/м 3 .
Величина динамической вязкости жидкого железа близка к 6 10 -7 м 2 /с.
Плотность железа при 1550 – 1650 о С равна 6700 – 6800 кг/м 3 . При температуре кристаллизации плотность жидкого металла близка к 6850 кг/м 3 . Плотность твердого железа при температуре кристаллизации равна 7450 кг/м 3 , при комнатной температуре – 7800 кг/м 3 .
Из обычных примесей наибольшее влияние на плотность расплавов железа оказывают углерод и кремний, понижая ее. Поэтому обычного состава жидкий чугун имеет плотность 6200 – 6400 кг/м 3 , твердый при комнатной температуре – 7000 – 7200 кг/м 3 .
Плотность жидкой и твердой стали занимает промежуточное положение между плотностями железа и чугуна и составляет соответственно 6500 – 6600 и 7500 – 7600 кг/м 3 .
Удельная теплоемкость жидкого металла практически не зависит от температуры. В оценочных расчетах величину ее можно принимать равной 0,88 кДж/(кг К) для чугуна и 0,84 кДж/(кг К) для стали.
Поверхностное натяжение железа имеет максимальное значение при температуре около 1550 о С. В области более высоких и низких температур величина его уменьшается. Это отличает железо от большинства металлов, для которых характерно понижение поверхностного натяжения при повышении температуры.
Поверхностное натяжение жидких сплавов железа существенно меняется в зависимости от химического состава и температуры. Обычно оно изменяется в пределах 1000 – 1800 мДж/м 2 (рисунок 1.1).
Каждый металл или сплав обладает уникальными свойствами, в число которых входит температура плавления. При этом объект переходит из одного состояния в другое, в конкретном случае становится из твёрдого жидким. Чтобы его расплавить, необходимо подвести к нему тепло и нагревать до достижения нужной температуры. В момент, когда достигается нужная точка температуры данного сплава, он ещё может остаться в твёрдом состоянии. При продолжении воздействия начинает плавиться.
Чтобы его расплавить, необходимо подвести к нему тепло и нагревать до достижения нужной температуры. В момент, когда достигается нужная точка температуры данного сплава, он ещё может остаться в твёрдом состоянии. При продолжении воздействия начинает плавиться.
Наиболее низкая температура плавления у ртути — она плавится даже при -39 °C, самая высокая у вольфрама — 3422 °C. Для сплавов (стали и других) определить точную цифру крайне сложно. Все зависит от соотношения компонентов в них. У сплавов она записывается как числовой промежуток.
Как происходит процесс
Элементы, какими бы они ни были: золото, железо, чугун, сталь или любой другой — плавятся примерно одинаково. Это происходит при внешнем или внутреннем нагревании. Внешнее нагревание осуществляется в термической печи. Для внутреннего применяют резистивный нагрев, пропуская электрический ток или индукционный нагрев в электромагнитном поле высокой частоты . Воздействие при этом примерно одинаковое.
Когда происходит нагревание , усиливается амплитуда тепловых колебаний молекул.
В зависимости от градуса, при котором плавятся металлы, они разделяются на:
- легкоплавкие — до 600 °C: свинец, цинк, олово;
- среднеплавкие — от 600 °C до 1600 °C: золото, медь, алюминий, чугун, железо и большая часть всех элементов и соединений;
- тугоплавкие — от 1600 °C: хром, вольфрам, молибден, титан.
В зависимости от того, каков максимальный градус, подбирается и плавильный аппарат. Он должен быть тем прочнее, чем сильнее будет нагревание.
Вторая важная величина — градус кипения. Это параметр, при достижении которого начинается кипение жидкостей. Как правило, она в два раза выше градуса плавления. Эти величины прямо пропорциональны между собой и обычно их приводят при нормальном давлении.
Если давление увеличивается, величина плавления тоже увеличивается. Если давление уменьшается, то и она уменьшается.
Таблица характеристик
Металлы и сплавы — непременная основа для ковки , литейного производства, ювелирной продукции и многих других сфер производства. Чтобы не делал мастер (ювелирные украшения из золота , ограды из чугуна, ножи из стали или браслеты из меди) , для правильной работы ему необходимо знать температуры, при которых плавится тот или иной элемент.
Чтобы узнать этот параметр, нужно обратиться к таблице. В таблице также можно найти и градус кипения.
Среди наиболее часто применяемых в быту элементов показатели температуры плавления такие:
- алюминий — 660 °C;
- температура плавления меди — 1083 °C;
- температура плавления золота — 1063 °C;
- серебро — 960 °C;
- олово — 232 °C. Олово часто используют при пайке, так как температура работающего паяльника составляет как раз 250–400 градусов;
- свинец — 327 °C;
- температура плавления железо — 1539 °C;
- температура плавления стали (сплав железа и углерода) — от 1300 °C до 1500 °C.
 Она колеблется в зависимости от насыщенности стали компонентами;
Она колеблется в зависимости от насыщенности стали компонентами; - температура плавления чугуна (также сплав железа и углерода) — от 1100 °C до 1300 °C;
- ртуть — -38,9 °C.
Как понятно из этой части таблицы, самый легкоплавкий металл — ртуть, которая при плюсовых температурах уже находится в жидком состоянии.
Градус кипения всех этих элементов почти вдвое, а иногда и ещё выше градуса плавления. Например, у золота он 2660 °C, у алюминия — 2519 °C , у железа — 2900 °C, у меди — 2580 °C, у ртути — 356,73 °C.
У сплавов типа стали, чугуна и прочих металлов расчёт примерно такой же и зависит от соотношения компонентов в сплаве.
Максимальная температура кипения у металлов — у рения — 5596 °C . Наибольшая температура кипения — у наиболее тугоплавящихся материалов.
Бывают таблицы, в которых также указана плотность металлов . Самым лёгким металлом является литий, самым тяжёлым — осмий. У осмия плотность выше, чем у урана и плутония, если рассматривать её при комнатной температуре. К лёгким металлам относятся: магний, алюминий, титан. К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа — очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
К лёгким металлам относятся: магний, алюминий, титан. К тяжёлым относится большинство распространённых металлов: железо, медь, цинк, олово и многие другие. Последняя группа — очень тяжёлые металлы, к ним относятся: вольфрам, золото, свинец и другие.
Ещё один показатель, встречающийся в таблицах — это теплопроводность металлов . Хуже всего тепло проводит нептуний, а лучший по теплопроводности металл — серебро. Золото, сталь, железо, чугун и прочие элементы находится посередине между этими двумя крайностями. Чёткие характеристики для каждого можно найти в нужной таблице.
Температура плавления, наряду с плотностью, относится к физическим характеристикам металлов . Температура плавления металла — температура, при которой металл переходит из твердого состояния, в котором находится в нормальном состоянии (кроме ртути), в жидкое состояние при нагревании. При плавлении объем металла практически не изменяется, поэтому на температуру плавления нормальное атмосферное давление не влияет .
Температура плавления металлов находится в диапазоне от -39 градусов Цельсия до +3410 градусов . Для большинства металлов температура плавления высокая, однако, некоторые металлы можно расплавить в домашних условиях при нагревании на обычной горелке (олово, свинец).
Классификация металлов по температуре плавления
- Легкоплавкие металлы , температура плавления которых колеблется до 600 градусов Цельсия, например цинк, олово, висмут .
- Среднеплавкие металлы , которые плавятся при температуре от 600 до 1600 градусов Цельсия: такие как алюминий, медь, олово, железо .
- Тугоплавкие металлы , температура плавления которых достигает более 1600 градусов Цельсия — вольфрам, титан, хром и др.
- — единственный металл, находящийся при обычных условиях (нормальное атмосферное давление, средняя температура окружающей среды) в жидком состоянии. Температура плавления ртути составляет порядка -39 градусов по Цельсию.

Таблица температур плавления металлов и сплавов
| Металл | Температура плавления, градусов Цельсия |
| Алюминий | 660,4 |
| Вольфрам | 3420 |
| Дюралюмин | ~650 |
| Железо | 1539 |
| Золото | 1063 |
| Иридий | 2447 |
| Калий | 63,6 |
| Кремний | 1415 |
| Латунь | ~1000 |
| Легкоплавкий сплав | 60,5 |
| Магний | 650 |
| Медь | 1084,5 |
| Натрий | 97,8 |
| Никель | 1455 |
| Олово | 231,9 |
| Платина | 1769,3 |
| Ртуть | –38,9 |
| Свинец | 327,4 |
| Серебро | 961,9 |
| Сталь | 1300-1500 |
| Цинк | 419,5 |
| Чугун | 1100-1300 |
При плавлении металла для изготовления металлических изделий-отливок от температуры плавления зависит выбор оборудования, материала для формовки металла и др.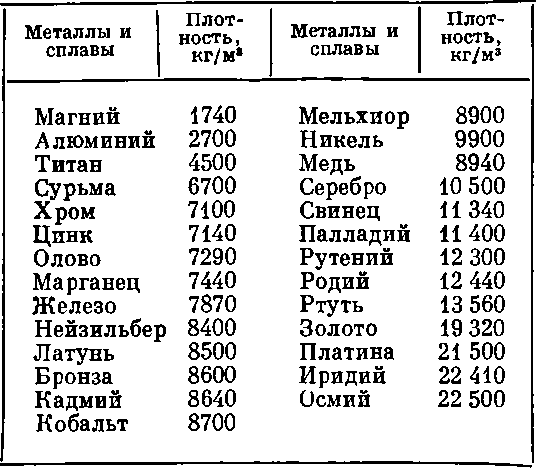 Следует также помнить, что при легировании металла другими элементами температура плавления чаще всего снижается .
Следует также помнить, что при легировании металла другими элементами температура плавления чаще всего снижается .
Интересный факт
Не стоит путать понятия «температура плавления металла» и «температура кипения металла» — для многих металлов эти характеристики существенно отличаются: так, серебро плавится при температуре 961 градус по Цельсию, а закипает только при достижении нагрева до 2180 градусов.
Температура плавления металла – это минимальная температура, при которой он переходит из твердого состояния в жидкое. При плавлении его объем практически не изменяется. Металлы классифицируют по температуре плавления в зависимости от степени нагревания.
Легкоплавкие металлы
Легкоплавкие металлы имеют температуру плавления ниже 600°C. Это цинк, олово, висмут. Такие металлы можно расплавить в домашних условиях, разогрев их на плите, или с помощью паяльника. Легкоплавкие металлы используются в электронике и технике для соединения металлических элементов и проводов для движения электрического тока.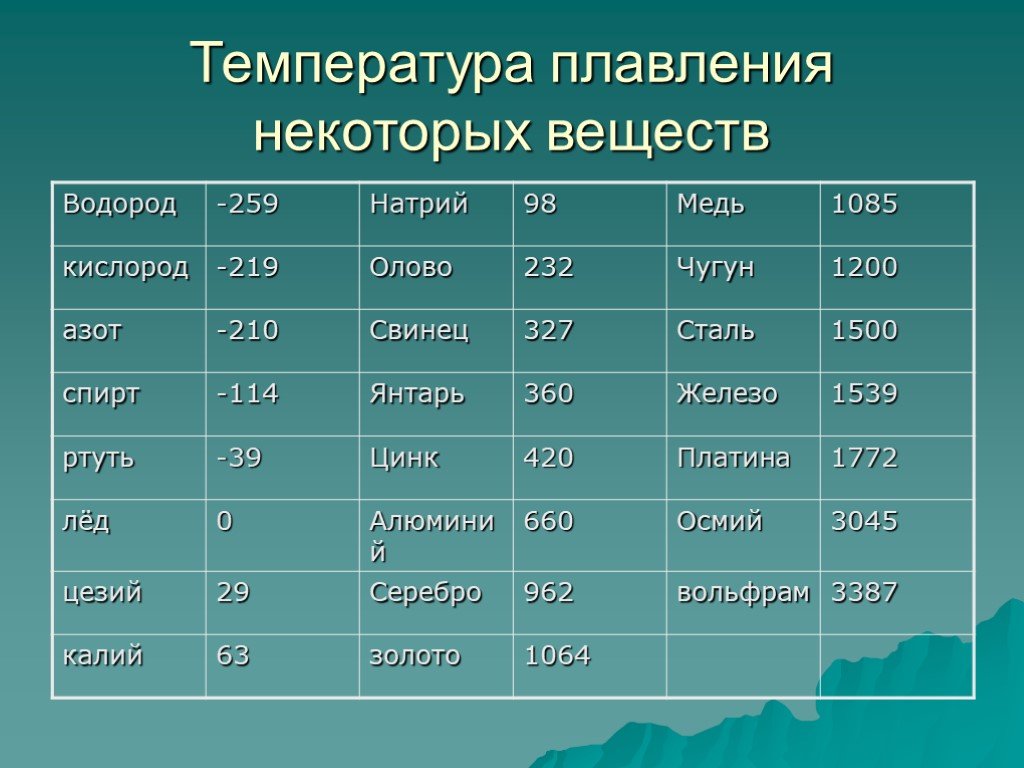 Температура плавления олова составляет 232 градуса, а цинка – 419.
Температура плавления олова составляет 232 градуса, а цинка – 419.
Среднеплавкие металлы
Среднеплавкие металлы начинают переходить из твердого в жидкое состояние при температуре от 600°C до 1600°C. Они используются для изготовления плит, арматур, блоков и других металлических конструкций, пригодных для строительства. К этой группе металлов относятся железо, медь, алюминий, они также входят в состав многих сплавов. Медь добавляют в сплавы драгоценных металлов, таких как золото, серебро, платина. Золото 750 пробы на 25% состоит из лигатурных металлов, в том числе и меди, которая придает ему красноватый оттенок. Температура плавления этого материала равна 1084 °C. А алюминий начинает плавиться при относительно низкой температуре, составляющей 660 градусов Цельсия. Это легкий пластичный и недорогой металл, который не окисляется и не ржавеет, поэтому широко используется при изготовлении посуды. Температура плавления железа равна 1539 градусов. Это один из самых популярных и доступных металлов, его применение распространено в строительстве и автомобильной промышленности. Но ввиду того, что железо подвергается коррозии, его нужно дополнительно обрабатывать и покрывать защитным слоем краски, олифы или не допускать попадания влаги.
Но ввиду того, что железо подвергается коррозии, его нужно дополнительно обрабатывать и покрывать защитным слоем краски, олифы или не допускать попадания влаги.
Тугоплавкие металлы
Температура тугоплавких металлов выше 1600°C. Это вольфрам, титан, платина, хром и другие. Их используют в качестве источников света, машинных деталей, смазочных материалов, а также в ядерной промышленности. Из них изготавливают проволоки, высоковольтные провода и используют для расплавки других металлов с более низкой температурой плавления. Платина начинает переходить из твердого в жидкое состояние при температуре 1769 градусов, а вольфрам – при температуре 3420°C.
Ртуть – единственный металл, находящийся в жидком состоянии при обычных условиях, а именно, нормальном атмосферном давлении и средней температуре окружающей среды. Температура плавления ртути составляет минус 39°C. Этот металл и его пары являются ядовитыми, поэтому он используется только в закрытых емкостях или в лабораториях. Распространенное применение ртути – градусник для измерения температуры тела.
Распространенное применение ртути – градусник для измерения температуры тела.
Железом человек начал владеть (ковать, плавить) спустя несколько тысячелетий после освоения работ с медью. Первое самородное железо в виде комков было найдено на Ближнем Востоке в 3000 году А металлургия железа, по мнению специалистов, возникла в нескольких местах планеты, разные народы осваивали этот процесс в разное время. Благодаря этому железо как материал для изготовления орудий труда, охоты и войны вытеснило камень и бронзу.
Первые процессы изготовления железа назывались сыродутными. Суть заключалась в том, что в яму засыпалась железная руда с древесным углем, который разжигали и плотно закупоривали, оставляя дутьевое отверстие, через которое подавался свежий воздух для дутья. В процессе такого нагрева температура плавления железа, конечно, не могла быть достигнута, получалась размягченная масса (крица), в которой находился шлак (зола от топлива, окислы руды и породы).
Далее полученную крицу несколько раз проковывали, удаляя шлак и другие не нужные включения, этот трудоемкий процесс производился по несколько раз, в результате чего из общей массы до финишной операции доходила пятая часть.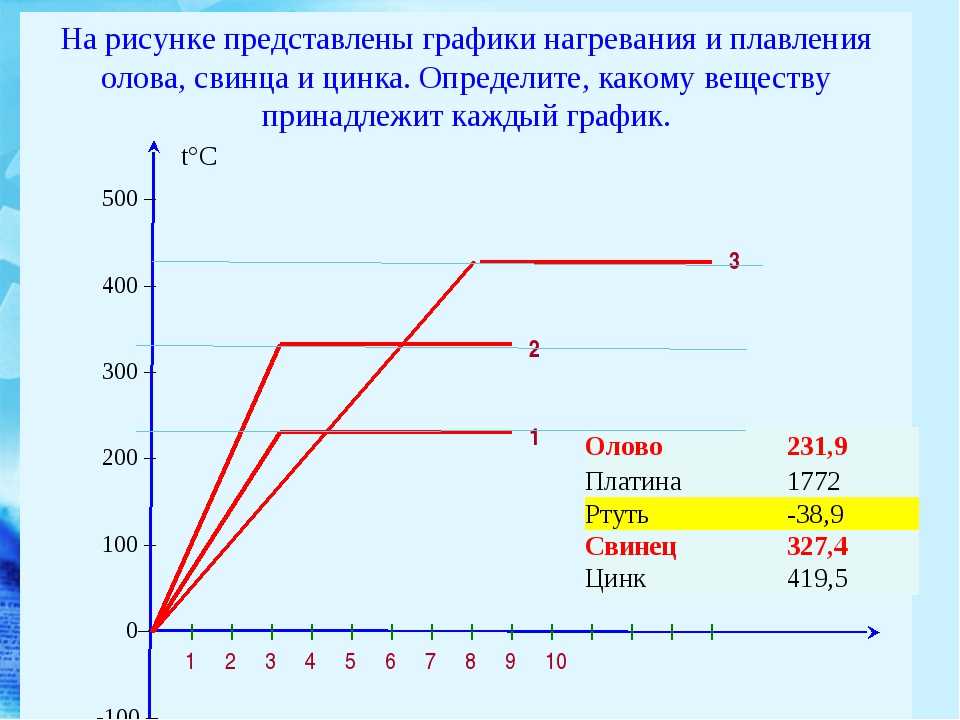 С изобретением водяного колеса появилась возможность подавать значительное количество воздуха. Благодаря такому дутью температура плавления железа стала достижимой, появился металл в жидком виде.
С изобретением водяного колеса появилась возможность подавать значительное количество воздуха. Благодаря такому дутью температура плавления железа стала достижимой, появился металл в жидком виде.
Этим металлом был чугун, который не ковался, но было замечено, что он хорошо заполняет форму. Это были первые опыты по которое с некоторыми усовершенствованиями и изменениями дошло до наших дней. Со временем был найден способ переработки чугуна в сварочное железо. Куски чугуна загружались с древесным углем, в ходе этого процесса чугун размягчался, происходило окисление примесей, в том числе углерода. В результате чего металл становился густым, температура плавления железа повышалась, т.е. получалось сварочное железо.
Таким образом, металлурги того времени смогли разделить единый процесс на две ступени. Этот двухступенчатый процесс в самой идее сохранился до настоящего времени, изменения в большей степени касаются появлению процессов, происходящих на втором этапе. Чистое железо или металл, имеющий минимум примесей, практического применения почти не имеет. Температура плавления железа по диаграмме железо — углерод находится в точке А, что соответствует 1535 градусам.
Температура плавления железа по диаграмме железо — углерод находится в точке А, что соответствует 1535 градусам.
Железа наступает при достижении отметки 3200 градусов.
На открытом воздухе железо со временем покрывается оксидной пленкой, во влажной среде появляется рыхлый слой ржавчины. Железо с момента его появления и по сегодняшний день является одним из главных металлов. Используется железо, главным образом, в виде сплавов, которые различаются по свойствам и составу.
При какой температуре плавится железо, зависит от содержания углерода и других компонентов, входящих в состав сплава. Наибольшее применение имеют углеродистые сплавы — чугун и сталь. Сплавы, содержащие углерод более 2%, называют чугуном, менее 2% относятся к стали. Чугун получают в доменных печах, путем переплава обогащенных на аглофабрике руд.
В мартеновских, электрических и индукционных печах, в конвертерах.
В качестве шихты применяется металлический лом и чугун. Путем окислительных процессов из шихты удаляется лишний углерод и вредные примеси, а добавки легирующих материалов позволяют получить нужную Для получения стали и других сплавов современные металлургия использует технологии электрошлакового переплава, вакуумные, электронно-лучевые и плазменные плавки.
В разработке находятся новые методы плавления стали, предусматривающие автоматизацию процесса и обеспечивающие получение высококачественного металла.
Научные разработки достигли такого уровня, когда можно получать материалы, выдерживающие вакуум и большое давление, большие температурные перепады, агрессивную среду, радиационные излучения и т.п.
В таблице представлена температура плавления металлов t пл , их температура кипения t к при атмосферном давлении, плотность металлов ρ при 25°С и теплопроводность λ при 27°С.
Температура плавления металлов, а также их плотность и теплопроводность приведены в таблице для следующих металлов: актиний Ac, серебро Ag, золото Au, барий Ba, берилий Be, кальций Ca, кадмий Cd, кобальт Co, хром Cr, цезий Cs, галлий Ga, гафний Hf, ртуть Hg, индий In, иридий Ir, калий K, литий Li, нептуний Np, осмий Os, протактиний Pa, свинец Pb, палладий Pd, полоний Po, плутоний Pu, радий Ra, рубидий Pb, рений Re, родий Rh, рутений Ru, сурьма Sb, стронций Sr, тантал Ta, технеций Tc, торий Th, таллий Tl, уран U, ванадий V, цинк Zn, цирконий Zr.
По данным таблицы видно, что температура плавления металлов изменяется в широком диапазоне (от -38,83°С у до 3422°С у вольфрама). Низкой положительной температурой плавления обладают такие металлы, как литий (18,05°С), цезий (28,44°С), рубидий (39,3°С) и другие щелочные металлы.
Наиболее тугоплавкими являются следующие металлы: гафний, иридий, молибден, ниобий, осмий, рений, рутений, тантал, технеций, вольфрам. Температура плавления этих металлов выше 2000°С.
Приведем примеры температуры плавления металлов , широко применяемых в промышленности и в быту:
- температура плавления алюминия 660,32 °С;
- температура плавления меди 1084,62 °С;
- температура плавления свинца 327,46 °С;
- температура плавления золота 1064,18 °С;
- температура плавления олова 231,93 °С;
- температура плавления серебра 961,78 °С;
- температура плавления ртути -38,83°С.
Максимальной температурой кипения из металлов, представленных в таблице, обладает рений Re — она составляет 5596°С. Также высокими температурами кипения обладают металлы, относящиеся к группе с высокой температурой плавления.
Также высокими температурами кипения обладают металлы, относящиеся к группе с высокой температурой плавления.
В таблице находится в диапазоне от 0,534 до 22,59 , то есть самым легким металлом является , а самым тяжелым металлом осмий. Следует отметить, что осмий имеет плотность большую, чем и даже плутония при комнатной температуре.
В таблице изменяется от 6,3 до 427 Вт/(м·град), таким образом хуже всего проводит тепло такой металл, как нептуний, а лучшим теплопроводящим металлом является серебро.
Температура плавления стали
Представлена таблица значений температуры плавления стали распространенных марок. Рассмотрены стали для отливок, конструкционные, жаропрочные, углеродистые и другие классы сталей.
Температура плавления стали находится в диапазоне от 1350 до 1535°С. Стали в таблице расположены в порядке возрастания их температуры плавления.
| Сталь | t пл, °С | Сталь | t пл, °С |
|---|---|---|---|
| Стали для отливок Х28Л и Х34Л | 1350 | Коррозионно-стойкая жаропрочная 12Х18Н9Т | 1425 |
| Сталь конструкционная 12Х18Н10Т | 1400 | Жаропрочная высоколегированная 20Х23Н13 | 1440 |
| Жаропрочная высоколегированная 20Х20Н14С2 | 1400 | Жаропрочная высоколегированная 40Х10С2М | 1480 |
| Жаропрочная высоколегированная 20Х25Н20С2 | 1400 | Сталь коррозионно-стойкая Х25С3Н (ЭИ261) | 1480 |
| Сталь конструкционная 12Х18Н10 | 1410 | Жаропрочная высоколегированная 40Х9С2 (ЭСХ8) | 1480 |
| Коррозионно-стойкая жаропрочная 12Х18Н9 | 1410 | Коррозионно-стойкие обыкновенные 95Х18…15Х28 | 1500 |
| Сталь жаропрочная Х20Н35 | 1410 | Коррозионно-стойкая жаропрочная 15Х25Т (ЭИ439) | 1500 |
| Жаропрочная высоколегированная 20Х23Н18 (ЭИ417) | 1415 | Углеродистые стали | 1535 |
Источники:
- Волков А.
 И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с. - Физические величины. Справочник. А. П. Бабичев, Н. А. Бабушкина, А. М. Братковский и др.; Под ред. И. С. Григорьева, Е. З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с.
таблица по возрастанию в градусах, самая высокая температура плавления
Таблица температур плавления
Узнать какая нужна температура для плавления металлов, поможет таблица по возрастанию температурных показателей.
| Элемент или соединение | Необходимый температурный режим |
| Литий | +18°С |
| Калий | +63,6°С |
| Индий | +156,6°С |
| Олово | +232°С |
| Таллий | +304°С |
| Кадмий | +321°С |
| Свинец | +327°С |
| Цинк | +420°С |
Таблица плавления среднеплавких металлов и сплавов.
| Элемент либо сплав | Температурный режим |
| Магний | +650°С |
| Алюминий | +660°С |
| Барий | +727°С |
| Серебро | +960°С |
| Золото | +1063°С |
| Марганец | +1246°С |
| Медь | +1083°С |
| Никель | +1455°С |
| Кобальт | +1495°С |
| Железо | +1539°С |
| Дюрали | +650°С |
| Латуни | +950…1050°С |
| Чугун | +1100…1300°С |
| Углеродистые стали | +1300…1500°С |
| Нихром | +1400°С |
Таблица плавления тугоплавких металлов и сплавов.
| Наименование элемента | Температурный режим |
| Титан | +1680°С |
| Платина | +1769,3°С |
| Хром | +1907°С |
| Цирконий | +1855°С |
| Ванадий | +1910°С |
| Иридий | +2447°С |
| Молибден | +2623°С |
| Тантал | +3017°С |
| Вольфрам | +3420°С |
Как был открыт галлий
Существование галлия было предсказано Д. И. Менделеевым в 1871 на основании сформулированного им . Менделеев дал этому элементу название «экаалюминий» и предсказал у него такие свойства как плотность, температуру плавления. Также Менделеев предсказал:
- характер оксида,
- связь в соединениях с хлором.

- что металл будет медленно растворяться в кислотах и щелочах;
- он не будет реагировать с воздухом;
- оксид экаалюминия M₂O₃ должен реагировать с кислотами с образованием солей MX₃;
- что он должен образовывать основные соли;
- хлорид обладает большей летучестью, чем ZnCl₂;
- что этот элемент откроют с помощью спектроскопии.
Менделеев оказался Ностардамусом в химии: когда галлий был получен, все предсказанные ученым свойства подтвердились!
В 1875 году французский химик Поль Эмиль Лекок де Буабодран изучал сфалерит с помощью спектроскопии и обнаружил две фиолетовые линии, принадлежащие новому элементу. Год спустя ученый выделил новый элемент с помощью электролиза. Этот элемент Буабодран назвал в честь латинского названия Франции — Gallia. Существует легенда, что в это название ученый вкладывал и другой смысл. Лекок созвучно с французским le coq
, т.е. «петух» (на латыни
gallus
). Буабодран как бы ненароком увековечил свое имя в названии нового элемента.
Изучая полученный галлий, Буабодран определил, что плотность отличается от предсказанной Менделеевым. Когда Менделеев узнал об этом, то написал французскому коллеге с рекомендацией . И как оказалось, не напрасно: первые данные Буабодрана действительно были неверными.
Что такое температура плавления
Каждый металл имеет неповторимые свойства, и в этот список входит температура плавления. При плавке металл уходит из одного состояния в другое, а именно из твёрдого превращается в жидкое. Чтобы сплавить металл, нужно приблизить к нему тепло и нагреть до необходимой температуры – этот процесс и называется температурой плавления. В момент, когда температура доходит до нужной отметки, он ещё может пребывать в твёрдом состоянии. Если продолжать воздействие – металл или сплав начнет плавиться.
Интересное: Особенности сварки алюминия
Плавление и кипение – это не одно и то же. Точкой перехода вещества из твердого состояния в жидкое, зачастую называют температуру плавления металла. В расплавленном состоянии у молекул нет определенного расположения, но притяжение сдерживает их рядом, в жидком виде кристаллическое тело оставляет объем, но форма теряется.
В расплавленном состоянии у молекул нет определенного расположения, но притяжение сдерживает их рядом, в жидком виде кристаллическое тело оставляет объем, но форма теряется.
При кипении объем теряется, молекулы между собой очень слабо взаимодействуют, движутся хаотично в разных направлениях, совершают отрыв от поверхности. Температура кипения – это процесс, при котором давление металлического пара приравнивается к давлению внешней среды.
Для того, чтобы упростить разницу между критическими точками нагрева мы подготовили для вас простую таблицу:
| Свойство | Температура плавки | Температура кипения |
| Физическое состояние | Сплав переходит в расплав, разрушается кристаллическая структура, проходит зернистость | Переходит в состояние газа, некоторые молекулы могут улетать за пределы расплава |
| Фазовый переход | Равновесие между твердым состоянием и жидким | Равновесие давления между парами металла и воздухом |
| Влияние внешнего давления | Нет изменений | Изменения есть, температура уменьшается при разряжении |
При какой температуре плавится
Металлические элементы, какими бы они ни были — плавятся почти один в один.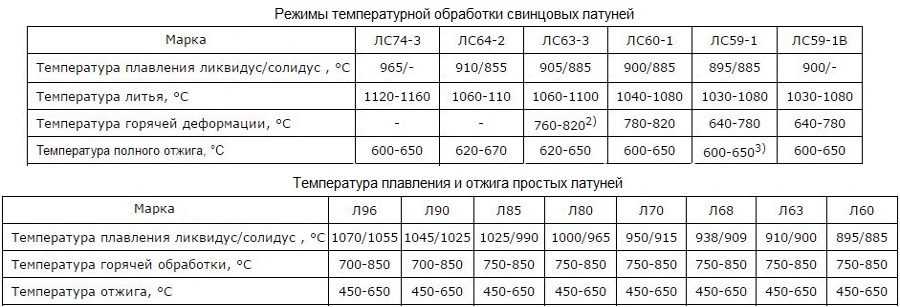 Этот процесс происходит при нагреве. Оно может быть, как внешнее, так и внутреннее. Первое проходит в печи, а для второго используют резистивный нагрев, пропуская электричество либо индукционный нагрев. Воздействие выходит практически схожее. При нагреве, увеличивается амплитуда колебаний молекул. Образуются структурные дефекты решётки, которые сопровождаются обрывом межатомных связей. Под процессом разрушения решётки и скоплением подобных дефектов и подразумевается плавление.
Этот процесс происходит при нагреве. Оно может быть, как внешнее, так и внутреннее. Первое проходит в печи, а для второго используют резистивный нагрев, пропуская электричество либо индукционный нагрев. Воздействие выходит практически схожее. При нагреве, увеличивается амплитуда колебаний молекул. Образуются структурные дефекты решётки, которые сопровождаются обрывом межатомных связей. Под процессом разрушения решётки и скоплением подобных дефектов и подразумевается плавление.
У разных веществ разные температуры плавления. Теоретически, металлы делят на:
- Легкоплавкие – достаточно температуры до 600 градусов Цельсия, для получения жидкого вещества.
- Среднеплавкие – необходима температура от 600 до 1600 ⁰С.
- Тугоплавкие – это металлы, для плавления которых требуется температура выше 1600 ⁰С.
Плавление железа
Температура плавления железа достаточно высока. Для технически чистого элемента требуется температура +1539 °C. В этом веществе имеется примесь — сера, а извлечь ее допустимо лишь в жидком виде.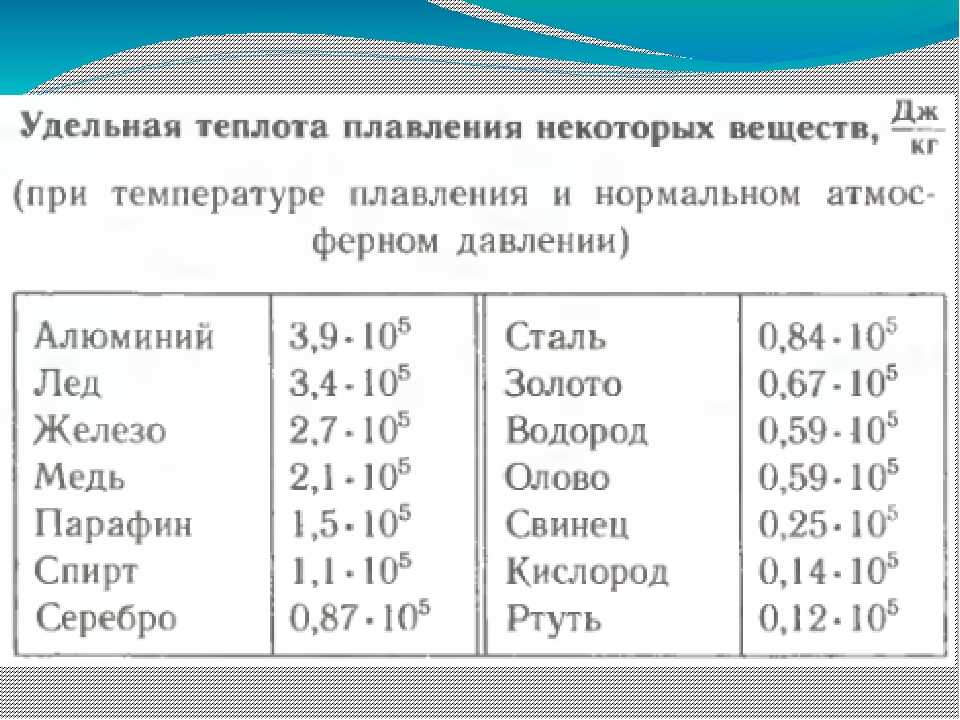
Интересное: Контроль неразрушающий соединения сварные методы ультразвуковые
Без примесей чистый материал можно получить при электролизе солей металла.
Плавление чугуна
Чугун – это лучший металл для плавки. Высокий показатель жидкотекучести и низкий показатель усадки дают возможность эффективнее пользоваться им при литье. Далее рассмотрим показатели температуры кипения чугуна в градусах Цельсия:
- Серый — температурный режим может достигать отметки 1260 градусов. При заливке в формы температура может подниматься до 1400.
- Белый — температура достигает отметки 1350 градусов. В формы заливается при показателе 1450.
Важно! Показатели плавления такого металла, как чугун – на 400 градусов ниже, по сравнению со сталью. Это значительно снижает затраты энергии при обработке.
Плавление стали
Температура плавления и кипения железа
Температура кипения и плавления металлов
В таблице представлена температура плавления металлов tпл, их температура кипения tк при атмосферном давлении, плотность металлов ρ при 25°С и теплопроводность λ при 27°С.
Температура плавления металлов, а также их плотность и теплопроводность приведены в таблице для следующих металлов: актиний Ac, серебро Ag, алюминий Al, золото Au, барий Ba, берилий Be, висмут Bi, кальций Ca, кадмий Cd, кобальт Co, хром Cr, цезий Cs, медь Cu, железо Fe, галлий Ga, гафний Hf, ртуть Hg, индий In, иридий Ir, калий K, литий Li, магний Mg, марганец Mn, молибден Mo, натрий Na, ниобий Nb, никель Ni, нептуний Np, осмий Os, протактиний Pa, свинец Pb, палладий Pd, полоний Po, платина Pt, плутоний Pu, радий Ra, рубидий Pb, рений Re, родий Rh, рутений Ru, сурьма Sb, олово Sn, стронций Sr, тантал Ta, технеций Tc, торий Th, титан Ti, таллий Tl, уран U, ванадий V, вольфрам W, цинк Zn, цирконий Zr.
По данным таблицы видно, что температура плавления металлов изменяется в широком диапазоне (от -38,83°С у ртути до 3422°С у вольфрама). Низкой положительной температурой плавления обладают такие металлы, как литий (18,05°С), цезий (28,44°С), рубидий (39,3°С) и другие щелочные металлы.
Наиболее тугоплавкими являются следующие металлы: гафний, иридий, молибден, ниобий, осмий, рений, рутений, тантал, технеций, вольфрам. Температура плавления этих металлов выше 2000°С.
Приведем примеры температуры плавления металлов, широко применяемых в промышленности и в быту:
- температура плавления алюминия 660,32 °С;
- температура плавления меди 1084,62 °С;
- температура плавления свинца 327,46 °С;
- температура плавления золота 1064,18 °С;
- температура плавления олова 231,93 °С;
- температура плавления серебра 961,78 °С;
- температура плавления ртути -38,83°С.
Максимальной температурой кипения из металлов, представленных в таблице, обладает рений Re — она составляет 5596°С. Также высокими температурами кипения обладают металлы, относящиеся к группе с высокой температурой плавления.
Плотность металлов в таблице находится в диапазоне от 0,534 до 22,59 г/см 3 , то есть самым легким металлом является литий, а самым тяжелым металлом осмий. Следует отметить, что осмий имеет плотность большую, чем плотность урана и даже плутония при комнатной температуре.
Следует отметить, что осмий имеет плотность большую, чем плотность урана и даже плутония при комнатной температуре.
Теплопроводность металлов в таблице изменяется от 6,3 до 427 Вт/(м·град), таким образом хуже всего проводит тепло такой металл, как нептуний, а лучшим теплопроводящим металлом является серебро.
Температура плавления стали
Представлена таблица значений температуры плавления стали распространенных марок. Рассмотрены стали для отливок, конструкционные, жаропрочные, углеродистые и другие классы сталей.
Температура плавления стали находится в диапазоне от 1350 до 1535°С. Стали в таблице расположены в порядке возрастания их температуры плавления.
| Сталь | tпл, °С | Сталь | tпл, °С |
|---|---|---|---|
| Стали для отливок Х28Л и Х34Л | 1350 | Коррозионно-стойкая жаропрочная 12Х18Н9Т | 1425 |
| Сталь конструкционная 12Х18Н10Т | 1400 | Жаропрочная высоколегированная 20Х23Н13 | 1440 |
| Жаропрочная высоколегированная 20Х20Н14С2 | 1400 | Жаропрочная высоколегированная 40Х10С2М | 1480 |
| Жаропрочная высоколегированная 20Х25Н20С2 | 1400 | Сталь коррозионно-стойкая Х25С3Н (ЭИ261) | 1480 |
| Сталь конструкционная 12Х18Н10 | 1410 | Жаропрочная высоколегированная 40Х9С2 (ЭСХ8) | 1480 |
| Коррозионно-стойкая жаропрочная 12Х18Н9 | 1410 | Коррозионно-стойкие обыкновенные 95Х18…15Х28 | 1500 |
| Сталь жаропрочная Х20Н35 | 1410 | Коррозионно-стойкая жаропрочная 15Х25Т (ЭИ439) | 1500 |
| Жаропрочная высоколегированная 20Х23Н18 (ЭИ417) | 1415 | Углеродистые стали | 1535 |
- Волков А.
 И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с. - Казанцев Е. И. Промышленные печи. Справочное руководство для расчетов и проектирования.
- Физические величины. Справочник. А. П. Бабичев, Н. А. Бабушкина, А. М. Братковский и др.; Под ред. И. С. Григорьева, Е. З. Мейлихова. — М.: Энергоатомиздат, 1991. — 1232 с.
Металлы плавятся, как правило, при очень высокой температуре, которая может достигать более 3 тыс. градусов. Хотя некоторые из них можно расплавить в домашних условиях, например, свинец или олово. А вот ртуть плавят при температуре минус 39 градусов. В домашних условиях этого добиться не удастся. Температура плавления — это один из важных показателей производства не только самого металла, но и его сплавов. Выплавляя сырье, специалисты учитывают и другие физические и химические свойства руды и металла.
Железо и его свойства
Железо — это химический элемент, который в таблице Менделеева находится под номером 26. Это один из самых распространенных элементов во всей Солнечной системе. Согласно материалам исследований, в составе ядра Земли находится примерно 79−85% этого вещества. В земной коре его тоже присутствует большое количество, но оно уступает алюминию.
Это один из самых распространенных элементов во всей Солнечной системе. Согласно материалам исследований, в составе ядра Земли находится примерно 79−85% этого вещества. В земной коре его тоже присутствует большое количество, но оно уступает алюминию.
В чистом виде металл имеет белый цвет с чуть серебристым оттенком. Он пластичен, но имеющиеся в нем примеси могут определять его физические свойства. Реагирует на магнит.
Железо присутствует в воде. В речных водах его концентрация равна примерно 2 мг/л металла. В морской воде его содержание может быть ниже в сто или даже тысячу раз.
Оксид железа — это основная форма, добыча которой осуществляется и которая находится в природе. Оксидное железо может располагаться в самой верхней части земной коры и быть составляющей осадочных образований.
Элемент, находящийся на двадцать шестом месте в таблице Менделеева, может иметь несколько степеней окисления. Именно они определяют его геохимическую особенность нахождения в определенной среде.
В ядре Земли металл присутствует в нейтральной форме.
Добыча полезных ископаемых
Руд, в которых присутствует железо, существует несколько. Однако, в качестве сырья для производства железа в промышленности используют в основном следующие:
- магнезитовую руду;
- гетитовую руду;
- гематитовую руду.
А также часто встречаются такие разновидности руды:
- леллингит;
- сидерит;
- марказит;
- ильменит;
- ярозит.
Существует еще минерал под названием мелантерит. Его используют преимущественно в фармацевтической промышленности. Из себя он представляет зелёного цвета хрупкие кристаллы, в которых присутствует стеклянный блеск. Из него производят лекарственные препараты, в составе которых имеется ферум.
Основным месторождением этого металла является Южная Америка, а именно Бразилия.
Плавление железа и необходимая температура
Точкой плавления металла называют такую минимальную температуру, при которой он переходит из твердого состояния в жидкое. При этом в объеме он практически остается неизменным.
При этом в объеме он практически остается неизменным.
Металл могут производить из руды различными способами, но самый основной из них — это доменный. Помимо доменного, используют еще выплавку железа при помощи обжига измельченной руды с примесью глины. Из полученной смеси формируют окатыши, которые обрабатываются в печи с последующим восстановлением водородом. Далее плавление железа осуществляется в электрической печи.
Температура плавления железа весьма высока. Для технически чистого элемента она составляет +1539 °C. В этом веществе присутствует примесь — Сера, которую можно извлечь лишь в жидком виде. Без примесей чистый материал получают при электролизе солей металла.
Классификация металлов по температуре плавления
Разные металлы могут переходить в жидкое состояние при разной температуре. Вследствие этого выделяют определённую классификацию. Их делят следующим образом:
- Легкоплавкие — те элементы, которые могут становиться жидкими уже при температуре ниже 600 градусов.
 К ним относят цинк, олово, свинец и пр. Их можно расплавить даже в домашних условиях — просто нужно разогреть при помощи плиты или паяльника. Такие виды нашли применение в технике и электронике. Они используются для соединения элементов из металла и движения электрического тока. Олово плавится при 232 градусах, а цинк — при 419 градусах.
К ним относят цинк, олово, свинец и пр. Их можно расплавить даже в домашних условиях — просто нужно разогреть при помощи плиты или паяльника. Такие виды нашли применение в технике и электронике. Они используются для соединения элементов из металла и движения электрического тока. Олово плавится при 232 градусах, а цинк — при 419 градусах. - Среднеплавкие — элементы, которые начинают расплавляться при температуре от шестисот до тысячи шестисот градусов. Эти элементы используют по большей части для строительных элементов и металлоконструкций, то есть при создании арматур, плит и строительных блоков. В эту группу входят: железо, медь, алюминий. Температура плавления алюминия сравнительно низка и составляет 660 градусов. А вот железо начинает переходить в жидкое состояние лишь при температуре 1539 градусов. Это один из самых распространенных металлов, используемых в промышленности, особенно в автомобильной. Однако железо подвержено коррозии, то есть ржавчине, поэтому ему требуется специальная поверхностная обработка.
 Его необходимо покрывать краской или олифой, и не допускать попадание влаги.
Его необходимо покрывать краской или олифой, и не допускать попадание влаги. - Тугоплавкие — это такие материалы, которые расплавляются и становятся жидкими при температуре выше 1600 градусов. В эту группу относят вольфрам, титан, платину, хром и т. п. Они используются в ядерной промышленности и для некоторых машинных деталей. Они могут применяться для расплавки других металлов, изготовления высоковольтных проводов или проволоки. Платину можно расплавить при 1769 градусах, а вольфрам — при 3420 °C.
Единственный элемент, который при обычных условиях находится в жидком состоянии — это ртуть. Температура его плавления составляет минус 39 градусов и его пары являются ядовитыми, поэтому его используют только в лабораториях и закрытых ёмкостях.
Каждый металл и сплав имеет собственный уникальный набор физических и химических свойств, среди которых не последнее место занимает температура плавления. Сам процесс означает переход тела из одного агрегатного состояния в другое, в данном случае, из твердого кристаллического состояния в жидкое. Чтобы расплавить металл, необходимо подводить к нему тепло до достижения температуры плавления. При ней он все еще может оставаться в твердом состоянии, но при дальнейшем воздействии и повышении тепла металл начинает плавиться. Если температуру понизить, то есть отвести часть тепла, элемент затвердеет.
Сам процесс означает переход тела из одного агрегатного состояния в другое, в данном случае, из твердого кристаллического состояния в жидкое. Чтобы расплавить металл, необходимо подводить к нему тепло до достижения температуры плавления. При ней он все еще может оставаться в твердом состоянии, но при дальнейшем воздействии и повышении тепла металл начинает плавиться. Если температуру понизить, то есть отвести часть тепла, элемент затвердеет.
Самая высокая температура плавления среди металлов принадлежит вольфраму: она составляет 3422С о , самая низкая — у ртути: элемент плавится уже при — 39С о . Определить точное значение для сплавов, как правило, не представляет возможности: оно может значительно колебаться в зависимости от процентного соотношения компонентов. Их обычно записывают в виде числового промежутка.
Как происходит
Плавление всех металлов происходит примерно одинаково — при помощи внешнего или внутреннего нагревания. Первый осуществляется в термической печи, для второго используют резистивный нагрев при пропускании электрического тока или индукционный нагрев в высокочастотном электромагнитном поле.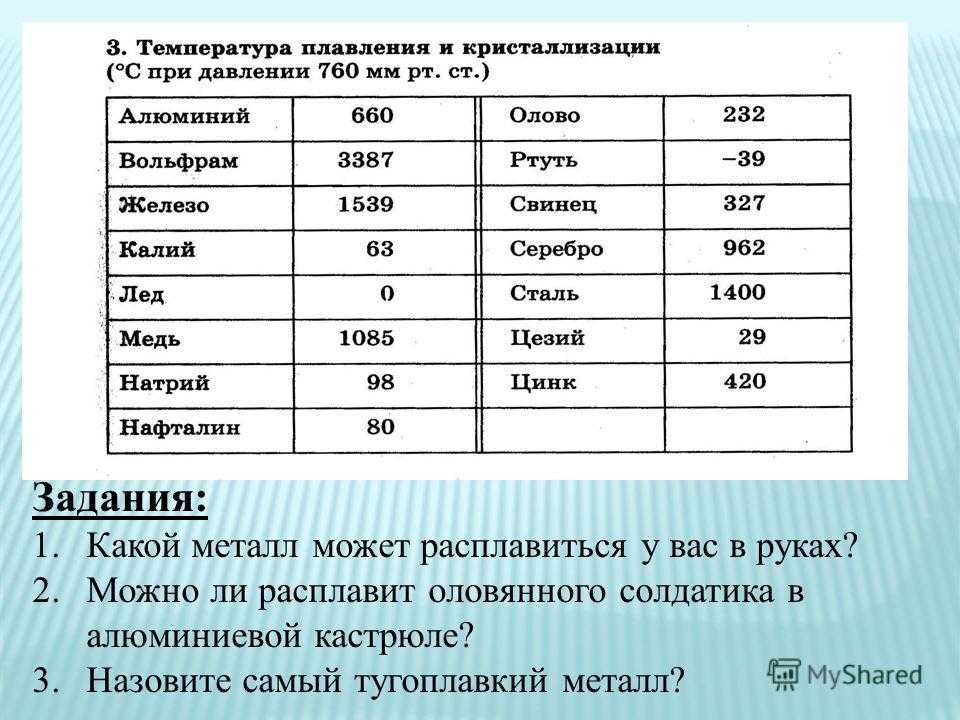 Оба варианта воздействуют на металл примерно одинаково.
Оба варианта воздействуют на металл примерно одинаково.
При увеличении температуры увеличивается и амплитуда тепловых колебаний молекул, возникают структурные дефекты решетки, выражающиеся в росте дислокаций, перескоке атомов и других нарушениях. Это сопровождается разрывом межатомных связей и требует определенного количества энергии. В это же время происходит образование квази-жидкого слоя на поверхности тела. Период разрушения решетки и накопления дефектов называется плавлением.
Разделение металлов
В зависимости от температуры плавления металлы делятся на:
- Легкоплавкие: им необходимо не более 600С о . Это цинк, свинец, виснут, олово.
- Среднеплавкие: температура плавления колеблется от 600С о до 1600С о . Это золото, медь, алюминий, магний, железо, никель и большая половина всех элементов.
- Тугоплавкие: требуется температура свыше 1600С о , чтобы сделать металл жидким. Сюда относятся хром, вольфрам, молибден, титан.
В зависимости от температуры плавления выбирают и плавильный аппарат. Чем выше показатель, тем прочнее он должен быть. Узнать температуру нужного вам элемента можно из таблицы.
Чем выше показатель, тем прочнее он должен быть. Узнать температуру нужного вам элемента можно из таблицы.
Еще одной немаловажной величиной является температура кипения. Это величина, при которой начинается процесс кипения жидкостей, она соответствует температуре насыщенного пара, который образуется над плоской поверхностью кипящей жидкости. Обычно она почти в два раза больше, чем температура плавления.
Обе величины принято приводить при нормальном давлении. Между собой они прямопропорциональны.
точек плавления/замерзания обычных материалов
точек плавления/замерзания обычных материалов Температура плавления/замерзания |
| Абсолютный ноль | 8+32″> -459.670 | -273,15 | * |
| Водород | -434,824 | -259,347 | * |
| Аргон | -308.820 | -189,344 | * |
| Меркурий | -38,8344 | * | |
| Вода | 32.018 | 0,01 | * |
| Галлий | 85,576 | 29.7646 | * |
| Индий | 87729999999999″ x:fmla=»=+C7*1.8+32″> 313.877 | 156,5985 | * |
| Ведущий | 325.400 | 163 | |
| Олово | 449.543 | 231.9681 | * |
| Цинк | 787.244 | 419,58 | * |
| Магний | 1202.000 | 650 | |
| Алюминий | 1220.581 | 660.323 | * |
| Бронза | 1675.400 | 913 | |
| Латунь | 8+32″> 1700.600 | 927 | |
| Серебро | 1763.204 | 961,78 | * |
| Золото | 1947.524 | 1064.18 | * |
| Медь | 1981.400 | 1083 | |
| Чугун | 2199.200 | 1204 | |
| Сталь | 2499.800 | 1371 | |
| Никель | 2647.400 | 1453 | |
| Кованое железо | 8+32″> 2699.600 | 1482 | |
| Железо | 2795.000 | 1535 | |
| Платина | 3221.600 | 1772 | |
| Вольфрам | 6150.200 | 3399 |
(*) означает стандарт метрологии.
Примечание. Для большинства веществ температура плавления и замерзания точка одинаковая.
Точка плавления золота — Детекторы горнодобывающего оборудования для поиска золота Защита от змей
- Силовые шлюзы/высокие банки
- Шлюзовые коробки
- Ле Трап — Гео Шлюз
- Золотой колодец Вихревой шлюз
- Шлюзы Dream Mat
- Покрытие для шлюза
- Золотой куб
- Спиральный кастрюля Desert Fox
- Ручные земснаряды
- Черная магия
- Концентратор с синей чашей
- Аляска Пайдирт
- Колорадо Пайдирт
- Чистое извлечение золота
- Силовой шлюз CC 690
- Камнедробилки
- Золотые барабаны
- Пылесос Vac Pac Gold
- Стаканы для камней
- Кирки, лопаты и многое другое
- Плавление золота
- Принадлежности для разведки
- Приятель Вудмана
- Классификатор землетрясений
- Золотые классификаторы
- Золотые кастрюли и комплекты
- Золотой коготь
- Сумки для инструментов
- Защита от змей
- Подарочные сертификаты
Металлодетекторы
- Garrett
- Металлоискатели Fisher
- Электроскопы
- Технетика
- Охотник за головами
- Пинпоинтеры
Информация
- О нас/Контакты
- Доставка/возврат
- Поисковый блог
- Ссылки/Ресурсы
- Предметы для разведки
|
Общие виды металлов, их свойства и применение
Металл — это материал, хорошо проводящий электричество и тепло. Металл имеет блестящий вид, когда он только что создан, отполирован или разбит. Металлы можно вытягивать в проволоку или сбивать молотком в тонкие листы (ковкие) (пластичные). Металлы имеют высокую температуру плавления и менее склонны к распаду при воздействии экстремальных температур. Металлы также более прочные, прочные и твердые, чем их пластиковые аналоги. Доступны тысячи различных типов металлов, каждый из которых был произведен для определенной цели. Мы составили информативное руководство, которое поможет вам узнать о некоторых из самых популярных металлов и о том, как они используются.
Подробнее: различные типы металлов и их классификации
Содержание
- 1 Типы металлов
- 1,1 Сталь:
- 1,2 Карбонная сталь:
- 1,3 1.
 3. Железо:
3. Железо: - 1,6 Железо свиньи:
- 1,7 чугун:
- 1,8 кованый железо:
- 1,9 Присоединяйтесь к нашему новостному бюллетеню
- 1.10 Алюминиевые0278 1.13 Bronze:
- 1.14 Cobalt:
- 1.14.1 Periodic Table of Metals:
- 1.15 Magnesium:
- 1.16 Silicon:
- 1.17 Silver:
- 1.18 Gold:
- 1.19 Nickel:
- 1.20 Lead :
- 1.21 Олово:
- 1.22 Цинк:
- 1.23 Титан:
- 1.24 Вольфрам:
- 1.25 Пожалуйста, поделитесь!
Различные типы металлов, которые сегодня распространены в промышленности, включают сталь, углеродистую сталь, легированную сталь, нержавеющую сталь, железо, чугун, чугун, кованое железо, алюминий, медь, латунь, бронзу, кобальт, Магний, никель, свинец, олово, цинк, титан, вольфрам, кремний, серебро и золото.
Сталь:
Сталь представляет собой химический сплав, состоящий из железа и углерода, улучшающий прочность и устойчивость материала к излому. Он сделан в основном из железа и углерода с большим содержанием углерода до 2%. Сталь является наиболее часто используемым материалом в мире для инфраструктуры и промышленности. Все, от швейных иголок до нефтяных танкеров, делается из него. Сталь используется в конструкциях, инструментах, автомобилях, машинах, электрическом оборудовании и оружии из-за ее высокой прочности на растяжение и низкой стоимости.
Он сделан в основном из железа и углерода с большим содержанием углерода до 2%. Сталь является наиболее часто используемым материалом в мире для инфраструктуры и промышленности. Все, от швейных иголок до нефтяных танкеров, делается из него. Сталь используется в конструкциях, инструментах, автомобилях, машинах, электрическом оборудовании и оружии из-за ее высокой прочности на растяжение и низкой стоимости.
Подробнее: Понимание порошковой металлургии
Углеродистая сталь:
Углеродистая сталь определяется как сталь, свойства которой в основном зависят от содержания углерода и содержат не более 0,5 процента кремния и 1,5 процента марганца. Хотя некоторые другие элементы могут быть добавлены в очень небольших количествах, именно основная сталь содержит углерод и железо. Углеродистая сталь подразделяется на три категории: низкоуглеродистая, среднеуглеродистая и высокоуглеродистая сталь. Больше углерода означает, что продукт тверже и прочнее, тогда как меньше углерода означает, что продукт дешевле и мягче. Из-за высокого содержания углерода, который помогает лезвию сохранять остроту, эта сталь обычно используется в производстве ножей.
Из-за высокого содержания углерода, который помогает лезвию сохранять остроту, эта сталь обычно используется в производстве ножей.
Легированная сталь:
Легированная сталь — это сталь, в которую помимо углерода добавлены элементы в количестве, достаточном для придания специфических для металла свойств. Марганец, ванадий, хром, никель и вольфрам являются одними из легирующих элементов. Обычно это делается для улучшения прочности, твердости, ударной вязкости, сопротивления истиранию и износу материала, а также его электрических и магнитных свойств. Это очень распространенный металл, поскольку его производство все еще очень недорого. Из этой стали изготавливают трубы, особенно для энергетических применений.
Подробнее: Разница между металлами и неметаллами
Нержавеющая сталь:
Этот тип металла определяется как сталь, устойчивая к окислению и коррозии в агрессивных средах при непосредственной термообработке и полировке. Она также известна как нержавеющая сталь, потому что она содержит не менее 11% хрома, который предотвращает ржавление железа, а также обеспечивает термостойкость. Углерод, азот, кремний, сера, титан, медь и другие элементы содержатся в различных разновидностях нержавеющей стали. Кухонные инструменты, ножи, столы, посуда и все остальное, что соприкасается с едой, сделано из нержавеющей стали. Они также использовали в двигателях и машинах детали, подвергающиеся высоким нагрузкам, такие как стержни, листы и проволока.
Углерод, азот, кремний, сера, титан, медь и другие элементы содержатся в различных разновидностях нержавеющей стали. Кухонные инструменты, ножи, столы, посуда и все остальное, что соприкасается с едой, сделано из нержавеющей стали. Они также использовали в двигателях и машинах детали, подвергающиеся высоким нагрузкам, такие как стержни, листы и проволока.
Железо:
Железо — это химический элемент, обозначенный символом Fe. Он принадлежит к первому переходному ряду периодической таблицы и группе 8. Несмотря на то, что это был очень старый металл в «железном веке», он все еще имеет множество современных применений. Железо является наиболее широко используемым и наименее дорогим металлом на планете. Чугун, чугун и кованое железо — это три типа железа, которые можно найти.
Подробнее: Понимание процессов промышленной обработки металлов
Чугун:
Это вид железа, который используется в качестве сырья для производства других черных металлов, включая чугун, кованое железо и сталь.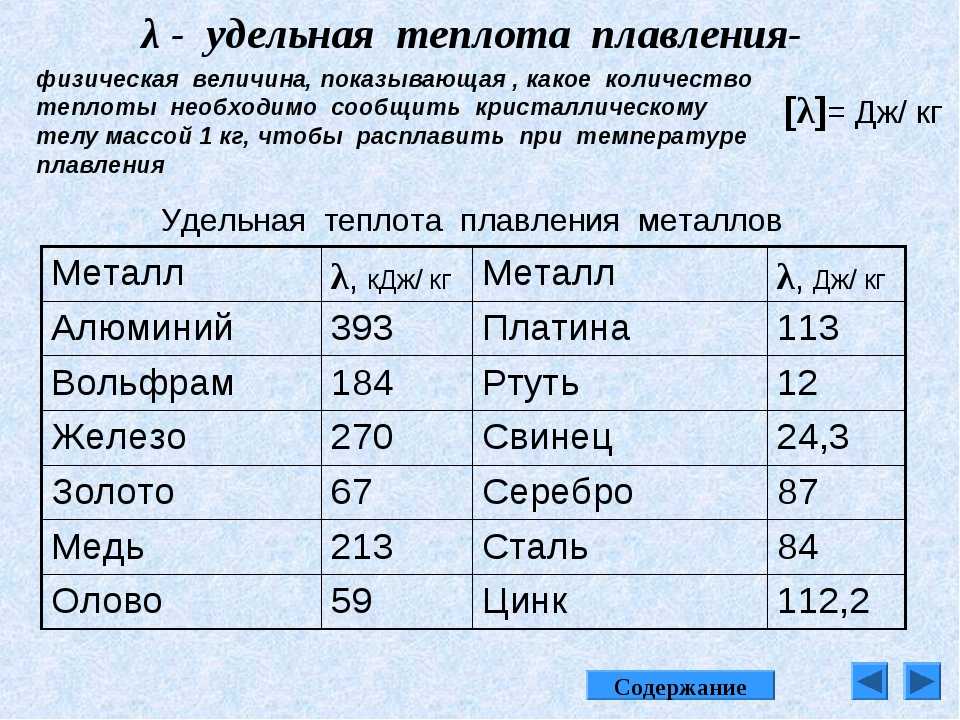 Плавка необработанных железных руд в доменной печи производит эти утюги. Вместе с кремнеземом и другими заполнителями чугун имеет очень высокое содержание углерода — 3,8–4,7%. В результате он чрезвычайно хрупок и имеет лишь несколько применений в качестве материала. Это железо обычно находится в электродуговой печи, которая используется для производства стали.
Плавка необработанных железных руд в доменной печи производит эти утюги. Вместе с кремнеземом и другими заполнителями чугун имеет очень высокое содержание углерода — 3,8–4,7%. В результате он чрезвычайно хрупок и имеет лишь несколько применений в качестве материала. Это железо обычно находится в электродуговой печи, которая используется для производства стали.
Чугун:
Чугун получают путем плавки чугуна, кокса и известняка в вагранке. Это основной источник железа и углерода. Чугун имеет процент углерода в диапазоне от 1,7 процента до 4,5 процента. Также присутствуют небольшое количество кремния, марганца, фосфора и серы. Его нельзя использовать в секциях, чувствительных к ударам, потому что это хрупкий материал. Чугун обладает прекрасными литейными качествами, а также большой прочностью, износостойкостью и приемлемой стоимостью.
Кованое железо:
В отличие от чугуна, эти типы металлов представляют собой сплавы железа с очень низким процентным содержанием углерода, примерно 0,08 процента. Кованое железо обладает различными механическими свойствами, включая ударную вязкость, пластичность и коррозионную стойкость. Кроме того, они легко свариваются, но их труднее сваривать электрическим током. Небольшие количества силикатного шлака отлиты в нити из этих металлов, которые представляют собой металлы высокой чистоты. Для кузнечных работ, таких как ковка, присутствие шлака может быть выгодным. Ограждения, садовая мебель и ворота — это лишь некоторые из вещей, сделанных из них.
Кованое железо обладает различными механическими свойствами, включая ударную вязкость, пластичность и коррозионную стойкость. Кроме того, они легко свариваются, но их труднее сваривать электрическим током. Небольшие количества силикатного шлака отлиты в нити из этих металлов, которые представляют собой металлы высокой чистоты. Для кузнечных работ, таких как ковка, присутствие шлака может быть выгодным. Ограждения, садовая мебель и ворота — это лишь некоторые из вещей, сделанных из них.
Подпишитесь на нашу рассылку новостей
Подробнее: Что такое кованое железо
Алюминий:
Алюминий – это металл с атомным номером 13 и символом Al. Это легкий голубовато-белый металл с удельным весом 2,7 и температурой плавления 658 градусов по Цельсию. Плотность металла составляет около одной трети плотности стали, что делает его менее плотным, чем другие популярные металлы. Металл в чистом виде был бы слабым и кашеобразным для большинства применений, но при смешивании с небольшим количеством других сплавов он становится прочным и жестким. В результате его можно было штамповать, формовать, вытягивать, точить, отливать, выковывать и, наконец, отливать под давлением. Он обладает высокой электропроводностью, что является важным качеством для воздушных кабелей. Из этого материала также изготавливают детали для самолетов и автомобилей.
В результате его можно было штамповать, формовать, вытягивать, точить, отливать, выковывать и, наконец, отливать под давлением. Он обладает высокой электропроводностью, что является важным качеством для воздушных кабелей. Из этого материала также изготавливают детали для самолетов и автомобилей.
Подробнее: Термическая обработка алюминия и алюминиевых сплавов
Медь:
Медь — это химический элемент с атомным номером 29 и символом Cu. Это красновато-коричневый металл, мягкий, ковкий и пластичный. Он имеет удельный вес 8,9 и температуру плавления 1083°C. Медь не находится в чистом виде под землей. Обладает отличной электропроводностью. Литье, ковка, прокатка и проволока — все это варианты металла. Он широко используется в производстве электрических проводов и проводов, а также электроприборов и оборудования, гальванопластики и гальваники, чеканки монет и домашней утвари.
Подробнее: Термическая обработка меди и медных сплавов
Латунь:
Латунь — это наиболее широко используемый сплав меди и цинка в современном мире.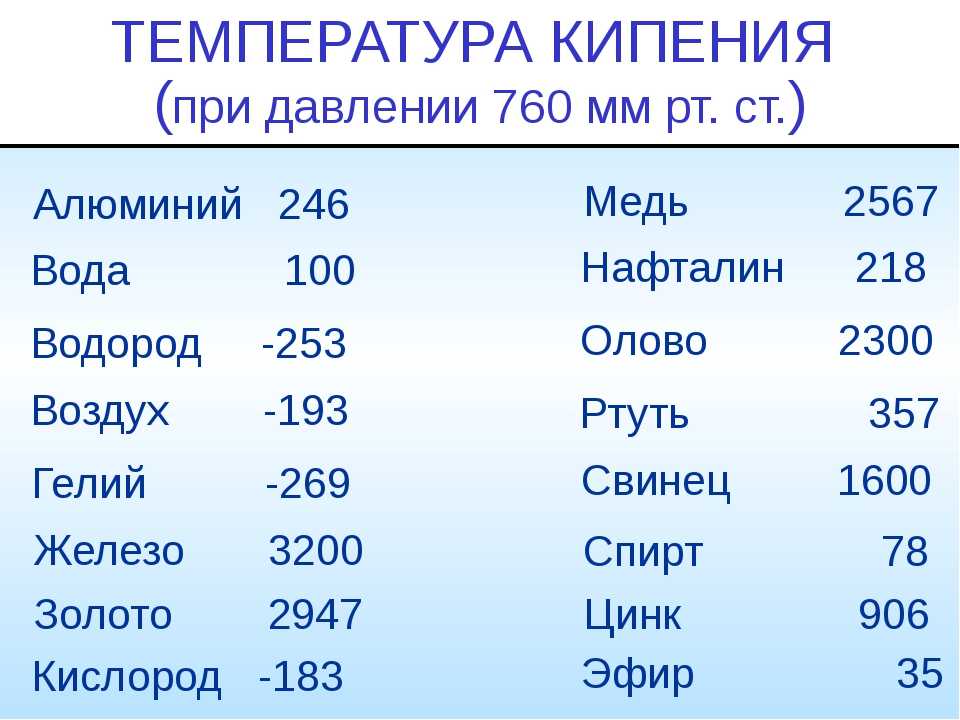 Доступны различные сорта латуни, в зависимости от соотношения меди и цинка. Качества латуни можно резко изменить, введя небольшое количество других элементов, которые могут быть механическими, электрическими или химическими. Латунь более прочна, чем медь, хотя имеет меньшую тепло- и электропроводность. Они чрезвычайно устойчивы к воздушной коррозии и просты в пайке. Могут быть обнаружены замки, шестерни, приводы, клапаны и другие часто используемые предметы.
Доступны различные сорта латуни, в зависимости от соотношения меди и цинка. Качества латуни можно резко изменить, введя небольшое количество других элементов, которые могут быть механическими, электрическими или химическими. Латунь более прочна, чем медь, хотя имеет меньшую тепло- и электропроводность. Они чрезвычайно устойчивы к воздушной коррозии и просты в пайке. Могут быть обнаружены замки, шестерни, приводы, клапаны и другие часто используемые предметы.
Бронза:
Бронза — это термин, используемый для описания сплавов меди и олова. От 75 до 95 процентов меди и от 5 до 25 процентов олова являются наиболее полезными пропорциями. Эти металлы довольно твердые, обладают высокой стойкостью к поверхностному износу, легко поддаются формованию или прокатке в проволоку, стержни и листы. Бронзы превосходят латуни, потому что они имеют лучшую коррозионную стойкость. Бронза также более плавится, а это означает, что ее легче расплавить и, следовательно, легче отлить. Трубная арматура, насосы, шестерни, корабли и лопасти турбин изготавливаются из алюминиевых бронз, которые отливаются или куются.
Подробнее: Разница между цветными и черными металлами
Кобальт:
Химический элемент кобальт имеет символ Co и атомный номер 27. Его физические свойства идентичны свойствам железа с добавлением никеля. Кобальт — прочный, блестящий металл серебристо-серого цвета, получаемый методом восстановительной плавки. Кобальт можно найти в растениях и животных, а также в воздухе, воде, почве и горных породах. Переносимая ветром пыль или дождевая вода также могут смыть богатую кобальтом почву и камни, что позволит им проникнуть в другие места обитания. Его содержат многие сплавы, в том числе используемые для создания деталей авиационных двигателей, газовых турбин, быстрорежущей стали.
Периодическая таблица металлов:
Магний:
Магний, обычно известный как Mg, представляет собой химический элемент с атомным номером 12 и символом Mg. Это глянцевое серое твердое вещество с множеством общих физических и химических свойств.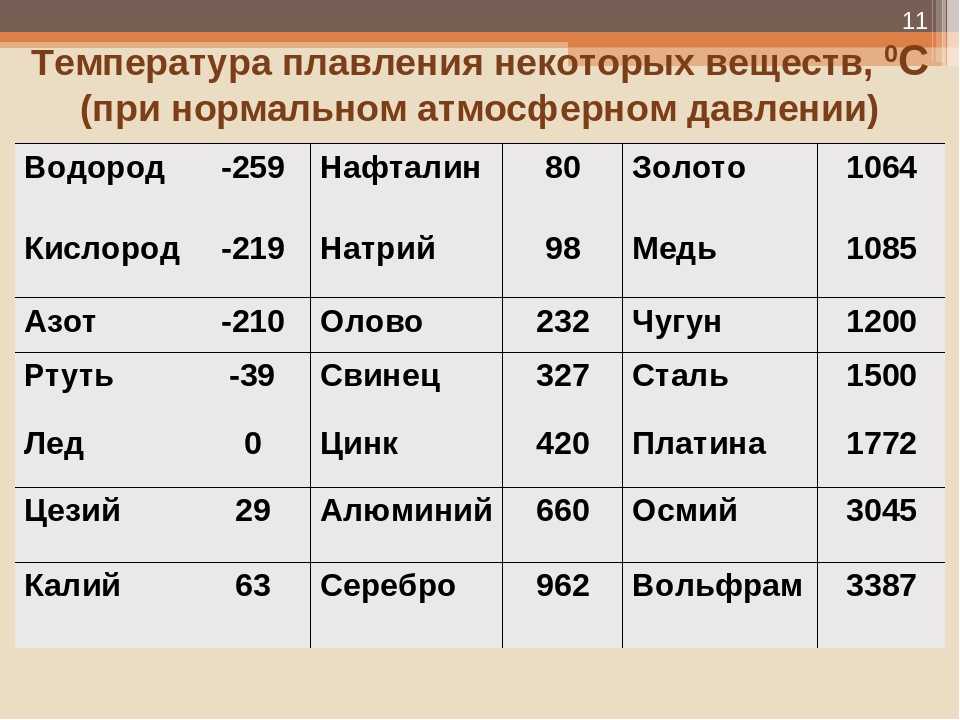 Это самый легкий металл, предел прочности литого металла на разрыв 910 кг/см2. Эти виды металлов прочнее алюминия и легко поддаются механической обработке. Они также допускают полировку под буферным кругом. Из-за его низкой плотности 1,74 его предпочитают, когда приоритетом является потеря веса. Из этих металлов изготавливают листы, проволоку, прутки, трубы и другие изделия.
Это самый легкий металл, предел прочности литого металла на разрыв 910 кг/см2. Эти виды металлов прочнее алюминия и легко поддаются механической обработке. Они также допускают полировку под буферным кругом. Из-за его низкой плотности 1,74 его предпочитают, когда приоритетом является потеря веса. Из этих металлов изготавливают листы, проволоку, прутки, трубы и другие изделия.
Подробнее: Различные типы цветных металлов и их применение
Кремний:
Кремний имеет символ Si и атомный номер 14 и является химическим элементом. Это голубовато-серый металл, твердый, хрупкий и твердый. Только кислород превосходит кремний как второй по распространенности элемент в земной коре. Он имеет температуру плавления 1414 градусов по Цельсию и температуру кипения 3265 градусов по Цельсию. Из-за использования хорошо зарекомендовавших себя процедур обработки он стоит недорого. Его можно найти в плитах динамо и трансформаторов, блоках двигателей, головках цилиндров, а также при изготовлении станков и в других местах.
Серебро:
Серебро имеет атомный номер 47 и обозначается символом Ag. Это мягкий, белый, глянцевый переходный металл с самой высокой электропроводностью и теплопроводностью среди всех переходных металлов. Это свободная самородная форма самородного серебра, которая в чистом виде встречается в земной коре. Это золотой сплав с добавлением нескольких других металлов. Серебро традиционно считалось ценным металлом, и многие инвестиционные монеты сделаны из него. Серебро используется в солнечных батареях, очистке воды, ювелирных изделиях, дорогой столовой посуде и посуде, а также в наличных деньгах. Из его смесей также изготавливают фото- и рентгеновскую пленку.
Золото:
Золото является переходным металлом, что означает, что оно находится в той же колонке, что и серебро и медь в периодической таблице. Его атомный номер 79, и он представлен символом Au. В чистом виде золото представляет собой ослепительный, светло-оранжево-желтого оттенка, плотный, мягкий, ковкий и пластичный металл. Золото — один из древнейших металлов, известных человечеству, он был открыт египтянами. Он также исторически служил символом процветания и красоты. Золото — редкий материал, который на протяжении всей истории использовался для изготовления монет, ювелирных изделий и других произведений искусства.
Золото — один из древнейших металлов, известных человечеству, он был открыт египтянами. Он также исторически служил символом процветания и красоты. Золото — редкий материал, который на протяжении всей истории использовался для изготовления монет, ювелирных изделий и других произведений искусства.
Никель:
Эти типы металлов имеют свой химический элемент с атомным номером 28 и символом Ni. Это серебристо-белый металл, который можно отполировать до блеска. Он имеет удельный вес 8,85 и температуру плавления 1452°C. Кроме того, он почти такой же твердый, как мягкая сталь. Он обладает довольно гибкими свойствами, когда в нем мало углерода. Он менее пластичен, чем мягкая сталь, однако при низком содержании магния пластичность резко улучшается. Он обычно используется в качестве декоративного и антикоррозионного покрытия для других металлов, таких как сталь, медь, латунь и т. д.
Подробнее: Понимание процесса обработки и станка
Свинец:
Свинец — это химический элемент с атомным номером 82 и символом Pb. Он тяжелее большинства обычных материалов и имеет более высокую плотность. Эти металлы более мягкие и пластичные, а также имеют более низкую температуру плавления. Он имеет удельный вес 1,36 и температуру плавления 326°C. Это голубовато-серый металл с удельным весом 1,36. Поскольку это мягкий металл, его легко резать лезвием. Также не хватает стойкости. Свинец обычно используется для изготовления припоев, а также для покрытия резервуаров с кислотой, цистерн и водопроводных труб, а также для покрытия электрических кабелей.
Он тяжелее большинства обычных материалов и имеет более высокую плотность. Эти металлы более мягкие и пластичные, а также имеют более низкую температуру плавления. Он имеет удельный вес 1,36 и температуру плавления 326°C. Это голубовато-серый металл с удельным весом 1,36. Поскольку это мягкий металл, его легко резать лезвием. Также не хватает стойкости. Свинец обычно используется для изготовления припоев, а также для покрытия резервуаров с кислотой, цистерн и водопроводных труб, а также для покрытия электрических кабелей.
Олово:
Химический символ олова — Sn, а его атомный номер — 50. Олово — серебристый металл с легким желтым оттенком. Олово достаточно мягкое, чтобы резать его с небольшим усилием, а полоску олова можно легко согнуть вручную. Это блестящий белый металл, мягкий, ковкий и пластичный. Металл можно очень просто раскатать в очень тонкий лист. Олово обычно используется для изготовления тонкого припоя для основных сплавов, в качестве защитного покрытия для железных и стальных листов, а также для производства оловянной фольги для влагонепроницаемой упаковки.
Цинк:
Цинк — это химический элемент с символом Zn и атомным номером 30. Когда окисление не происходит, цинк представляет собой хрупкий металл серебристо-коричневого цвета. Цинк имеет удельный вес 7,1 и температуру плавления 420°C. Эти типы металлов используются для покрытия стальных листов при производстве оцинкованного железа из-за их высокой устойчивости к воздушной коррозии. Цинк скатывается в листы и используется, среди прочего, в качестве кровельного покрытия и влагонепроницаемой, неагрессивной облицовки контейнеров. Другие известные применения цинка включают изготовление латуни и литье под давлением на основе цинка.
Титан:
Этот тип металла также имеет символ Ti и атомный номер 22. Титан — красивый переходный металл с серебристым оттенком, низкой плотностью, большой прочностью и коррозионной стойкостью, который можно найти в природе. Это легкий, высокопрочный металл с низкой коррозией, который используется в качестве сплава в деталях высокоскоростной авиации.

 Она колеблется в зависимости от насыщенности стали компонентами;
Она колеблется в зависимости от насыщенности стали компонентами;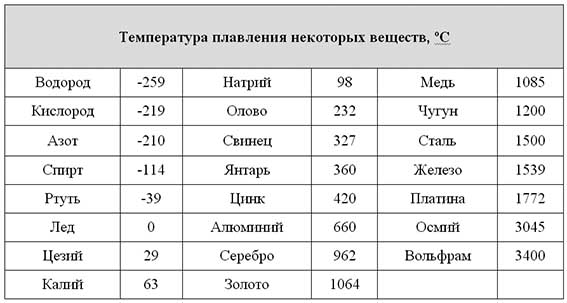
 И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
 И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с.
И., Жарский И. М. Большой химический справочник. — М: Советская школа, 2005. — 608 с. В ядре Земли металл присутствует в нейтральной форме.
В ядре Земли металл присутствует в нейтральной форме.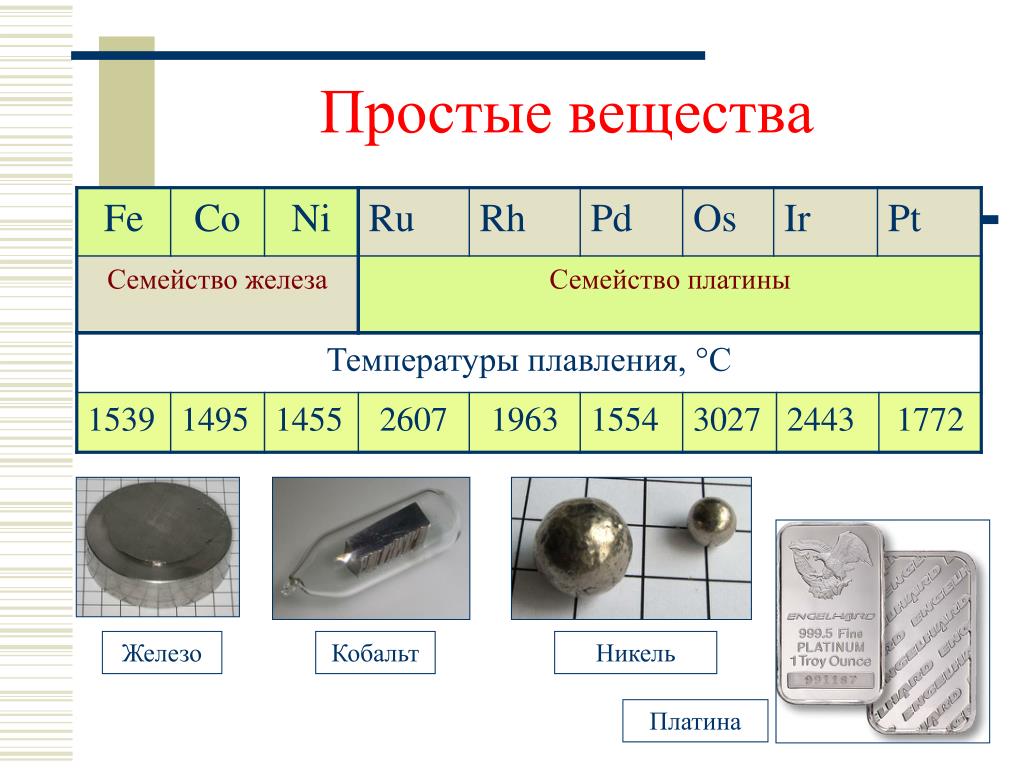 К ним относят цинк, олово, свинец и пр. Их можно расплавить даже в домашних условиях — просто нужно разогреть при помощи плиты или паяльника. Такие виды нашли применение в технике и электронике. Они используются для соединения элементов из металла и движения электрического тока. Олово плавится при 232 градусах, а цинк — при 419 градусах.
К ним относят цинк, олово, свинец и пр. Их можно расплавить даже в домашних условиях — просто нужно разогреть при помощи плиты или паяльника. Такие виды нашли применение в технике и электронике. Они используются для соединения элементов из металла и движения электрического тока. Олово плавится при 232 градусах, а цинк — при 419 градусах.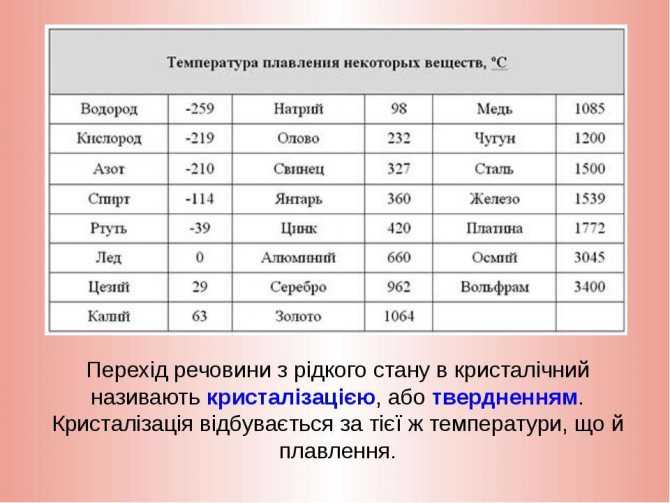 Его необходимо покрывать краской или олифой, и не допускать попадание влаги.
Его необходимо покрывать краской или олифой, и не допускать попадание влаги.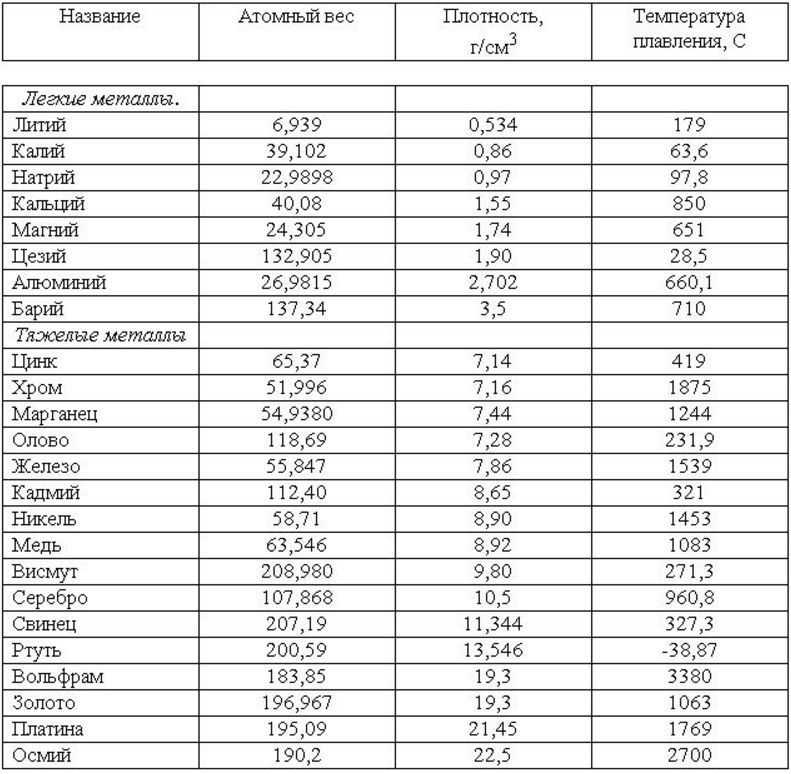 Сплавы с более низким весом в каратах, обычно 22k, 18k, 14k или 10k, содержат более высокие проценты меди или других неблагородных металлов, серебра или палладия в сплаве.
Сплавы с более низким весом в каратах, обычно 22k, 18k, 14k или 10k, содержат более высокие проценты меди или других неблагородных металлов, серебра или палладия в сплаве.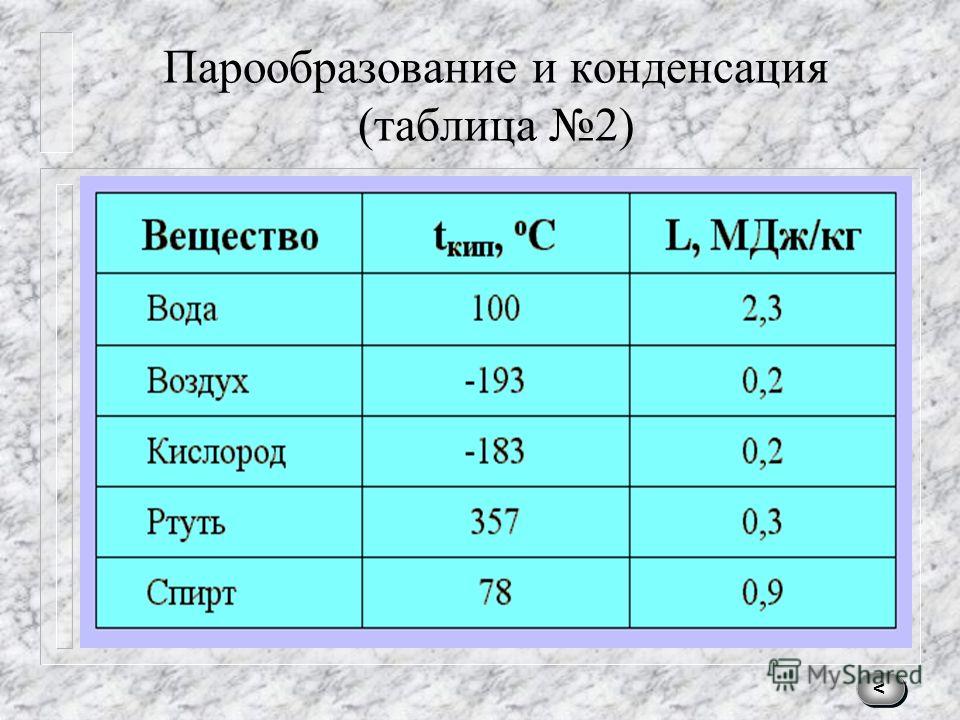 Обычные цветные сплавы золота, такие как розовое золото, могут быть созданы путем добавления различных количеств меди и серебра.
Обычные цветные сплавы золота, такие как розовое золото, могут быть созданы путем добавления различных количеств меди и серебра. Это относится к «сжиганию» примесей, с которыми может быть смешано ваше золото, в результате чего получается почти чистое золото.
Это относится к «сжиганию» примесей, с которыми может быть смешано ваше золото, в результате чего получается почти чистое золото.
 3. Железо:
3. Железо: