Никель — что это за металл?
Никель — металл с атомным номером 28. Обозначается символом Ni. Он имеет серебристо-белый оттенок, в нормальных условиях покрывается оксидной пленкой. Благодаря своей пластичности, никель легко поддается ковке.
Физические свойства
Никель — ферромагнетик, то есть при температуре ниже точки Кюри он обладает намагниченностью при отсутствии внешнего магнитного поля. Для никеля точка Кюри составляет 358 ⁰С. Металл не тускнеет на открытом воздухе.
Основные физические свойства никеля:
- Структура решетки — кубическая гранецентрированая.
- Плотность при нормальных условиях — 8,902 г/см3.
- Температура плавления — 1453 ⁰С.
- Удельная теплота плавления — 17,61 кДж/моль.
- Температура кипения – 3000 ⁰С.
- Удельная теплота испарения — 378,6 кДж/моль.
- Молярная теплоемкость — 26,1 Дж/(K*моль)
- Удельная теплоемкость — 0,440 кдж/(кг*К).
- Теплопроводность — 90,9 Вт/(м*К).
- Удельное электрическое сопротивление — 0,0684 мкОм*м.
История
Никель был официально открыт в 1751 году химиком Акселем Кронстедтом, который нашел его в кобальтовой земле. Однако еще раньше его раскапывали в горах Саксонии. Горняки использовали руду, содержащую никель, для изготовления стекла. По внешним признакам саксонцы сначала принимали эту руду за серебряную и пытались переплавить ее в драгоценный металл, но этого не получалось. Кроме того, при плавлении из руды выделялся ядовитый газ, который наносил вред горнякам. Неудачу потерпели и попытки добыть из этой руды медь.
В итоге в конце XVII в. саксонцы назвали руду «купферникель», что в переводе означает «медный дьявол». Это связано с тем, что горняки считали выделение ядовитого газа происками злых духов, обитавших в горах. Именно купферникель исследовал Аксель Кронстедт в 1751 году. Он получил из него окисел зеленого цвета и восстановил его до металла, который до этого не был известен науке. Химик назвал этот металл никелем.
В 1775 году Торберн Улаф Бергман получил никель в более чистом виде и подробнее описал его свойства. Он выяснил, что по своему составу этот металл больше похож на железо, чем на медь. В конце XVIII – начале XIX вв. многие химики, начиная с Жозефа Луи Пруста, детально изучали никель. В 1804 году немецкий химик Иеремия Вениамин Рихтер получил наконец чистый металл, и никель окончательно утвердился как химический элемент.
Биологическая роль
Никель — микроэлемент, который необходим всем живым организмам. Его среднее содержание в растениях — 0,00005 %, в наземных животных — 0,000001 %, в морских — 0,00016 % массы тела.
Роль никеля в организме изучена не до конца. Известно, что он участвует в ферментативных реакциях и влияет на окислительные процессы. Он содержится в легких, печени, мышцах, поджелудочной и щитовидной железах, некоторых отделах головного мозга. Микроэлемент также накапливается в ороговевших тканях человека, животных и птиц, в том числе в волосах и перьях.
Избыточное содержание никеля в растениях приводит к уродливым формам, в организме животных — к различным глазным заболеваниям (кератоконъюнктивитам, кератитам).
Пары и пыль никеля токсичны и могут вызывать поражения кожи, легких и носоглотки, а частое вдыхание паров металла опасно появлением злокачественных новообразований.
Нахождение в природе и производство
Больше всего никеля содержится в глубоких слоях. В земной коре — его 0,0058%, в ультраосновных породах — 0,2 %. Если верить гипотезе, что земное ядро состоит из никелистого железа, общее содержание никеля в земле составляет примерно 3%. Никель также обнаружен в некоторых метеоритах.
В земной коре этот металл соседствует с железом и магнием, с которыми он имеет сходную валентность. В минералах магния и железа никель содержится в виде изоморфной примеси. Также существует 53 известных науке минерала никеля. Большая часть из них была образована под воздействием давления и высоких температур, например, при застывании магмы. Сульфидные руды, содержащие данный металл, имеют в своем составе медь. Некоторые руды никеля включают железо, серу, мышьяк, кобальт, магний.
Больше всего этого металла добывается на территории России. Крупные никелевые рудники также находятся в Канаде, Австралии, Новой Каледонии, Индонезии и на Кубе.
Больше всего никеля (около 80%) получают из сульфидных медно-никелевых руд, значительно меньше — из силикатных (окисленных) руд.
Химические свойства
Никель химически малоактивен. Он образует поверхностную оксидную пленку, из-за чего устойчив в атмосфере, щелочи, многих кислотах и воде. Металл не подвергается коррозии. Образует два оксида (NiO и Ni2O3) и два гидроксида (Ni(OH)2 и Ni(OH)3).
Хлорид, нитрат, сульфат и нитрат никеля — четыре растворимые соли. Они имеют желтый или желто-коричневый оттенок и окрашивают растворы в зеленый цвет. Фосфат, оксалат и сульфиды никеля (черный, зеленый и бронзовый) — нерастворимые соли.
Металл поглощает газы (углерод, водород и многие другие), которые ухудшают его механические свойства. С кислородом взаимодействует при температуре выше 500 ⁰С.
В мелкодисперсном состоянии никель самовоспламеняется на воздухе. При нагревании соединяется с галогенами. Образует сульфид при горении в сере, а при нагревании оксида NiO с серой получается моносульфид. Металл также вступает в реакцию с азотной кислотой: образуются нитрат никеля и оксид азота.
По химическим свойствам больше всего похож на железо и кобальт, в меньшей степени — на благородные металлы и медь. Он горит только в виде порошка, проявляет переменную валентность в соединениях (чаще всего двухвалентен). Образует комплексные и координационные соединения.
Применение
Наиболее широкая область применения никеля — изготовление сплавов различных металлов. Его сплавляют:
- Со сталью. Это повышает химическую стойкость сплава: все нержавеющие стали содержат в своем составе никель.
- С железом. Этот сплав имеет низкий коэффициент термического расширения, благодаря чему он успешно используется для изготовления различных деталей для электроприборов.
- С кобальтом и магнием. Образуется жаростойкий сплав, который выдерживает высокие температуры до 500 ⁰С и отличается устойчивостью к коррозии.
- С золотом и серебром. Это так называемое «белое золото» — прочный ювелирный сплав.
- С хромом. В результате образуется нихром — жаропрочный, крипоустойчивый, пластичный сплав, который хорошо держит форму.
- С железом, медью и хромом. Этот сплав характеризуется высокой магнитной восприимчивостью.
Сплавы никеля отличаются высокой степенью вязкости, благодаря чему находят применение при изготовлении брони. Многие сплавы используются в газотурбинных установках, конструкциях атомных реакторов. Из них также делают нагревательные элементы и монеты. Сплавы получили широкое применение в производстве аккумуляторов.
Никель используется и в чистом виде: из него изготавливают трубы, листы и др., а в химических лабораториях он служит катализатором многих реакций. Из металла также производят специализированную химическую аппаратуру. Оксид никеля применяется в производстве стекла, керамики и глазурей. Для многих металлов используется никелирование — создание никелевого покрытия с целью защитить от коррозии.
Из никеля делают спирали электронных сигарет, им обматывают струны музыкальных инструментов. В медицине этот элемент используется для протезирования и изготовления брекет-систем.
Никель. Описание, свойства, происхождение и применение металла
 Никель — простое вещество, пластичный, ковкий, переходный металл серебристо-белого цвета, при обычных температурах на воздухе покрывается тонкой плёнкой оксида. Химически малоактивен. Относится к тяжелым цветным металлам, в чистом виде на земле не встречается — обычно входит в состав различных руд, высокой твердостью, хорошо полируется, является ферромагнетиком — притягивается магнитом, в периодической системе Менделеева обозначается символом Ni и имеет 28 порядковый номер.
Никель — простое вещество, пластичный, ковкий, переходный металл серебристо-белого цвета, при обычных температурах на воздухе покрывается тонкой плёнкой оксида. Химически малоактивен. Относится к тяжелым цветным металлам, в чистом виде на земле не встречается — обычно входит в состав различных руд, высокой твердостью, хорошо полируется, является ферромагнетиком — притягивается магнитом, в периодической системе Менделеева обозначается символом Ni и имеет 28 порядковый номер.
СТРУКТУРА
 Имеет гранецентрированную кубическую решетку с периодом a = 0,35238 å нм, пространственная группа Fm3m. Эта кристаллическая структура устойчива к давлению, по меньшей мере 70 ГПа. При обычных условиях никель существует в виде b-модификации, имеющей гранецентрированную кубическую решётку ( a = 3,5236 å). Но никель, подвергнутый катодному распылению в атмосфере h 2 , образует a-модификацию, имеющую гексагональную решётку плотнейшей упаковки ( а = 2,65 å, с = 4,32 å), которая при нагревании выше 200 °С переходит в кубическую. Компактный кубический никель имеет плотность 8,9 г/см
Имеет гранецентрированную кубическую решетку с периодом a = 0,35238 å нм, пространственная группа Fm3m. Эта кристаллическая структура устойчива к давлению, по меньшей мере 70 ГПа. При обычных условиях никель существует в виде b-модификации, имеющей гранецентрированную кубическую решётку ( a = 3,5236 å). Но никель, подвергнутый катодному распылению в атмосфере h 2 , образует a-модификацию, имеющую гексагональную решётку плотнейшей упаковки ( а = 2,65 å, с = 4,32 å), которая при нагревании выше 200 °С переходит в кубическую. Компактный кубический никель имеет плотность 8,9 г/см
СВОЙСТВА
 Никель — ковкий и тягучий металл, из него можно изготовлять тончайшие листы и трубки. Предел прочности при растяжении 400—500 Мн/м2, предел упругости 80 Мн/м2 , предел текучести 120 Мн/м2; относительное удлинение 40%; модуль нормальной упругости 205 Гн/м2; твёрдость по Бринеллю 600—800 Мн/м2. В температурном интервале от 0 до 631К (верхняя граница соответствует Кюри точке ). Ферромагнетизм никеля обусловлен особенностями строения внешних электронных оболочек его атомов. Никель входит в состав важнейших магнитных материалов и сплавов с минимальным значением коэффициента теплового расширения (пермаллой, монель-металл, инвар и др.).
Никель — ковкий и тягучий металл, из него можно изготовлять тончайшие листы и трубки. Предел прочности при растяжении 400—500 Мн/м2, предел упругости 80 Мн/м2 , предел текучести 120 Мн/м2; относительное удлинение 40%; модуль нормальной упругости 205 Гн/м2; твёрдость по Бринеллю 600—800 Мн/м2. В температурном интервале от 0 до 631К (верхняя граница соответствует Кюри точке ). Ферромагнетизм никеля обусловлен особенностями строения внешних электронных оболочек его атомов. Никель входит в состав важнейших магнитных материалов и сплавов с минимальным значением коэффициента теплового расширения (пермаллой, монель-металл, инвар и др.).
ЗАПАСЫ И ДОБЫЧА
 Никель довольно распространён в природе — его содержание в земной коре составляет около 0,01%(масс.). В земной коре встречается только в связанном виде, в железных метеоритах содержится самородный никель (до 8%). Содержание его в ультраосновных породах примерно в 200 раз выше, чем в кислых (1,2кг/т и 8г/т). В ультраосновных породах преобладающее количество никеля связано с оливинами, содержащими 0,13 — 0,41% Ni.
Никель довольно распространён в природе — его содержание в земной коре составляет около 0,01%(масс.). В земной коре встречается только в связанном виде, в железных метеоритах содержится самородный никель (до 8%). Содержание его в ультраосновных породах примерно в 200 раз выше, чем в кислых (1,2кг/т и 8г/т). В ультраосновных породах преобладающее количество никеля связано с оливинами, содержащими 0,13 — 0,41% Ni.
В растениях в среднем 5·10−5 весовых процентов никеля, в морских животных — 1,6·10−4, в наземных — 1·10−6, в человеческом организме — 1…2·10−6.
Основную массу никеля получают из гарниерита и магнитного колчедана.
Силикатную руду восстанавливают угольной пылью во вращающихся трубчатых печах до железо-никелевых окатышей (5—8% Ni), которые затем очищают от серы, прокаливают и обрабатывают раствором аммиака. После подкисления раствора из него электролитически получают металл.
Алюминотермический способ восстановления никеля из оксидной руды: 3NiO + 2Al = 3Ni +Al2O3
ПРОИСХОЖДЕНИЕ
 Месторождения сульфидных медно-никелевых руд связаны с лополитоподобными или плитообразными массивами расслоенных габброидов, приуроченных к зонам глубинных разломов на древних щитах и платформах. Характерной особенностью медно-никелевых месторождений всего мира является выдержанный минеральный состав руд: пирротин, пентландит, халькопирит, магнетит; кроме них в рудах встречаются пирит, кубанит, полидимит, никелин, миллерит, виоларит, минералы группы платины, изредка хромит, арсениды никеля и кобальта, галенит, сфалерит, борнит, макинавит, валлерит, графит, самородное золото.
Месторождения сульфидных медно-никелевых руд связаны с лополитоподобными или плитообразными массивами расслоенных габброидов, приуроченных к зонам глубинных разломов на древних щитах и платформах. Характерной особенностью медно-никелевых месторождений всего мира является выдержанный минеральный состав руд: пирротин, пентландит, халькопирит, магнетит; кроме них в рудах встречаются пирит, кубанит, полидимит, никелин, миллерит, виоларит, минералы группы платины, изредка хромит, арсениды никеля и кобальта, галенит, сфалерит, борнит, макинавит, валлерит, графит, самородное золото.
Экзогенные месторождения силикатных никелевых руд повсеместно связаны с тем или иным типом коры выветривания серпентенитов. при выветривании происходит стадийное разложение минералов, а также перенос подвижных элементов, с помощью воды из верхних частей коры в нижние. Там эти элементы выпадают в осадок в виде вторичных минералов.
В месторождениях этого типа заключены запасы никеля в 3 раза превышающие его запасы в сульфидных рудах, а запасы некоторых месторождений достигают 1 млн т. и более никеля. Крупные запасы силикатных руд сосредоточены на Новой Каледонии, Филиппинах, Индонезии, Австралии и др. странах. Среднее содержание в них никеля равно 1.1-2%. Кроме того в рудах часто содержится кобальт.
ПРИМЕНЕНИЕ
Подавляющая часть никеля используется для получения сплавов с другими металлами (fe, cr, cu и др.), отличающихся высокими механическими, антикоррозионными, магнитными или электрическими и термоэлектрическими свойствами. В связи с развитием реактивной техники и созданием газотурбинных установок особенно важны жаропрочные и жаростойкие хромоникелевые сплавы. Сплавы никеля используются в конструкциях атомных реакторов.
Значительное количество никеля расходуется для производства щелочных аккумуляторов и антикоррозионных покрытий. Ковкий никель в чистом виде применяют для изготовления листов, труб и т.д. Он используется также в химической промышленности для изготовления специальной химической аппаратуры и как катализатор многих химических процессов. Никель — весьма дефицитный металл и по возможности должен заменяться другими, более дешёвыми и распространёнными материалами.
Применяется при изготовлении брекет-систем (никелид титана), протезирования. Широко применяется при производстве монет во многих странах. В США монета достоинством в 5 центов носит разговорное название «никель». Также никель используется для производства обмотки струн музыкальных инструментов.
Никель (англ. Nickel) — Ni
| Молекулярный вес | 58.69 г/моль |
| Происхождение названия | Из немецкого Nickel, означает демон, как сокращенная форма Kupfernickel, медь дьявола |
| IMA статус | утвержден |
КЛАССИФИКАЦИЯ
| Strunz (8-ое издание) | 1/A.08-10 |
| Nickel-Strunz (10-ое издание) | 1.AA.05 |
| Dana (7-ое издание) | 1.1.17.2 |
| Dana (8-ое издание) | 1.1.11.5 | Hey’s CIM Ref | 1.61 |
ФИЗИЧЕСКИЕ СВОЙСТВА
| Цвет минерала | белый, светло-серебрянный |
| Цвет черты | серо белый |
| Прозрачность | непрозрачный |
| Блеск | металлический |
| Спайность | нет |
| Твердость (шкала Мооса) | 3,5 |
| Прочность | ковкий |
| Излом | зазубренный |
| Плотность (измеренная) | 7.8 — 8.2 г/см3 |
| Радиоактивность (GRapi) | 0 |
| Магнетизм | ферромагнетик |
ОПТИЧЕСКИЕ СВОЙСТВА
| Тип | изотропный |
| Цвет в отраженном свете | белый, голубоватый |
| Плеохроизм | не плеохроирует |
| Люминесценция в ультрафиолетовом излучении | не флюоресцентный |
КРИСТАЛЛОГРАФИЧЕСКИЕ СВОЙСТВА
| Точечная группа | (4/m 3 2/m) — изометрический гексаоктаэдральный |
| Пространственная группа | Fm3m |
| Сингония | кубическая |
| Параметры ячейки | a = 3.5238Å |
| Двойникование | нет |
Интересные статьи:
mineralpro.ru 13.07.2016Никель — Википедия
Материал из Википедии — свободной энциклопедии
| Внешний вид простого вещества | |
|---|---|
| Серебристо-белый металл | |
| Свойства атома | |
| Название, символ, номер | Ни́кель / Niccolum (Ni), 28 |
| Атомная масса (молярная масса) | 58,6934(4)[1] а. е. м. (г/моль) |
| Электронная конфигурация | [Ar] 3d8 4s2 |
| Радиус атома | 124 пм |
| Химические свойства | |
| Ковалентный радиус | 115 пм |
| Радиус иона | (+2e) 69 пм |
| Электроотрицательность | 1,91 (шкала Полинга) |
| Электродный потенциал | -0,25 В |
| Степени окисления | 3, 2, 0 |
| Энергия ионизации (первый электрон) | 736,2 (7,63) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 8,902 г/см³ |
| Температура плавления | 1726 K (1453 °C, 2647 °F) |
| Температура кипения | 3005 K (2732 °C, 4949 °F) |
| Уд. теплота плавления | 17,61 кДж/моль |
| Уд. теплота испарения | 378,6 кДж/моль |
| Молярная теплоёмкость | 26,1[2] Дж/(K·моль) |
| Молярный объём | 6,6 см³/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая гранецентрированая |
| Параметры решётки | 3,524 Å |
| Температура Дебая | 375 K |
| Прочие характеристики | |
| Теплопроводность | (300 K) 90,9 Вт/(м·К) |
| Номер CAS | 7440-02-0 |
Ни́кель — элемент десятой (по устаревшей короткопериодной форме — восьмой) группы, четвёртого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 28. Обозначается символом Ni (лат. Niccolum). Простое вещество никель — это пластичный, ковкий, переходный металл серебристо-белого цвета, при обычных температурах на воздухе покрывается тонкой плёнкой оксида. Химически малоактивен.
Никель: свойства и применение
Что такое никель и никелевые сплавы
Никель – пластичный металл серебристо-белого цвета с характерным блеском. Относится к тяжелым цветным металлам. Никель ценная легирующая добавка. В природе в чистом виде никель не встречается, обычно входит в состав руд. Чистый никель (Nickel/Никель), Nickel 200 и Nickel 201, добывают путем специальных технологий.
В соединении с другими металлами никель способен образовывать твердые и прочные никелевые сплавы:
- никель-медный сплав (Monel/Монель) – сплав на медной основе с никелем в качестве легирующей добавки. В составе обычно до 67% никеля и до 38% меди. К этой группе сплавов относят: Monel 400, Monel 401, Monel 404, Monel R-405, Monel K-500 и др.
- никель-хромовый сплав (Inconel/Инконель) – аустенитный жаропрочный сплав. К этой группе относят: Inconel 600, Inconel 601, Inconel 617, Inconel 625, Inconel 690, Inconel 718, Inconel 725, Inconel X-750 и др.
- никель-железо-хромовый сплав (Inconloy/Инколой) – возможно добавление в сплав молибдена, меди, титана. К этой группе относят: Incoloy 20, Incoloy 800, Incoloy 800H, Incoloy 800HT, Incoloy 825, Incoloy 925 и др.
- никель-молибденовый сплав (Hastelloy/Хастеллой) – возможно присутствие в составе хрома, железа и углерода. К этой группе относят: Hastelloy C-4, Hastelloy C-22, Hastelloy C-276, Hastelloy B-2 и др.
Свойства никеля
Никель – ферромагнетик, точка Кюри – 358°C, температура плавления – 1455°C, температура кипения – 2730-2915°C. Плотность – 8,9 г/см3 , коэффициент теплового расширения -13,5∙10−6 K−1. На воздухе компактный никель – стабилен, а высокодисперсный – пирофорен.
Никель обладает такими свойствами, как:
- пластичность и ковкость;
- прочность при высоких температурных режимах;
- устойчивость к окислению в воде и на воздухе;
- твердость и достаточная вязкость;
- высокая коррозионная стойкость;
- ферромагнетик;
- хороший катализатор;
- хорошо полируется.
Поверхность никеля покрыта тонким слоем оксида NiO, защищающим металл от окисления.
Преимущества и недостатки
Главные плюсы никеля и сплавов — жаропрочность, жаростойкость и повышенная механическая прочность (давление до 440 МПа). К достоинствам также можно отнести эксплуатацию в раскаленных концентрированных щелочных и кислотных растворах. Помимо этого никель способен сохранять магнитные свойства при пониженных температурах.
Главным недостатком никеля является значительное снижение показателей термоЭДС при быстром охлаждении после отжига (до 600°C). Также к минусам никеля можно отнести тот факт, что в природе чистый никель не встречается. Его получают путем дорогих технологий, что сказывается на его стоимости.
Область применения
Основная сфера применения никеля – металлургия. В ней он задействован в производстве высоколегированных нержавеющих сталей. Добавляя в расплав железа никель, металлурги получают прочные и пластичные сплавы, которые обладают повышенной коррозионной стойкостью и устойчивостью к высоким температурам. Стоит отметить, что никелевые сплавы сохраняют свои качества при многократном длительном нагревании.
Благодаря этим свойствам нержавеющая и термостойкая никелевая сталь применяется:
- в пищевой и химической промышленности;
- в нефтехимической промышленности и строительстве;
- в медицине и фармацевтике;
- в авиа- и машиностроении;
- в изготовлении подводных кабелей;
- в изготовлении нагревательных элементов промышленного оборудования;
- в производстве постоянных магнитов;
- в производстве станков и специального оборудования;
- в изготовлении интерьерных элементов зданий;
- в мебельной промышленности;
- в изготовлении бытовых приборов и домашней утвари;
Благодаря своей пластичности и легкости в ковке из никеля получают очень тонкие изделия, например, полосы, ленты и листы из никеля. Также никель активно используют в производстве проволоки и прутков.
Никель, хим. состав и применение никелевых и медно-никелевых сплавов
Никель — высокопрочный пластичный металл серебристо-белого цвета. Был открыт в 1751 году шведским химиком Акселем Кронстедтом. В периодической системе Д. И. Менделеева имеет номер 28 и символ Ni, атомная масса равна 58,71.
Никель — твердый и вязкий металл с ферромагнитными свойствами. Он хорошо поддается сварке, ковке, штамповке и прокатке. Отличается устойчивостью в химически активных средах, в том числе в щелочах. В атмосферных условиях покрывается защитной оксидной пленкой и не окисляется даже при температуре 800 ⁰С.
Физические свойства никеля:
- Температура плавления — 1455 ⁰С.
- Скрытая теплота плавления — 73 кал/г.
- Температура кипения — 2913 ⁰С.
- Скрытая теплота испарения — 1450 кал/г.
- Плотность — 8800 кг/м3.
- Предел прочности при растяжении отожженного никеля — 4000−5000 МПа.
- Предел прочности при растяжении деформированного никеля — 7500−9000 МПа.
- Предел текучести отожженного никеля — кГ/мм2.
- Предел текучести деформированного никеля — 70 кГ/мм2.
- Теплопроводность — 90,9 Вт/(м*К).
- Удельное электросопротивление — 0,0684 мкОм*м.
- Модуль упругости — 196−210 ГПа.
- Модуль нормальной упругости — 20000 кГ/мм2.
- Модуль сдвига — 7300 кГ/мм2.
- Твердость литого никеля — 60−70 кГ/мм2.
- Твердость отожженного никеля 70−90 кГ/мм2.
- Твердость деформированного никеля — 200 кГ/мм2.
Благодаря своим свойствам никель в чистом виде и особенно в сплавах широко применяется в различных областях промышленности. Металл образует твердые растворы со многими элементами.
Марки и химический состав никеля
Согласно ГОСТ 849-2008, выпускается 7 марок никеля — Н0, Н1Ау, Н1у, Н1, Н2, Н3 и Н4. В их составе содержится от 97,6 до 99,99 % никеля в сумме с небольшим процентом кобальта (Co) — от 0,005 до 0,7 %. Остальную массу занимают примеси:
- Углерод (C) — есть во всех марках никеля.
- Магний (Mg).
- Алюминий (Al).
- Кремний (Si).
- Фосфор (P).
- Сера (S) — есть во всех марках.
- Марганец (Mn).
- Железо (Fe).
- Медь (Cu) — есть во всех марках.
- Цинк (Zn).
- Мышьяк (As)
- Кадмий Cd).
- Олово (Sn).
- Сурьма (Sb).
- Свинец (Pb).
- Висмут (Bi).
Подробный химический состав никеля разных марок представлен в таблице ниже.
| Марка | Химический состав, % | |||||||||||||||||
| Ni и co, не менее | В том числе Co, не более | Примеси, не более | ||||||||||||||||
| C | Mg | Al | Si | P | S | Mn | Fe | Cu | Zn | As | Cd | Sn | Sb | Pb | Bi | |||
| H0 | 99,99 | 0,005 | 0,005 | 0,001 | 0,001 | 0,001 | 0,001 | 0,001 | 0,001 | 0,002 | 0,001 | 0,0005 | 0,0005 | 0,0003 | 0,0003 | 0,0003 | 0,0003 | 0,0001 |
| h2Ay | 99,95 | 0,1 | 0,001 | 0,001 | — | 0,002 | 0,001 | 0,001 | — | 0,01 | 0,1 | 0,001 | 0,001 | 0,0006 | 0,0005 | 0,0005 | 0,0005 | 0,0001 |
| h2y | 99,95 | 0,1 | 0,01 | 0,001 | — | 0,002 | 0,001 | 0,001 | — | 0,01 | 0,015 | 0,001 | 0,001 | 0,0005 | 0,0005 | 0,0005 | 0,0005 | 0,0003 |
| h2 | 99,93 | 0,1 | 0,01 | 0,001 | — | 0,002 | 0,001 | 0,001 | — | 0,02 | 0,02 | 0,001 | 0,001 | 0,001 | 0,001 | 0,0001 | 0,001 | 0,0006 |
| h3 | 99,8 | 0,15 | 0,02 | — | — | 0,002 | — | 0,003 | — | 0,04 | 0,04 | 0,005 | — | — | — | 0,1 | — | |
| h4 | 98,6 | 0,7 | 0,1 | — | — | — | — | 0,03 | — | — | 0,6 | — | — | — | — | — | — | |
| h5 | 97,6 | 0,7 | 0,15 | — | — | — | — | 0,04 | — | — | 1,0 | — | — | — | — | — | — | |
Влияние примесей на свойства металла
Сера является одной из наиболее вредных примесей. Она придает никелю краcноломкость, из-за которой ухудшаются свойства металла при обработке давлением. Чтобы нейтрализовать действие серы, добавляют марганец и/или магний.
Углерод в количестве до 0,1 % никак не влияет на свойства металла, однако при большем содержании этого элемента он выпадает из твердого раствора при отжиге и снижает пластичность холодного никеля.
При содержании висмута и свинца в количестве от 0,002 % становится невозможной горячая обработка металла: так как эти элементы почти не растворяютися в твердом состоянии, из-за них разрушается слиток. Поэтому во всех марках никеля количество свинца и висмута ограничено 0,001 и 0,0006 % соответственно.
Алюминий увеличивает электросопротивление никеля. Данный элемент содержится в самой чистой марке — Н0. Кроме того, широко применяются сплавы никеля и алюминия: у них высокая жаропрочность и устойчивость к коррозии.
Железо не оказывает ощутимого влияния на свойства никеля. Кремний раскисляет основной металл, благодаря чему благоприятно влияет на его литейные свойства, химическую стойкость и прочность.
Кобальт повышает жаростойкость, жаропрочность и прочность никеля, а марганец оказывает положительные влияние на технологические и механические свойства металла, улучшает его электросопротивление.
Применение никеля в чистом виде
Для защиты металлов от коррозии
Для этого используются покрытия, которые наносятся гальванопластикой или плакированием. Первый способ применяют для алюминия, чугуна, магния и цинка, второй — для нелегированных сталей и железа.
Для производства металлических изделий, которые имеют постоянные формы и высокую коррозионную устойчивость
Никель в чистом виде стоит дороже, чем железо и сталь, поэтому используется в тех случаях, когда невозможно обойтись другим металлом с никелевым покрытием. Из никеля производят тигли и котлы, цистерны для перевозки и плавления щелочей, хранения реагентов, пищевых продуктов и др. В никелевых трубах изготавливают конденсаты. Инструменты их этого металла устойчивы при взаимодействии с агрессивными элементами, поэтому они практически незаменимы в химических лабораториях и медицинских центрах. Различные приборы из никеля применяются для телевидения, радиолокации и атомной техники.
В качестве катализаторов и фильтров в химической промышленности
Никель обладает такими же каталитическими свойствами, что и палладий, но стоит значительно меньше, поэтому широко используется в виде порошка в реакциях гидрирования спиртов, непредельных и ароматических углеводородов, циклических альдегидов.
Порошок чистого никеля также подходит для создания пористых фильтров, которые используются для фильтрования различных продуктов: топлива, газов и др.
Для механических прерывателей нейтронного пучка.
Свойства никеля позволяют получать нейтронные импульсы с большой энергией, в результате чего пластины из этого металла применяются в ядерной физике.
Также никель используют при изготовлении электродов в щелочных аккумуляторах.
Никелевые сплавы
В сплавах никель (вместе с кобальтом) соединяется с алюминием, кремнием, марганцем, железом и хромом. Согласно ГОСТ 492-73, в них допускается не более 1,4 % примесей. В составе примесей содержится незначительная доля магния, свинца, серы, углерода, висмута, мышьяка, сурьмы, кадмия, олова. Отдельной группой выступают медно-никелевые сплавы.
Все сплавы никеля разделяются на четыре большие группы:
- Конструкционные. Особенность этих сплавов — высокие механические свойства и повышенная устойчивость к коррозии. К этой группе относятся прежде всего сплавы на медно-никелевой основе, такие как мельхиор, монель, нейзильбер. Они хорошо свариваются и поддаются обработке в холодном и горячем виде.
- Жаростойкие. Основными элементами этих сплавов являются никель и железо. Они отличаются высокой жаростойкостью и жаропрочностью, применяются преимущественно для производства электронагревательных приборов. Их также используют для изготовления малогабаритных тензорезисторов и потенциометрических обмоток.
- Термоэлектродные. Это сплавы с высоким удельным сопротивлением и большой электродвижущей силой. Их используют для производства компенсационных проводов, термопар, прецизионных приборов. К данной группе относятся некоторые никелевые (хромель, алюмель) и медно-никелевые (константан, копель, манганин) сплавы.
- Сплавы с особыми свойствами. В эту группу входят сплавы, которые находят особое применение благодаря своим уникальным свойствам. Инвар — сплав никеля и железа, который отличается повышенной упругостью. Он применяется для изготовления эталонов длины, мерных геодезических проволок, несущих конструкций лазеров, деталей часовых механизмов и др. Пермаллой — также сплав никеля и железа, обладающий высокой проницаемостью в магнитных полях. Его используют для производства магнитопроводов, деталей реле, сердечников трансформаторов и др.
Сплав с кремнием
Кремнистый никель НК 0,2 содержит 99,4 % никеля (с кобальтом), 0,15 — 0,25 % кремния и до 0,45 % примесей. Из этого сплава изготавливаются ленты и полосы, которые находят применения в электротехнике: из них делают детали приборов и устройств.
Сплавы никеля и марганца
Марганцевый никель выпускается четырех марок — НМц1, НМц2, НМц2,5 и НМц5. Из сплава НМц1 производят сетки управления ртутных выпрямителей. НМц2 находит применение в электронных лампах повышенной прочности, используется для держателей сеток и др. Проволока из сплавов НМц2,5 и НМц5 используется в свечах двигателей — автомобильных, авиационных и тракторных. НМц5 также применяется для радиоламп.
Алюмель
Алюмель (НМцАК 2-2-1) — сплав никеля, алюминия, марганца и кремния. Он содержит 1,60−2,40 % алюминия, 1,80−2,70 % марганца, 0,85−1,50 кремния, до 0,7 % примесей, остальная часть — никель с кобальтом (кобальта — до 1,2 %). Алюмель применяется для изготовления термопар, которые используются для измерения температуры в различных областях промышленности, системах автоматики, а также в медицине и научных исследованиях.
Хромели
Хромель Т (НХ 9,5) — сплав никеля и 9-10 % хрома с содержанием примесей в количестве не более 1,4 %. Из этого сплава изготавливают проволоку для термопар.
Хромель К (НХ 9) содержит 8,5−10 % хрома и до 1,4 % примесей. Проволока из данного сплава используется для компенсационных проводов.
В состав хромеля ТМ (НХМ 9,5) входит 9−10 % хрома, 0,1−0,6 % кремния и до 0,15 % примесей. Сплав используется для изготовления термопар.
Хромель КМ (НХМ 9) — это сплав никеля, 8,5−10 % хрома, 0,1−0,6 % кремния с содержанием не более 0,15 % примесей. Применяется для изготовления проволоки компенсационных проводов.
Медно-никелевые сплавы
Это сплавы на медной основе, при этом никель является в них основным легирующим элементом. Смешение никеля и меди гарантирует высокую прочность, электросопротивление и устойчивость к коррозии.
В качестве элементов медно-никелевых сплавов могут также выступать алюминий, железо, марганец, цинк, титан, свинец, кремний. Согласно ГОСТ 492-73, допускается не более 2 % примесей, для некоторых сплавов — не более 0,15 %. Наиболее распространенные медно-никелевые сплавы — это копель, константан, мельхиор, нейзильбер, куниаль, манганин, монель.
Копель
Копель (МНМц43-0,5) содержит 0,1−1 % марганца, 42,5−44 % никеля, до 0,6 % примесей, остальная масса приходится на медь. Сплав имеет большую термоэлектродвижущую силу, выпускается в виде проволоки, которая применяется для компенсационных проводов, а также для изготовления термопар.
Константан
Константан (МНМц40-1,5) — термостабильный сплав с высоким удельным электросопротивлением. Он состоит из 1-2 % марганца, 39-41 % никеля, примерно 59 % меди и не более 0,9 % примесей. Константан выпускается в виде проволоки, полос и лент. Используется для изготовления приборов высокого класса точности, реостатов и электронагревательных элементов, компенсационных проводов и термопар.
Мельхиор
Мельхиор (МНЖМц30-1-1) — конструкционный медно-никелевый сплав с содержанием 18-22 % никеля, примерно 80 % меди и не боле 0,6 % примесей. Некоторые разновидности мельхиора содержат железо и марганец. Он обладает высокой пластичностью и коррозионной стойкостью. Хорошо поддается обработке давлением в холодном и горячем виде — штампуется, режется, чеканится. Его легко паять и полировать. Мельхиор имеет серебристый оттенок, выпускается в виде труб, полос и ленты. Применяется для изготовления монет, недорогих ювелирных украшений и посуды. Из него делают трубные доски кондиционеров, конденсаторные трубы. Сплав также используется в приборостроении.
Нейзильбер
Название нейзильбер (МНЦ15-20) переводится с немецкого как «новое серебро». Такое название он получил из-за того, что напоминает драгоценный металл, но при этом он стоит намного дешевле. Из него делают столовые приборы, которые серебрятся после отливки. В промышленности нейзильбер применяется для производства паровой и водяной арматуры, медицинских инструментов и деталей точных приборов. Из него производят ордены и медали, ювелирные изделия, гитарные лады. Нейзильбер также используется для изготовления финифти и филиграни. Сплав содержит 18-22 % цинка, 13,5-16,5 % никеля, около 38 % меди и не более 0,9 % примесей. Выпускается в виде ленты, труб, полос, проволоки и прутков.
Куниаль
Куниаль — дисперсионно-твердеющий сплав меди, никеля и алюминия. Куниаль А (МНА13-3) содержит 2,3-3 % алюминия, 12-15 % никеля, около 80 % меди и не более 1,9% примесей. Куниаль Б (МНА6-1,5) — 1,2-1,8 % алюминия, 5,5-6,5 % никеля, около 90 % меди и не более 1,1 % примесей.
Куниаль А выпускается в виде прутков, применяется в машиностроении для изделий повышенной прочности. Из куниаля Б изготавливают полосы, которые используются в электротехнике для пружин и других изделий.
Манганин
Манганин (МНМц3-12) — термостабильный сплав, содержащий 11,5-13,5 % марганца, 2,5-3,5 % никеля, около 85 % меди и не более 0,9 % примесей. Он выпускается в виде листов и проволоки, находит применение в измерительной технике: из манганина делают шунты, катушки, добавочные сопротивления, магазины сопротивлений и др.
Монель
Монель (НМЖМц28-2,5-1,5) — сплав на основе никеля, который содержит 2-3 % железа, 1,2-1,8 % марганца, 27-29 % меди и не более 0,6 % примесей. Выпускается в виде лент, полос, листов и проволоки. Применяется в различных сферах промышленности: медицинской, химической, нефтяной, судо- и авиастроительной. Из него делают дрели, музыкальные инструменты, оправы для очков, различные антикоррозионные детали.
Температура плавления никеля
Температура плавления никеля.
Температура плавления никеля относится к разделу о плавкости металлов, так как данный химический элемент является металлом.
Температура плавления (обычно совпадает с температурой кристаллизации) — температура, при которой твёрдое кристаллическое тело совершает переход в жидкое состояние и наоборот.
Температура — физическая величина, характеризующая термодинамическую систему и количественно выражающая интуитивное понятие о различной степени нагретости тел.
Жидкое состояние вещества является промежуточным между твердым (кристаллическим) и газообразным состоянием.
Удельная теплота плавления — количество теплоты, которое необходимо сообщить одной единице массы кристаллического вещества в равновесном изобарно-изотермическом процессе, чтобы перевести его из твёрдого (кристаллического) состояния в жидкое (то же количество теплоты выделяется при кристаллизации вещества).
Температура плавления никеля при нормальных условиях:
Температуру плавления обозначают Тпл
Температура плавления никеля (Тпл) составляет 1455 °C (1728 K).
Температура плавления никеля приведена при нормальных условиях (согласно ИЮПАК), т.е. при давлении 105 (100 000) Па.
Для сведения: 101 325 Па = 1 атм = 760 мм рт. ст.
Необходимо иметь в виду, что температура плавления металлов может изменяться в зависимости от условий окружающей среды (давления). Точное значение температуры плавления металлов в зависимости от условий окружающей среды (давления) необходимо смотреть в справочниках.
Зависимость температуры фазового перехода (в том числе и плавления, и кипения) от давления для однокомпонентной системы даётся уравнением Клапейрона-Клаузиуса.
Источник: https://ru.wikipedia.org
Примечание: © Фото https://www.pexels.com, https://pixabay.com
Никель (металлургия, свойства, применение), никелевые сплавы
- Главная
- Механизмы
- Часть 1
- Элементы механизмов
- Простейшие рычажные механизмы
- Шарнирно-рычажные механизмы
- Часть 2
- Кулисно-рычажные механизмы
- Кривошипно-ползунные механизмы
- Часть 3
- Рычажно-кулачковые механизмы
- Рычажно-зубчатые механизмы
- Рычажно-храповые механизмы
- Механизмы рычажные с гибкими звеньями
- Механизмы рычажные с упругим звеном
- Рычажно-клиновые механизмы
- Винто-рычажные механизмы
- Часть 4
- Часть 1
Температура плавления никеля — Большая химическая энциклопедия
Краски для трафаретной печати электродов содержат субмикронный металлический порошок, либо сплав Ag-Pd, либо основной металл, обычно никель (точка плавления 1455 ° C), но иногда медь (точка плавления 1084 ° C). Палладий (точка плавления 1554 ° C) и серебро (точка плавления 961 ° C) образуют твердые растворы с температурами плавления, приблизительно пропорциональными содержанию концевых элементов. [Стр.265]Хром. Хром предлагает ряд потенциальных преимуществ для высокотемпературных применений, включая стойкость к окислению, низкую плотность и температуру плавления на 400 ° C выше, чем у никеля.Тем не менее, все попытки использовать хром сдерживаются его чрезвычайной хрупкостью (58). [Стр.127]
Никель встречается в первом переходном ряду 10-й группы (VIIIB) Периодической таблицы. Некоторые физические свойства приведены в таблице 1 (14). Никель — это элемент с высокой температурой плавления, имеющий пластичную кристаллическую структуру. Его химические свойства позволяют сочетать его с другими элементами с образованием многих сплавов. [Стр.1]
Спекание — это термический процесс, посредством которого рыхлая масса частиц преобразуется в когерентное тело.Обычно это происходит при температуре, равной 2/3 температуры плавления, или около 800—1000 ° C для никеля. Структура из спеченного никеля без активного материала называется пластиной, и ее можно приготовить либо сухим, либо влажным способами (см. Металлургия, порошок). [Pg.548]
Карбиды металлов группы железа. Карбиды железа, никеля, кобальта и марганца имеют более низкие температуры плавления, более низкую твердость и другую структуру, чем твердые металлические материалы. Тем не менее, эти карбиды, особенно карбид железа и двойные карбиды с другими переходными металлами, имеют большое техническое значение в качестве упрочняющих компонентов легированных сталей и чугуна.[Pg.453]
Смазка И смазочные материалы). Оптимальные результаты достигаются при 130 ± 5 ° C и давлении 1,5… 2,0 МПа (15… 20 бар) с использованием никелевого катализатора 0,2 мас.%. Другие катализаторы и параметры обработки могут быть использованы для получения уникальных производных. Простое гидрирование по двойной связи при 140 ° C в присутствии никелевого катализатора Ренея дает глицерилтрис (12-гидроксистеарат) [139-44-6], имеющий точку плавления 86 ° C (46,47). [Стр.154]
Реакция с водородом при 220 ° C в присутствии восстановленного никелевого катализатора приводит к полному разложению до хлористого водорода и углерода.Взрывная реакция происходит с бутилутием в растворе петролейного эфира (4). Тетрахлорэтилен также вступает во взрывоопасную реакцию с металлическим калием при его температуре плавления, однако он не реагирует с натрием (5). [Стр.28]
Арчер из-за очень неудачного совпадения принял кислый тартрат калия за ацетиламиновую кислоту. Goldfarb et al. получали аутентичную 5-ацетиламино-2-тиофенкарбоновую кислоту, т.пл. 230 232 ° C (метиловый эфир, т.пл.171-171,5 ° C, этиловый эфир, т.пл. 161 ° C), путем восстановления 5-нитро-2-тиофенкарбоновой кислоты никелем Ренея в уксусный ангидрид и доказал его структуру десульфуризацией никеля Ренея до 8-аминовалериановой кислоты.Они также подтвердили, что кислота с температурой плавления 272-273 ° C (метиловый эфир, температура плавления 135-136 ° C, этиловый эфир, температура плавления 116-117 ° C) представляет собой 4-ацетиламино-2-тиофенкарбоновую кислоту, как первоначально заявили Стейнкопф и Мюллер. . Утверждение Тируфле и Чана о том, что кислота, полученная при восстановлении и ацетилировании 5-нитро-2-тиофенкарбоновой кислоты, плавится при 272 ° C, должно быть результатом некоторой ошибки, поскольку они дают правильную температуру плавления метилового эфира. [Стр.51]
Стали и аустенитные нержавеющие стали чувствительны к расплаву цинка, меди, свинца и других металлов.Расплавленная ртуть, цинк и свинец разрушают алюминиевые и медные сплавы. Ртуть, цинк, серебро и другие агрессивны к никелевым сплавам. Другие металлы с низкой температурой плавления, которые могут повредить обычные конструкционные материалы, включают олово, кадмий, литий, индий, натрий и галлий. [Стр.895]
Сульфидирование аналогично, но катастрофическое сульфидирование является обычным явлением из-за, как правило, более низких точек плавления сульфидов, чем соответствующих оксидов. Это особенно верно в случае никелевых сплавов, когда образуется эвтектика никель / сульфид никеля.[Pg.896]
Расплавленные соли способствуют быстрой коррозии многих конструкционных материалов при относительно низких температурах. Соли с низкой температурой плавления включают соли натрия из соленой атмосферы, золу у костра, силикатную изоляцию, загрязняющие вещества в сырье и т. Д. Скорость коррозии в несколько мм / год может наблюдаться при температурах всего лишь 520 ° C. Используются сплавы с высоким содержанием хрома и никеля до 50% Cr / 50% Ni. [Pg.900]
.
Нитинол (никель-титан) — свойства, применение и состав
Металлический сплав нитинола — один из наиболее полезных сплавов, используемых для различных целей. Он имеет множество важных медицинских применений.
Что такое нитинол?
Это металлический сплав никель-титан с некоторыми уникальными свойствами. Он также известен как никель-титан. Этот сплав проявляет сверхупругость или псевдоупругость и свойства памяти формы. Это означает, что этот уникальный металл может помнить свою первоначальную форму и проявлять большую эластичность при нагрузках.
Нитинол Состав
Этот металлический сплав состоит из никеля и титана. Он содержит эти два элемента примерно в равных атомных процентах. Никель — известный аллерген, который также может обладать канцерогенными свойствами. По этой причине содержание никеля в этом сплаве вызывает большие опасения по поводу его применимости в медицинской промышленности.
Производство нитинола
Для изготовления этого сплава требуется очень жесткий контроль состава. По этой причине приготовить этот сплав очень сложно.Необычайная реакционная способность титана — еще одно препятствие на пути его получения. В настоящее время для этой цели используются два основных метода плавки:
- Вакуумные дуговой переплав: В этом методе электрическая дуга заключена между охлаждаемой водой медной ударной пластиной и сырьем. Медная форма с водяным охлаждением используется для плавления компонентов в высоком вакууме, чтобы предотвратить попадание углерода.
- Вакуумная индукционная плавка: Сырье нагревается в углеродном тигле с использованием переменных магнитных полей.Это также достигается в высоком вакууме; однако в этом процессе вводится углерод.
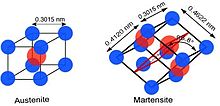
Рисунок 1 — Нитинол
Нет значительных объемов данных, показывающих, что продукт одного метода лучше другого. Оба эти метода имеют разные преимущества. Другие методы, такие как индукционная плавка черепа, плазменная дуговая плавка и электронно-лучевая плавка, также используются для этой цели в небольших масштабах. Процесс физического осаждения из паровой фазы также используется в лабораториях.
Символ нитинола
Этот металлический сплав обозначается символами составляющих его металлов. Формула этого сплава — NiTi.
История нитинола
Этот материал получил свое название от компонентов и места обнаружения. В 1962 году Уильям Дж. Бюлер и Фредерик Ван впервые обнаружили уникальные свойства этого металла в Военно-морской артиллерийской лаборатории.
Коммерциализация этого сплава была возможна только десятилетие спустя. Эта задержка в основном была вызвана сложностью плавления, механической обработки и обработки материала.
Свойства нитинола
Память формы и свойства сверхупругости — самые уникальные свойства этого сплава. Свойство памяти формы позволяет этому металлу «запоминать» свою первоначальную форму и сохранять ее при нагревании выше температуры превращения. Это происходит из-за разной кристаллической структуры никеля и титана. Этот псевдоупругий металл также демонстрирует невероятную эластичность, которая примерно в 10-30 раз больше, чем у любого обычного металла.
Вот некоторые основные физико-механические свойства этого сплава:
Физические свойства
Внешний вид: это яркий серебристый металл.
Плотность: Плотность этого сплава 6,45 г / см 3
Точка плавления: Его температура плавления составляет около 1310 ° C.
Удельное сопротивление: Он имеет удельное сопротивление 82 Ом-см при более высоких температурах и 76 Ом-см при более низких температурах.
Теплопроводность: Теплопроводность этого металла составляет 0,1 Вт / см- ° C.
Теплоемкость: Теплоемкость 0,077 кал / г · м- ° C.
Скрытая теплота: этот материал имеет скрытую теплоту 5.78 кал / г.
Магнитная восприимчивость: Его магнитная восприимчивость составляет 3,8 эмм при высоких температурах и 2,5 при низких температурах.
Механические свойства
Предел прочности на разрыв: Предел прочности на разрыв этого материала составляет от 754 до 960 МПа.
Типичное удлинение до разрушения: 15,5%
Типичный предел текучести: 560 МПа при высоких температурах; 100 МПа при низких температурах
Приблизительный модуль упругости: 75 ГПа при высоких температурах; 28 ГПа при низких температурах
Приблизительный коэффициент Пуассона: 0.3
Изготовление нитиноловых устройств
Горячая обработка этого материала относительно проще, чем холодная обработка. Чрезвычайная эластичность этого материала затрудняет холодную обработку из-за увеличения контакта валков. Это приводит к экстремальному износу инструмента и сопротивлению трению. Эти причины также чрезвычайно затрудняют обработку этого сплава. Тот факт, что этот материал имеет плохую теплопроводность, в этом не помогает. Относительно легко выполнять шлифовку, лазерную резку и электроэрозионную обработку (EDM) этого металла.
Термическая обработка этого материала очень ответственная и деликатная. Комбинация термообработки и холодной обработки важна для контроля полезных свойств этого металла.
Нитиноловая проволока
Нитинол используется для изготовления приводных проводов с памятью формы, используемых во многих промышленных целях. Эта проволока используется для изготовления проводников, стилетов и ортодонтических файлов. Этот провод идеально подходит для приложений, требующих высоких нагрузок и разгрузочных плато, а также для оправ для очков и антенн сотовых телефонов.Однако в основном эта проволока используется в стентах и корзинах для извлечения камней.
Нитинол стент
Этот сплав используется для изготовления эндоваскулярных стентов, которые очень полезны при лечении различных сердечных заболеваний. Он используется для улучшения кровотока путем введения в вену разрушенного никель-титанового стента и его нагревания. Эти стенты также используются как заменитель швов.
Корзина с нитинолом
Никель-титановые проволочные корзины хорошо подходят для многих медицинских применений, поскольку они более упругие и менее гибкие, чем многие другие металлы.Этот инструмент-корзина очень полезен для желчного пузыря.
Нитинол использует
Вот некоторые из основных применений металлического сплава нитинола:
Медицинские приложения
- Этот сплав очень полезен в стоматологии, особенно в ортодонтии для проволоки и скоб, соединяющих зубы. Sure Smile (разновидность скобок) является примером ее ортодонтического применения.
- Он также используется в эндодонтии, в основном во время обработки корневых каналов, для очистки и придания формы корневым каналам.
- В колоректальной хирургии он используется в различных устройствах для восстановления соединения кишечника после удаления патологии.
- Стенты из нитинола — еще одно важное применение этого металла в медицине.
- Его биосовместимые свойства делают его полезным в ортопедических имплантатах.
- Нитиноловая проволока может использоваться для маркировки и определения местонахождения опухолей груди.
- Использование нитиноловых трубок для различных медицинских целей становится все более популярным.
Промышленное использование
- Нитиноловая проволока используется в модельных тепловых двигателях, изготовленных в демонстрационных целях.
- Этот материал используется для контроля температуры. Его свойства изменения формы могут быть использованы для активации переменного резистора или переключателя для управления температурой.
- Этот металл часто используется в пружинах механических часов.
- Он используется в качестве микрофонной стойки или выдвижной антенны в сотовых телефонах из-за своей механической и гибкой памяти.
- Пружина из нитинола используется в различных отраслях промышленности с целью использования сверхупругих свойств этого металла.
- Листы нитинола используются для вырубки, штамповки и глубокой вытяжки.
Другое применение
- Он также используется в качестве вставки для клюшек для гольфа благодаря своей способности изменять форму.
- Это популярный выбор для изготовления чрезвычайно прочных стеклянных рам.
- Нитинол используется для изготовления самосгибающихся ложек, используемых в магических шоу.
Наличие нитинола
Никель-титан выпускается в различных формах, включая проволоку, трубки, листы и пружины.НДЦ — один из ведущих производителей и поставщиков этого металлического сплава. Однако есть много других поставщиков нитиноловой проволоки, трубок, пружин и т. Д. Различные формы этого металла также доступны в Интернете по разумным ценам.
Нитинол считается одним из наиболее полезных металлических сплавов с многочисленными промышленными и медицинскими применениями. Часто это лучший выбор для многих приложений, требующих огромного движения и гибкости. Однако этот материал показал усталостное разрушение во многих областях применения.Специалисты работают над определением пределов долговечности этого металлического сплава.
Артикул:
http://www.nitinol.com/nitinol-university/nitinol-facts/
http://www.memry.com/nitinol-iq/nitinol-fundamentals/physical-properties
http://jmmedical.com/resources/221/Nitinol-Technical-Properties.html
http://www.dynalloy.com/AboutNitinol.html
.