Титан плавления — Справочник химика 21
Титан имеет довольно высокую (1668 °С) температуру плавления и плотность 4,5 г/см . Благодаря высокой удельной прочности и превосходным противокоррозионным свойствам его широко применяют в авиационной технике. В настоящее время его используют также для изготовления оборудования химических производств. В ряду напряжений титан является активным металлом расчетный стандартный потенциал для реакции Т + + 2ё Л составляет —1,63 В . В активном состоянии он может окисляться с переходом в раствор в виде ионов Т » [1]. Металл легко пассивируется в аэрированных водных растворах, включая разбавленные кислоты и щелочи. В пассивном состоянии титан покрыт нестехиометрической оксидной пленкой усредненный состав пленки соответствует ТЮ . Полупроводниковые свойства пассивирующей пленки обусловлены в основном наличием кислородных анионных вакансий и междоузельных ионов Т , которые выполняют функцию доноров электронов и обеспечивают оксиду проводимость /г-типа. Потенциал титана в морской воде близок к потенциалу нержавеющих сталей. Фладе-потенциал имеет довольно отрицательное значение (Ер = —0,05В) [2, 3], что указывает на устойчивую пассивность металла. Нарушение пассивности происходит только под действием крепких кислот и щелочей и сопровождается значительной коррозией.Титан и его сплавы хорошо обрабатываются давлением всеми известными способами ковкой, прокаткой, штамповкой и др. Титан обладает высокой температурой плавления 1670°С, что определяет возможность разработки жаропрочных сплавов на его основе. Малый коэффициент линейного расширения обеспечивает надежность использования титана в условиях периодического изменения теплового состояния. Однако он неудовлетворительно работает при трении из-за его склонности к задиранию и заеданию. Значительного повышения износостойкости титана и его сплавов удалось достигнуть комплексным насыщением хромом и кремнием парофазным методом [11].
 При этом повысилась износостойкость титана более чем в 3—5 раза, а коэффициент трения [c.66]
При этом повысилась износостойкость титана более чем в 3—5 раза, а коэффициент трения [c.66] Простые вещества. Физические и химические свойства. В компактном состоянии все три элемента V—КЬ—Та представляют собой металлы светло-серого цвета, хорошо поддающиеся механической обработке в чистом состоянии. Все эти металлы характеризуются кристаллическими структурами с координационным числом 8 (ОЦК). Для металлов это сравнительно неплотная упаковка. В сочетании с более высокими температурами плавления элементов подгруппы ванадия по сравнению с титаном и его аналогами факт неплотной упаковки указывает иа возрастание ковалентного вклада в химическую связь. Это обусловлено увеличением числа иеспаренных электроиов на заполняющейся дефектной (п—1) -оболочке. Закономерность изменения параметров кристаллических решеток хорошо коррелирует с величинами атомных радиусов.
Химические свойства. Титан, цирконий и гафний представляют очень большой интерес в связи С тем, что их восстановительная активность весьма сильно зависит от температуры. При обычных температурах титан, цирконий и гафний имеют чрезвычайно низкую восстановительную активность и обладают высокой коррозионной устойчивостью в большинстве агрессивных сред. С повышением температуры восстановительная активность металлов растет и у титана при температуре его плавления является одной из самых высоких среди металлов. [c.79]
Как уже было указано, титан, цирконий и гафний (особенно в расплавленном виде) способны интенсивно реагировать с азотом при высоких температурах с образованием рядов твердых растворов, а также нитридов, из которых преимущественную роль играют мононитриды МеЫ. Нитриды титана, циркония и гафния — кристаллические очень твердые и тугоплавкие металлоподобные вещества. Температуры их плавления соответственно равны 2930, 2950, 3310° С. [c.85]
Из двойных металлических систем с образованием непрерывных твердых растворов рассмотрим систему титан — цирконий. -титан образует непрерывный ряд твердых растворов с р-цирконием, а а-ти-тан — непрерывный ряд твердых растворов с а-цирконием. На диаграмме состояния системы (рис. 16) нижние кривые соответствуют превращению твердых растворов Р-титана с р-цирконием в твердые растворы а-титана с а-цирконием. Кривые превращения проходят через минимум (68% циркония. 540 С). Верхние кривые соответствуют плавлению твердых растворов р-титана с р-цирконием. Кривые плавления проходят через минимум (46% циркония, 1560 С). [c.86]
-титан образует непрерывный ряд твердых растворов с р-цирконием, а а-ти-тан — непрерывный ряд твердых растворов с а-цирконием. На диаграмме состояния системы (рис. 16) нижние кривые соответствуют превращению твердых растворов Р-титана с р-цирконием в твердые растворы а-титана с а-цирконием. Кривые превращения проходят через минимум (68% циркония. 540 С). Верхние кривые соответствуют плавлению твердых растворов р-титана с р-цирконием. Кривые плавления проходят через минимум (46% циркония, 1560 С). [c.86]
Во многих случаях в системах, образованных титаном, цирконием или гафнием с другими металлами, возникают интерметаллические соединения. Как правило, они сравнительно непрочны. С некоторыми металлами только а-видоизменения образуют интерметаллиды, а р-видоизменения образуют с этими металлами только твердые растворы. Интерметаллические соединения титана, циркония и гафния с этими металлами существуют только при сравнительно низких температурах и разлагаются при температурах полиморфных превращений а р. Большинство интерметаллических соединений титана, циркония и гафния нацело разлагаются при плавлении, и только некоторые из них остаются частично неразложенными. С титаном, цирконием и гафнием образуют соединения металлы, расположенные в периодической системе правее У1В-группы, т. е. сравнительно мало активные.
Фазы внедрения образуются и при взаимодействии титана, циркония и гафния с углеродом и азотом. Растворимость этих элементов в титане и его аналогах значительно меньше, чем водорода, хотя они также образуют твердые растворы внедрения. Поскольку атомные радиусы углерода и азота больше, чем водорода, предельный состав фаз внедрения в этом случае отвечает формуле ЭС и ЭЫ, т. е. заполняются только октаэдрические пустоты в ГЦК решетке. Эти фазы относятся к наиболее тугоплавким. Ниже приводим температуры плавления карбидов и нитридов в сопоставлении с температурами плавления металлов [c.243]
Плотность титана 4,54 г/сж , температура плавления 1668° С, температура кипения около 3260° С. По внешнему виду титан похож на сталь. Титан имеет переменную валентность, но основная валентность его равна 4. На воздухе при нормальной температуре компактный титан устойчив. При нагревании выше 400° С он окисляется и растворяет азот и водород, отчего становится хрупким. Хрупкость металлу придают также примеси. [c.326]
По внешнему виду титан похож на сталь. Титан имеет переменную валентность, но основная валентность его равна 4. На воздухе при нормальной температуре компактный титан устойчив. При нагревании выше 400° С он окисляется и растворяет азот и водород, отчего становится хрупким. Хрупкость металлу придают также примеси. [c.326]
Таким образом, механизм дуги можно представить себе следующим. Из катода в результате высокой степени его разогрева (термоэлектронная эмиссия) или наличия около его поверхности больших напряженностей электрического поля (10 —10 в см — автоэлектронная эмиссия) вырывается поток электронов. Первый случай имеет место для материалов катода с высокой температурой плавления и испарения металла (уголь, графит, вольфрам, молибден), благодаря чему температура на их поверхности может достигать в катодных пятнах значений 2 500—3 000° С и выше, когда начинается заметная термоэлектронная эмиссия. Второй случай соответствует материалам с низкой температурой кипения и испарения (ртуть, титан, медь). В области катодного падения поток электронов разгоняется настолько, что за ее пределами происходит интенсивная ионизация частиц газа в дуговом промежутке, причем здесь, по-видимому, весьма существенна роль ступенчатой ионизации. Образовавшиеся положительные ионы под действием поля направляются к катоду и разогревают его вторичные и первичные электроны направляются через столб дуги в направлении анода. На их пути происходят новые соударения (главным образом термическая ионизация) и образование новых заряженных частиц, что компенсирует их исчезновение в более холодных частях столба путем рекомбинации и диффузии. При попадании на анод отрицательные частицы нейтрализуются, выбивая из него некоторое количество положительных ионов, устремляющихся через столб дуги к катоду. Плазма столба в целом нейтральна, т. е. концентрация положительных и отрицательных частиц одинакова, но из-за того, что подвижность электронов по
Прочность металлической связи возрастает с ростом числа валентных электронов, участвующих в ее образовании, о чем можно судить по температурам плавления.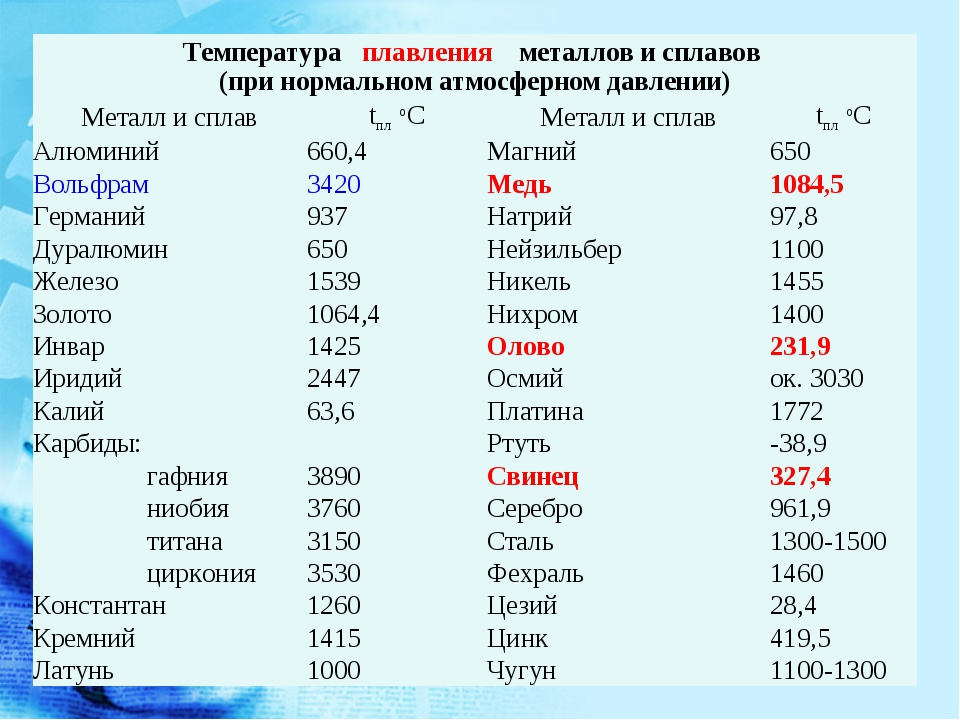 Титан, цирконий и гафний имеют по 4 валентных электрона (хотя точно не известно, сколько электронов они отдают на образование металлической связи), их температуры плавления выше температур плавления, например, металлов третьей группы, но ниже температур плавления металлов V и VI групп, имеющих большее число валентных электронов.
Титан, цирконий и гафний имеют по 4 валентных электрона (хотя точно не известно, сколько электронов они отдают на образование металлической связи), их температуры плавления выше температур плавления, например, металлов третьей группы, но ниже температур плавления металлов V и VI групп, имеющих большее число валентных электронов.
Титан, цирконий и гафний наиболее заметно различаются по плотности, температуре плавления и температуре кипения. Кроме того, у гафния высокое эффективное поперечное сечение поглощения тепловых нейтронов, равное 105 барн у циркония оно 0,18 0,02 барн. [c.212]
Химическая активность компактных Ti, Zr, Hf зависит от чистоты металла и температуры. При обычной температуре они исключительно инертны по отношению к атмосферным газам их поверхность неограниченное время остается блестящей. Высокая стойкость к окислению обусловлена рядом факторов высокими температурами плавления самих металлов и их двуокисей, обладающих малой летучестью, образованием окисных или окисно-нитридных пленок, защищающих поверхность металла. Взаимодействие компактных металлов с кислородом начинается при 200—250°, однако скорость окисления ничтожна, более того, со временем она уменьшается, так как образующаяся тонкая и плотная окисная пленка, обладающая высокой адгезией к металлам, защищает их от дальнейшего окисления. Защитные свойства пленки сохраняются до 500—600°. При более высокой температуре скорость окисления увеличивается из-за того, что окисная пленка теряет защитные свойства. С ростом ее толщины уменьшается адгезия к металлу, в ней развиваются трещины, она частично осыпается. Тем не менее титан в интервале 600—1200° более стоек к окислению, чем нержавею-ш,ая сталь. [c.212]
Титан можно вводить в электролит в виде различных соединений. Электролиз ведут ниже температуры плавления титана, поэтому он получается в виде небольших кристаллов. Процесс сопровождается образованием на катоде продуктов неполного восстановления, которые могут перемещаться к аноду и окисляться на нем, что снижает выход по току. Уменьшить образование соединений низших степеней окисления можно подбором режима электролиза, состава электролита и отделением анодного пространства пористой диафрагмой [45, 57, 58].
Уменьшить образование соединений низших степеней окисления можно подбором режима электролиза, состава электролита и отделением анодного пространства пористой диафрагмой [45, 57, 58].
Другой причиной, препятствующей определению р и а двойных сплавов на основе железа, является высокая химическая активность ряда элементов. Нет пока материалов, которые могли бы контактировать, не взаимодействуя, с жидким титаном, цирконием, ванадием и рядом лантанидов. Изучение р и сг двойных систем на основе железа во всем концентрационном интервале также ограничено высокой температурой плавления одного из компонентов (бор, гафний, ниобий, тантал, молибден, вольфрам, рений, рутений, родий, осмий, иридий). [c.39]
Г фиий, а также искусственно полученный элемент курчатовин (№ 104). Конфигурация электронной оболочки атомов этих элементов такая же, как у титана, — d s . Аналоги титана цирконий и гафний являются тяжелыми металлами — их плотности соответственно 6,45 и 13,31 г/см температуры их плавления также выше, чем у титана 1852 и 2225°С. Цирконий и гафний образуют разнообразные соединения, в устойчивых и наиболее характерных из которых цирконий и гафний четырехвалентны. Устойчивость соединений, в которых эти элементы трех- и двухвалентны, невелика п убывает в направлении Ti—Zr — Hf. В этом же направлении возрастает металлическая активность этих элементов. Цирконий и гафний, подобно титану, существуют в двух полиморфных видо-измеР ениях — а и р. Также подобно титану цирконий и гафпин при обычных температурах химически неактивны и коррозионноустойчивы, а при высокой температуре реагируют с кислородом, азотом н другими элементарными окислителями. [c.275]
Металлический титан обладает очень высокой прочностью он легок (плотность 4,44 г-см» ), огнеупорен (т. пл. 1800°С) и коррозионноустойчив. С 1950 г. начат промышленный выпуск металлического титана, который применяют всюду, где необходим легкий и прочный металл с высокой температурой плавления так, он служит конструкционным материалом для обшивки тех участков крыла самолета, на которые попадают выбрасываемые мотором раскаленные газы. [c.574]
[c.574]
Магиий медлеппо реагирует с сухим хлором вплоть до температуры плавления металла. Серебро в хлоре и хлористом водороде не разрушается при температурах до 425° С. Титан, обладая прекрасной стойкостью во влажном газообразном хлоре, подвергается сильному разрушению в сухом хлоре, что приводит да> [c.157]
Как указано выше, титан способен интенсивно реагировать с азотом при высоких температурах с образованием ряда тверлых растворов, а также нитридов, из которых преимущественную роль играет нитрид T N. Нитрид титана — кристаллическое, очень твердое (по твердости приближается к алмазу) металлоподобное вещество с температурой плавления 2930°С. Этот нитрид проводит электрический ток, причем электрическая проводимость его уменьшается с повышением температуры, что указывает па его металлический характер. Химически нитрид титана д0В0Л1зН0 инертен. С элементарным титаном образует фазы переменного состава, в основном состоящие из TiзN (субнитрид) и ограниченных твердых растворов. [c.270]
Как уже указывалось, титан способен взаимодействовать с углеродом лишь при высоких температурах. В системе титан — углерод при этих условиях образуются очень твердые сплавы, содержащие карбид титана Т1С — кристаллическое металлоподобное вещество с температурой плавления 3140°С, и ряд твердых растворов. Карбид титана проводит электрический ток, легко сплавляется с металлами и другими карбидами, образуя при этом иногда чрезвычайно твердые тугоплавкие сплавы. При обычной температуре карбид титана довольно инертен, при высоких же температурах ведет себя подобно элементарному титану — реагирует с галогенами, кислородом, серой, азотом, а таклсе с кислотами и солями — окислителями с образованием продуктов, аналогичных получающимся при действии на элементарный титан. Подобные карбиду соединения титан образует с фосфором (фосфиды), кремнием (силиды), бором (бориды). [c.270]
Диоксид титана ТЮ2 известен в виде трех модификаций рутила, анатаза и брукита.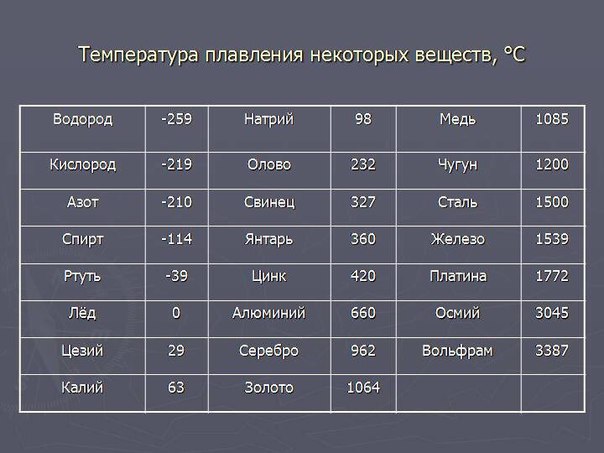 Наиболее стабильная фаза — рутил. Температура плавления его 1870°. Во всех этих формах титан находится в шестерной координации. В структуре рутила октаэдры [Т10б] соединяются между собой вершинами и двумя ребрами, в бруките — [c.118]
Наиболее стабильная фаза — рутил. Температура плавления его 1870°. Во всех этих формах титан находится в шестерной координации. В структуре рутила октаэдры [Т10б] соединяются между собой вершинами и двумя ребрами, в бруките — [c.118]
Резкий скачок в промышленном производстве А1 произошел в 80-х годах прошлого столетия, когда было технически освоено получение алюминия электролизом расплавленного раствора глинозема в криолите. Теория электрометаллургии была создана П. П. Фе-дотьевым. Отечественные ученые разработали метод получения глинозема нз нефелина. Глинозем — тугоплавкий материал, температура плавления чистого А1 0з 2072 °С, и для ее понижения добавляют преимущественно криолит Мал[А1Рг,1. При этом температура плавления понижается до 960 °С. Получение А ведут в специальных электрических печах. Продажный металл содержит примерно 99% А1. Главными примесями являются железо, кремний, титан, натрий, углерод, фториды и др. Для получения алюминия высокой степени чистоты его подвергают электролитическому рафинированию. Используют также процесс нагревания А1 в парах А1Рз (транспортную реакцию) [c.271]
Скандий широкого применения в технике пока не находит, но является перспективным. Скандий при почти равной плотности с алюминием имеет температуру плавления примерно на 750 выше. В связи с этим он мог бы представить интерес как конструкционный материал в авиа- и ракетостроении (для ядерного авиационного двигателя), представляют интерес и сплавы скандия с титаном, обладающие высокой прочностью. Сплавы скандия с висмутом или сурьмой являются сверхпроводящими материалами. Светотехника располагает возможностью резко повысить чувствительность к инфракрасным лучам цинкосульфидных фосфоров добавлением скандия. [c.70]
Титан входит в состав многих сплавов. Добавляемый к рас плавленной стали (получение ферротитана), он соединяется с со держаш,пмнся в ней кислородом и азотом и предотвраш,ает образе вание пустот, литье получается однородным (тнтан как дегазант) [c.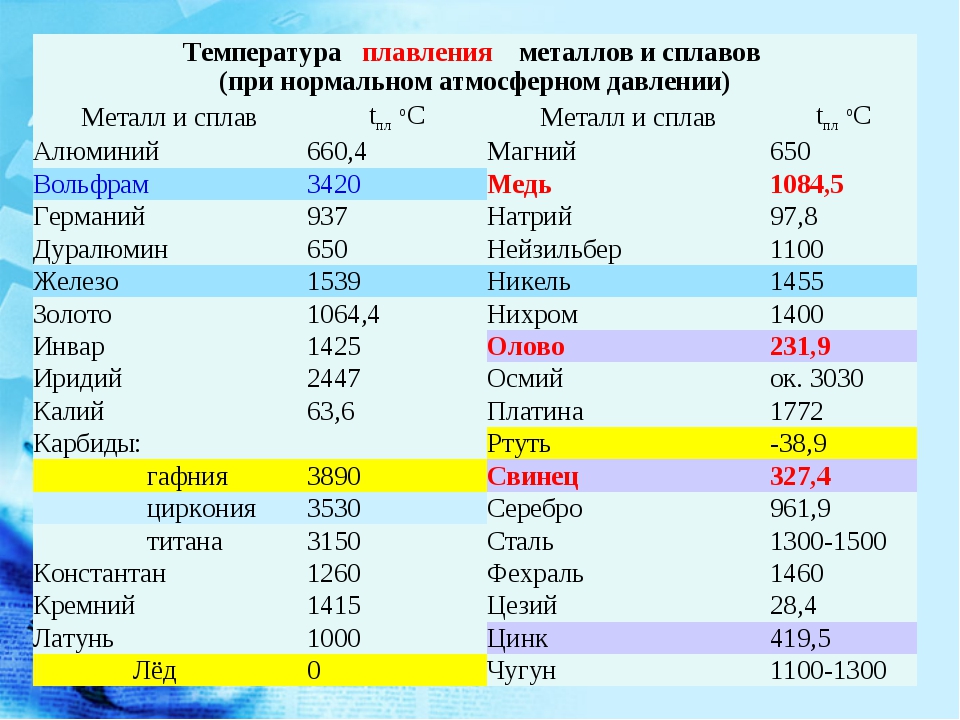 193]
193]
Металлохимия элементов подгруппы титана. Физико-химические характеристики титана и его аналогов дефектность -электронной оболочки, средние по величине значения потенциалов ионизации и атомных радиусов, высокие температуры плавления и типичные для металлов плотноупаковапные структуры — обусловливают многообразие металлохимических возможностей этих элементов. Титан, цирконий и гафний образуют непрерывные твердые растворы друг с другом в обеих модификациях. Тройная система Ti—Zr—Hf является единственным примером системы, в которой реализуются два вида непрерывных твердых трехкомпонентных растворов в двух модификациях (рис. 47). Со многими переходными металлами они [c.242]
С кислородом воздуха титан и цирконий энергично образуют диоксиды титан при 1200°, цирконий —при 650° С. В атмосфере азота оба горят, образуя нитриды типа 3N. Это очень твердые вещества переменного состава, с металлической проводимостью, температура плавления порядка 3000° С. Нитрид циркония — один из самых прочных в термодинамическом отношении нитридов. Состав его ZrNi изменяется от д = О до л = 0,42, энтальпия образования соответственно изменяется от —90,7 до —56,1 ккал ф.вес, а свободная энергия образования Д бивариантной системе — в зависимости от температуры и давления азота [49, стр. 251 ) [c.330]
Закись ТЮ, окись TI2O3 и промежуточные фазы можно получить, действуя на TIO2 восстановителями титаном, магнием, цинком, углеродом и водородом, Повыщение температуры способствует получению соединений с меньшим содержанием кислорода. Так, при восстановлении титаном в интервале 900—1000° образуется преимущественно TI2O3, а при 1400—1500° — ТЮ. Все окислы титана имеют высокую температуру плавления (табл. 54). Закись, окись и промежуточные фазы сравнительно устой- [c.216]
Восстанавливают Ti в герметичном стальном реакторе (реторте) в атмосфере аргона или гелия (рис. 82). В реактор заливают расплавленный магний и при 800° сверху подают жидкий Ti li.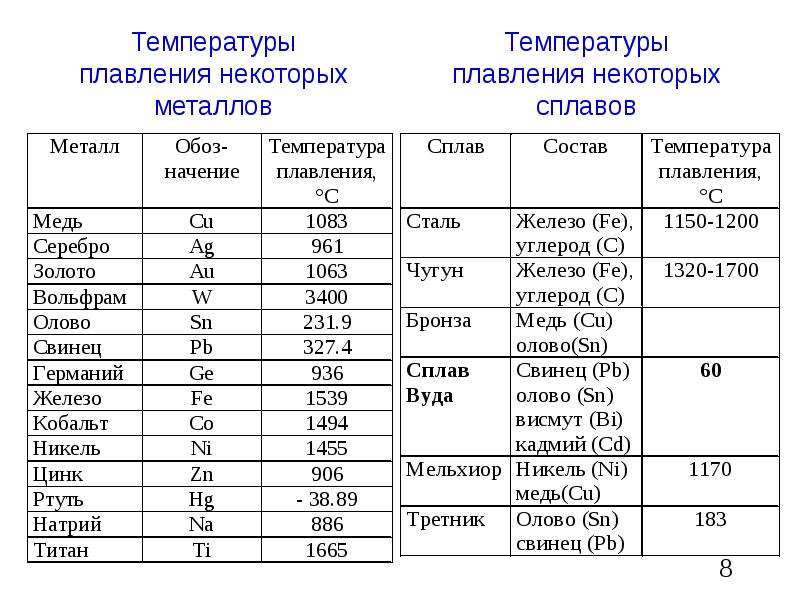 Температурный интервал, в котором проводится восстановление, невелик нижний предел— температура плавления Mg (714°), верхний предел обусловлен следующим. Титан, взаимодействуя с материалом реторты — железом, образует эвтектический сплав с т. пл. 1085°. При 1085° реактор проплавляется, выше 900° усиливается загрязнение титана железом, которое переносится через газовую фазу хлоридом железа (II), образующимся при взаимодействии Ti l со стенками реторты и расплавленным магнием, растворяющим металлическое железо. При 900° растворимость железа в магнии равна 0,17%. Вследствие экзотермич-ности реакций температура повышается до 1400°. Такая температура допустима только в центральной зоне реактора, у стенок же не должна превышать намного 900°. Поэтому реактор охлаждают воздухом. [c.270]
Температурный интервал, в котором проводится восстановление, невелик нижний предел— температура плавления Mg (714°), верхний предел обусловлен следующим. Титан, взаимодействуя с материалом реторты — железом, образует эвтектический сплав с т. пл. 1085°. При 1085° реактор проплавляется, выше 900° усиливается загрязнение титана железом, которое переносится через газовую фазу хлоридом железа (II), образующимся при взаимодействии Ti l со стенками реторты и расплавленным магнием, растворяющим металлическое железо. При 900° растворимость железа в магнии равна 0,17%. Вследствие экзотермич-ности реакций температура повышается до 1400°. Такая температура допустима только в центральной зоне реактора, у стенок же не должна превышать намного 900°. Поэтому реактор охлаждают воздухом. [c.270]
Для электролиза удобен гексафторотитанат калия K2TiFg. Его электролизом получен титан, не уступающий по качеству лучшим сортам магниетермического титана. Недостаток процесса — увеличение вязкости и температуры плавления электролита вследствие накопления в нем КЕ [34, 45, 58]. [c.277]
Свойства титана, циркония и гафиия. Титан, шрконий и гафний — сеоебристо-белые тугоплавкие металлы. Они образуют по две аллотропических модификации а-форма устойчива при комнатной температуре, а р-(зЬоржа —при высоких температурах. Плотность, теМ пературы плавления и кипения, а также электрическая проводимость возрастают от титана к гафнию, причем последняя для гафния в 3 раза выше, чем для титана. [c.460]
Характерной особенностью элементов подгруппы титана является образование твердых растворов и фаз внедрения с легкими неметаллами (Н, В, С, N1 О). Это обстоятельство накладывает заметный отпечаток на металлохимию этих элементов. Титан и его аналоги обладают способностью сильно поглощать водород. Фазам внедрения отвечают номинальные составы ЭН и ЭН2(Т1Н2, 2гН и 2гН2, НШ и НШг)- Для этих фаз характерна ГЦК-решетка. Фазы внедрения образуются и при взаимодействии титана, циркония и гафния с тлеродом и азотом. Растворимость этих элементов в титане и его аналогах значительно меньше, чем водорода, хотя они также образуют твердые растворы внедрения. Поскольку атомные радиусы углерода и азота больше, чем водорода, предельный состав фаз внедрения в этом случае отвечает формуле ЭС и ЭК, т.е. заполняются только октаэдрические пустоты в ГЦК-решетке. Эти фазы относятся к наиболее тугоплавким. Ниже приведены температуры плавления карбидов и нитридов металлов подгруппы титана [c.396]
Растворимость этих элементов в титане и его аналогах значительно меньше, чем водорода, хотя они также образуют твердые растворы внедрения. Поскольку атомные радиусы углерода и азота больше, чем водорода, предельный состав фаз внедрения в этом случае отвечает формуле ЭС и ЭК, т.е. заполняются только октаэдрические пустоты в ГЦК-решетке. Эти фазы относятся к наиболее тугоплавким. Ниже приведены температуры плавления карбидов и нитридов металлов подгруппы титана [c.396]
Титан — серебристо-белый металл. Его плотность равна 4,5 г/см а температура плавления составляет 1668 °С, Чистьп титан прочен и пластичен. [c.261]
По коррозионной стойкости Мо значительно превосходит высоконикелевые сплавы и титан. Согласно приведенным выше данным, в Н2 SO4, как и в дрзггих кислотах (НС1, h3SO4), по коррозионной стойкости молибден занимает промежуточное положение между ниобием и танталом (см. рис. 41, 42). Необходимо отметить, что ни различие в химическом составе молибденового сплава, ни технология его изготовления (вакуум-плавлен-ный, спеченный), ни структурное состояние (наклепанный, рекристаллизованный) не влияют на скорость общей коррозии, определяемую весовым методом. В связи с этим все промышленные сплавы, если их рассматривать как коррозионностойкие, можно объединить под общим названием — молибден. Несмотря на одинаковую скорость общей коррозии, [c.90]
Возможно и другое объяснение несоответствия имеющихся экспериментальных данных и ожидаемых результатов. Титан с железом образует прочный интерметаллид TiFej с температурой плавления 1530° С. Здесь вероятна такая же ситуация, как и в случае системы Fe — В. Решать этот вопрос можно только постановкой корректных экспериментов. [c.41]
ICSC 1230 — ТЕТРАХЛОРИД ТИТАНА
ICSC 1230 — ТЕТРАХЛОРИД ТИТАНА| ТЕТРАХЛОРИД ТИТАНА | ICSC: 1230 |
| Апрель 2004 |
| CAS #: 7550-45-0 | |
| UN #: 1838 | |
| EINECS #: 231-441-9 |
| ОСОБЫЕ ОПАСНОСТИ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ТУШЕНИЕ ПОЖАРА | |
|---|---|---|---|
| ПОЖАР И ВЗРЫВ | Не горючее. При пожаре выделяет раздражающие или токсичные пары (или газы). При пожаре выделяет раздражающие или токсичные пары (или газы). | В случае возникновения пожара в рабочей зоне, использовать надлежащие средства пожаротушения. В случае пожара: охлаждать бочки и т.д. распыляя воду. НЕ допускать прямого контакта с водой. |
| ИЗБЕГАТЬ ЛЮБЫХ КОНТАКТОВ! ВО ВСЕХ СЛУЧАЯХ ОБРАТИТЬСЯ К ВРАЧУ! | |||
|---|---|---|---|
| СИМПТОМЫ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ПЕРВАЯ ПОМОЩЬ | |
| Вдыхание | Боли в горле. Кашель. Ощущения жжения. Сбивчивое дыхание. Затрудненное дыхание. Симптомы могут проявляться позже. См. примечания. | Применять вентиляцию, местную вытяжку или средства защиты органов дыхания. | Свежий воздух, покой. Полусидячее положение. Может потребоваться искусственное дыхание. Обратиться за медицинской помощью. |
| Кожа | Боль. Покраснение. Серьезные ожоги кожи. | Защитные перчатки. Защитная одежда. | Снять загрязненную одежду. Промыть кожу большим количеством воды или принять душ. обратиться за медицинской помощью . |
| Глаза | Боль. Покраснение. Сильные глубокие ожоги. | Использовать маску для лица или средства защиты глаз в комбинации со средствами защиты органов дыхания.. | Прежде всего промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это возможно сделать без затруднений), затем обратится за медицинской помощью. |
| Проглатывание | Ощущение жжения. Боль в животе. Шок или сильная слабость. | Не принимать пищу, напитки и не курить во время работы. | Прополоскать рот. НЕ вызывать рвоту. Обратиться за медицинской помощью . |
| ЛИКВИДАЦИЯ УТЕЧЕК | КЛАССИФИКАЦИЯ И МАРКИРОВКА |
|---|---|
Покинуть опасную зону! Проконсультироваться со специалистом! Индивидуальная защита: полный комплект защитной одежды, включая автономный дыхательный аппарат. НЕ допускать попадания этого химического вещества в окружающую среду. Вентилировать. НЕ использовать воду. КислотостойкиеКак можно быстрее собрать пролитую жидкость в закрывающиеся емкости. Удалить оставшуюся жидкость при помощи сухого песка или инертного абсорбента. Затем хранить и утилизировать в соответствии с местными правилами. НЕ допускать попадания этого химического вещества в окружающую среду. Вентилировать. НЕ использовать воду. КислотостойкиеКак можно быстрее собрать пролитую жидкость в закрывающиеся емкости. Удалить оставшуюся жидкость при помощи сухого песка или инертного абсорбента. Затем хранить и утилизировать в соответствии с местными правилами. | Согласно критериям СГС ООН Транспортировка |
| ХРАНЕНИЕ | |
| Отдельно от пищевых продуктов и кормов. Хранить сухим. Хорошо закрывать. | |
| УПАКОВКА | |
| Не перевозить с продуктами питания и кормами для животных. |
Исходная информация на английском языке подготовлена группой международных экспертов, работающих от имени МОТ и ВОЗ при финансовой поддержке Европейского Союза. |
| ТЕТРАХЛОРИД ТИТАНА | ICSC: 1230 |
| ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА | |
|---|---|
Агрегатное Состояние; Внешний Вид Физические опасности Химические опасности | Формула: TiCl4 |
| ВОЗДЕЙСТВИЕ НА ОРГАНИЗМ И ЭФФЕКТЫ ОТ ВОЗДЕЙСТВИЯ | |
|---|---|
Пути воздействия Эффекты от кратковременного воздействия | Риск вдыхания Эффекты от длительного или повторяющегося воздействия |
| Предельно-допустимые концентрации |
|---|
| ОКРУЖАЮЩАЯ СРЕДА |
|---|
| Настоятельно рекомендуется не допускать попадания вещества в окружающую среду. |
| ПРИМЕЧАНИЯ |
|---|
Бурно реагирует с такими средствами пожаротушения, как вода. В зависимости от степени воздействия, рекомендуется периодическое медицинское обследование. Симптомы отека легких часто не проявляются, пока не пройдет несколько часов, и они усугубляются физическими усилиями. Поэтому крайне важны отдых и медицинское наблюдение. Следует рассмотреть возможность немедленного проведения соответствующей ингаляционной терапии врачом или уполномоченным на это лицом. The decomposition products of this substance may cause effects on the environment. |
| ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ |
|---|
| Классификация ЕС Символ: C; R: 14-34; S: (1/2)-7/8-26-36/37/39-45 |
| (ru) | Ни МОТ, ни ВОЗ, ни Европейский Союз не несут ответственности за качество и точность перевода или за возможное использование данной информации. © Версия на русском языке, 2018 |
Тита́н — химический элемент с атомным номером 22[4]. Принадлежит к 4-й группе периодической таблицы химических элементов (по устаревшей короткой форме периодической системы принадлежит к побочной подгруппе IV группы, или к группе IVB), находится в четвёртом периоде таблицы. Атомная масса элемента 47,867(1) а. е. м.[1]. Обозначается символом Ti. Простое вещество титан — лёгкий прочный металл серебристо-белого цвета. Обладает высокой коррозионной стойкостью. ИсторияОткрытие диоксида титана (TiO2) сделали практически одновременно и независимо друг от друга англичанин У. Грегор и немецкий химик М. Г. Клапрот. У. Грегор, исследуя состав магнитного железистого песка (Крид, Корнуолл, Англия, 1791), выделил новую «землю» (оксид) неизвестного металла, которую назвал менакеновой. В 1795 году немецкий химик Клапрот открыл в минерале рутиле новый элемент и назвал его титаном. Спустя два года Клапрот установил, что рутил и менакеновая земля — оксиды одного и того же элемента, за которым и осталось название «титан», предложенное Клапротом. Первый образец металлического титана получил в 1825 году швед Й. Я. Берцелиус. Из-за высокой химической активности титана и сложности его очистки чистый образец Ti получили голландцы А. ван Аркел и И. де Бур в 1925 году термическим разложением паров иодида титана TiI4. Титан не находил промышленного применения, пока люксембуржец Г. Кролл (англ.)русск. в 1940 году не запатентовал простой магниетермический метод восстановления металлического титана из тетрахлорида; этот метод (процесс Кролла (англ.)русск.) до настоящего времени остаётся одним из основных в промышленном получении титана. Происхождение названияМеталл получил своё название в честь титанов, персонажей древнегреческой мифологии, детей Геи. Название элементу дал Мартин Клапрот в соответствии со своими взглядами на химическую номенклатуру в противовес французской химической школе, где элемент старались называть по его химическим свойствам. Поскольку немецкий исследователь сам отметил невозможность определения свойств нового элемента только по его оксиду, он подобрал для него имя из мифологии, по аналогии с открытым им ранее ураном. Нахождение в природеТитан находится на 10-м месте по распространённости в природе. Содержание в земной коре — 0,57 % по массе, в морской воде — 0,001 мг/л[5]. В ультраосновных породах 300 г/т, в основных — 9 кг/т, в кислых 2,3 кг/т, в глинах и сланцах 4,5 кг/т. В земной коре титан почти всегда четырёхвалентен и присутствует только в кислородных соединениях. В свободном виде не встречается. Титан в условиях выветривания и осаждения имеет геохимическое сродство с Al2O3. Он концентрируется в бокситах коры выветривания и в морских глинистых осадках. Перенос титана осуществляется в виде механических обломков минералов и в виде коллоидов. МесторожденияКрупные коренные месторождения титана находятся на территории ЮАР, России, Украины, Канады, США, Китая, Норвегии, Швеции, Египта, Австралии, Индии, Южной Кореи, Казахстана; россыпные месторождения имеются в Бразилии, Индии, США, Сьерра-Леоне, Австралии[6][3]. В странах СНГ ведущее место по разведанным запасам титановых руд занимает РФ (58,5 %) и Украина (40,2 %)[7]. Крупнейшее месторождение в России — Ярегское. Запасы и добычаОсновные руды: ильменит (FeTiO3), рутил (TiO2), титанит (CaTiSiO5). По данным на 2002 год, 90 % добываемого титана использовалось на производство диоксида титана TiO2. Мировое производство диоксида титана составляло 4,5 млн т. в год. Подтверждённые запасы диоксида титана (без России) составляют около 800 млн т. На 2006 год, по оценке Геологической службы США, в пересчёте на диоксид титана и без учёта России, запасы ильменитовых руд составляют 603—673 млн т., а рутиловых — 49,7—52,7 млн т[8]. Таким образом, при нынешних темпах добычи мировых разведанных запасов титана (без учёта России) хватит более чем на 150 лет. Россия обладает вторыми в мире, после Китая, запасами титана. Минерально-сырьевую базу титана России составляют 20 месторождений (из них 11 коренных и 9 россыпных), достаточно равномерно рассредоточенных по территории страны. Самое крупное из разведанных месторождений (Ярегское) находится в 25 км от города Ухта (Республика Коми). Крупнейший в мире производитель титана — российская компания «ВСМПО-АВИСМА»[10]. ПолучениеКак правило, исходным материалом для производства титана и его соединений служит диоксид титана со сравнительно небольшим количеством примесей. В частности, это может быть рутиловый концентрат, получаемый при обогащении титановых руд. Однако запасы рутила в мире весьма ограничены, и чаще применяют так называемый синтетический рутил или титановый шлак, получаемые при переработке ильменитовых концентратов. Для получения титанового шлака ильменитовый концентрат восстанавливают в электродуговой печи, при этом железо отделяется в металлическую фазу (чугун), а невосстановленные оксиды титана и примесей образуют шлаковую фазу. Богатый шлак перерабатывают хлоридным или сернокислотным способом. Концентрат титановых руд подвергают сернокислотной или пирометаллургической переработке. Продукт сернокислотной обработки — порошок диоксида титана TiO2. Пирометаллургическим методом руду спекают с коксом и обрабатывают хлором, получая пары тетрахлорида титана TiCl4:
Образующиеся пары TiCl4 при 850 °C восстанавливают магнием:
Кроме этого, в настоящее время начинает получать популярность так называемый процесс FFC Cambridge, названный по именам его разработчиков Дерека Фрэя, Тома Фартинга и Джорджа Чена из Кембриджского университета, где он был создан. Этот электрохимический процесс позволяет осуществлять прямое непрерывное восстановление титана из оксида в расплаве смеси хлорида кальция и негашёной извести (оксида кальция). В этом процессе используется электролитическая ванна, наполненная смесью хлорида кальция и извести, с графитовым расходуемым (либо нейтральным) анодом и катодом, изготовленным из подлежащего восстановлению оксида.
Полученный кислород окисляет анод (в случае использования графита), а кальций мигрирует в расплаве к катоду, где и восстанавливает титан из его оксида:
Образующийся оксид кальция вновь диссоциирует на кислород и металлический кальций, и процесс повторяется вплоть до полного преобразования катода в титановую губку либо исчерпания оксида кальция. Хлорид кальция в данном процессе используется как электролит для придания электропроводности расплаву и подвижности активным ионам кальция и кислорода. При использовании инертного анода (например, диоксида олова), вместо углекислого газа на аноде выделяется молекулярный кислород, что меньше загрязняет окружающую среду, однако процесс в таком случае становится менее стабильным, и, кроме того, в некоторых условиях более энергетически выгодным становится разложение хлорида, а не оксида кальция, что приводит к высвобождению молекулярного хлора. Полученную титановую «губку» переплавляют и очищают. Рафинируют титан иодидным способом или электролизом, выделяя Ti из TiCl4. Для получения титановых слитков применяют дуговую, электронно-лучевую или плазменную переработку. Физические свойстваТитан — лёгкий серебристо-белый металл. При нормальном давлении существует в двух кристаллических модификациях: низкотемпературный α-Ti с гексагональной плотноупакованной решёткой (гексагональная сингония, пространственная группа C6mmc, параметры ячейки a = 0,2953 нм, c = 0,4729 нм, Z = 2) и высокотемпературный β-Ti с кубической объёмно-центрированной упаковкой (кубическая сингония, пространственная группа Im3m, параметры ячейки a = 0,3269 нм, Z = 2), температура перехода α↔β 883 °C, теплота перехода ΔH=3,8 кДж/моль[3] (87,4 кДж/кг[11]). Температура плавления титана при нормальном давлении равна 1670 ± 2 °C, или 1943 ± 2 К (принята в качестве одной из вторичных калибровочных точек температурной шкалы ITS-90 (англ.)русск.)[2]. Температура кипения 3287 °C[2]. При достаточно низкой температуре (-80°C)[2] , титан становится довольно хрупким. Молярная теплоёмкость при нормальных условиях Cp = 25,060 кДж/(моль·K), что соответствует удельной теплоёмкости 0,523 кДж/(кг·K)[2]. Теплота плавления 15 кДж/моль[11], теплота испарения 410 кДж/моль[11]. Характеристическая дебаевская температура 430 К[11]. Теплопроводность 21,9 Вт/(м·К) при 20 °C[11]. Температурный коэффициент линейного расширения 9,2·10−6 К−1 в интервале от −120 до +860 °C[11]. Молярная энтропия α-титана S0 = 30,7 кДж/(моль·К)[2]. Для титана в газовой фазе энтальпия формирования ΔH0 Удельное электрическое сопротивление при 20 °C составляет 0,58 мкОм·м[11] (по другим данным 0,42 мкОм·м[3]), при 800 °C 1,80 мкОм·м[3]. Температурный коэффициент сопротивления 0,003 К−1 в диапазоне 0…20 °C[11]. Пластичен, сваривается в инертной атмосфере. Прочностные характеристики мало зависят от температуры, однако сильно зависят от чистоты и предварительной обработки[3]. Имеет высокую вязкость, при механической обработке склонен к налипанию на режущий инструмент, и поэтому требуется нанесение специальных покрытий на инструмент, различных смазок. При обычной температуре покрывается защитной пассивирующей плёнкой оксида TiO2, благодаря этому коррозионностоек в большинстве сред (кроме щелочной). Температура перехода в сверхпроводящее состояние 0,387 К. При температурах выше 73 кельвин титан парамагнитен. Магнитная восприимчивость при 20 °C составляет 3,2·10−6[3]. Постоянная Холла α-титана равна +1,82·10−13[3]. Химические свойстваУстойчив к коррозии благодаря оксидной плёнке, но при измельчении в порошок, а также в тонкой стружке или проволоке титан пирофорен[3]. Титановая пыль имеет свойство взрываться. Температура вспышки — 400 °C. Титановая стружка пожароопасна. Титан устойчив к разбавленным растворам многих кислот и щелочей (кроме HF, H3PO4 и концентрированной H2SO4). Титан устойчив к влажному хлору и водным растворам хлора[2]. Легко реагирует даже со слабыми кислотами в присутствии комплексообразователей, например, с плавиковой кислотой HF он взаимодействует благодаря образованию комплексного аниона [TiF6]2−. Титан наиболее подвержен коррозии в органических средах, так как в присутствии воды на поверхности титанового изделия образуется плотная пассивная плёнка из оксидов и гидрида титана. Наиболее заметное повышение коррозионной стойкости титана заметно при повышении содержания воды в агрессивной среде с 0,5 до 8,0 %, что подтверждается электрохимическими исследованиями электродных потенциалов титана в растворах кислот и щелочей в смешанных водно-органических средах[14]. При нагревании на воздухе до 1200 °C Ti загорается ярким белым пламенем с образованием оксидных фаз переменного состава TiOx. Из растворов солей титана осаждается гидроксид TiO(OH)2·xH2O, осторожным прокаливанием которого получают оксид TiO2. Гидроксид TiO(OH)2·xH2O и диоксид TiO2амфотерны. TiO2 взаимодействует с серной кислотой при длительном кипячении. При сплавлении с содой Na2CO3 или поташом K2CO3 оксид TiO2 образует титанаты:
При нагревании Ti взаимодействует с галогенами (например, с хлором — при 550 °C[2]). Тетрахлорид титана TiCl4 при обычных условиях — бесцветная жидкость, сильно дымящая на воздухе, что объясняется гидролизом TiCl4, содержащимися в воздухе парами воды и образованием мельчайших капелек HCl и взвеси гидроксида титана. Восстановлением TiCl4водородом, алюминием, кремнием, другими сильными восстановителями, получен трихлорид и дихлорид титана TiCl3 и TiCl2 — твёрдые вещества, обладающие сильными восстановительными свойствами. Ti взаимодействует с Br2 и I2. С азотом N2 выше 400 °C титан образует нитрид TiNx (x = 0.58—1.00). Титан — единственный элемент, который горит в атмосфере азота[2]. При взаимодействии титана с углеродом образуется карбид титана TiCx (x = 0.49—1.00). При нагревании Ti поглощает H2 с образованием соединения переменного состава TiHx (x = 2.00—2.98). При нагревании эти гидриды разлагаются с выделением H2. Титан образует сплавы и интерметаллические соединения со многими металлами. ПрименениеВ чистом виде и в виде сплавовЧасы из титанового сплава Заготовка титанового шпангоута истребителя F-15 до и после прессования на штамповочном прессе компании Alcoa усилием 45 тыс. тонн, май 1985 тонн, май 1985Использование металлического титана во многих отраслях промышленности обусловлено тем, что его прочность примерно равна прочности стали при том, что он на 45 % легче. Титан на 60 % тяжелее алюминия, но прочнее его примерно вдвое[2].
Существует множество титановых сплавов с различными металлами. Самым распространённым титановым сплавом является сплав Ti-6Al-4V?! (в российской классификации — ВТ6), содержащий около 6% алюминия и около 4% ванадия. По соотношению кристаллических фаз он классифицируется как (α+β)-сплав. На его производство идёт до 50% добываемого титана[3]. Ферротитан (сплав титана с железом, содержащий 18—25% титана) используют в чёрной металлургии для раскисления стали и удаления растворённых в ней нежелательных примесей (сера, азот, кислород)[3]. В 1980-х годах около 60-65 % добываемого в мире титана использовалось в строительстве летательных аппаратов и ракет, 15% — в химическом машиностроении, 10% — в энергетике, 8% — в строительстве судов и для опреснителей воды[3]. В виде соединений
Анализ рынков потребленияВ 2005 компания Titanium Corporation опубликовала следующую оценку потребления титана в мире:
ЦеныЦена титана составляет $5,9-6,0 за килограмм, в зависимости от чистоты[16]. Чистота и марка чернового титана (титановой губки) обычно определяется по его твёрдости, которая зависит от содержания примесей. Физиологическое действиеТитан считается физиологически инертным, благодаря чему применяется в протезировании как металл, непосредственно контактирующий с тканями организма. Однако титановая пыль может быть канцерогенной[2]. Как было сказано выше, титан применяется также в стоматологии. Отличительная черта применения титана заключается не только в прочности, но и способности самого металла сращиваться с костью, что даёт возможность обеспечить квазимонолитность основы зуба. ИзотопыПриродный титан состоит из смеси пяти стабильных изотопов: 46Ti (7,95 %), 47Ti (7,75 %), 48Ti (73,45 %), 49Ti (5,51 %), 50Ti (5,34 %). Известны искусственные радиоактивные изотопы 45Ti (T½ = 3,09 ч), 51Ti (Т½ = 5,79 мин) и другие. Примечания
СсылкиWikiorg.ru | ||
Титан или Ti6Al4V
Материал: Ti6Al4V
Принтер: Arcam A2
Технология: Electron Beam Melting (EBM) или технология электронно-лучевой плавки
Толщина слоя: +/- 0.2 мм, +/- 0.13 мм
Размер камеры: 200 х 200 х 350 мм.
Характеристики материала для 3D-печати Ti6Al4V:
Данные снимались с использованием следующих моделей:
- Эталонная модель ARCAM размером 100 мм
- Эталонная модель ARCAM размером 10 мм
Шероховатость поверхности (по вертикали и горизонтали) Ra25/Ra35
Диаметр электронного луча (FWHM) 0.2 мм – 1.0 мм (с плавной регулировкой)
Скорость сканирования 800s м/с
Скорость построения (эталонная модель ARCAM) 55/80 см3/ч (Ti6Al4V)
Сплав Ti6Al4V — наиболее распространенный материал, применяемый в EBM-процессе, включая 3D-принтер Arcam A2, на котором мы работаем.
По составу это 6% алюминия, 4% ванадия, остальное — титан. Также могут присутствовать мелкие примеси — максимум 0.25% железа и 0.2% кислорода.
Вообще титан сам по себе — замечательный металл. Его главные достоинства — низкая плотность, переносимость высоких температур и хорошая коррозийная стойкость в любых условиях. Изначально уделом титана была аэрокосмическая отрасль, где его применяли, в первую очередь, для изготовления лопастей турбин. Сейчас потребителем титана на 70% является самолетостроение и космонавтика. Материал используется и в других областях, таких как ювелирное дело, спорт-инвентарь, здесь оценили его легкий вес и прочность. Также титан незаменим в биотехнологиях как заменитель или протез: его совместимость в живыми тканями великолепна.
Также титан незаменим в биотехнологиях как заменитель или протез: его совместимость в живыми тканями великолепна.
Ti6Al4V является самым “ходовым” сплавом титана, на его выпуск уходит от 50% до 70% процентов всего добываемого в мире титана. По химической классификации его микроструктура относится к группе α+β-сплавов. Детали имеют более высокую плотность и значительно меньшую зернистость благодаря быстрому охлаждению расплавленного материала. При 3D-печати из Ti6Al4V микроструктура материала лучше, чем литые детали из тоже сплава.
Максимальная температура применения составляет 400 ⁰С, плотность — 4420 кг/см2, модуль Юнга — 100 ГПа, предел прочности — 1000 МПа. Для сравнения, стандартная отожженная нержавеющая сталь имеет плотность 8000 кг/см2, модуль Юнга 193 ГПа, предел прочности — всего 570 МПа. Температура плавления сплава — около 1600 ⁰С.
Сферы применения материала для 3D-печати Ti6Al4V
Аэрокосмическая отрасль:
Детали газотурбинных двигателей, каркасы
Энергетика:
Лопасти паровых турбин, теплообменники
Химическая промышленность:
Емкость для хранения химикатов
Производство топлива:
Детали, стойкие к бензинам, растворителям и другим углеводородам
Медицина:
Бедренные и зубные импланты
Спорт и отдых:
Теннисные ракетки, клюшки для гольфа, ювелирные украшения
Паспорт материала титан Ti6Al4V
Сплав адаптированный для строительной индустрии, состоящий на 99.995% из чистого цинка и легирующих добавок из титана и меди. Легирующие элементы содержатся в сплаве в количестве лишь 0,06–0,20 %. Медь придает материалу необходимую пластичность, увеличивая предел прочности материала при растяжении, а титан повышает коррозионную стойкость и увеличивает сопротивление ползучести, что сочетание обоих химических элементов уменьшает коэффициент расширения. |
|
| Цинк-титан отлично поддается глубокой вытяжке и не имеет проблем в пайке. Благодаря этому сложные архитектурные элементы и оригинальные объемные конструкции часто изготавливают из цинк-титана. | |
| Антикоррозионные свойства обеспечивают срок службы цинк-титана более 100 лет. Коррозия возникает при неправильном устройстве вентиляции с обратной стороны поверхности и контакте с несовместимым материалом — медь и железо. Цинк- титан совместим с алюминием, свинцом, нержавеющей и оцинкованной сталью. | |
| Обладает свойством самовосстановления. Небольшие повреждения и царапины самостоятельно «залечиваются» самим сплавом. | |
| Цинк-титан не обладает канцерогенными свойствами и не оказывает вредных воздействий на здоровье человека. Он относится к классу негорючих строительных материалов. | |
| Свойства цинк-титана гарантируют меньшее шумовое воздействие по сравнению с другими металлами. Кровельная система с деревянной обрешеткой блокирует звук и не вызывает никаких шумовых неудобств. | |
| При воздействии атмосферных элементов на цинк-титане образуется привлекательная натуральная светло-серая патина, представляющая собой слой карбоната щелочи цинка, который защищает материал. Патина формируется при контакте цинка с кислородом и водой, в результате чего образуется слой первичного гидроксида цинка; постепенно, в процессе контакта с углекислым газом, этот слой становится слоем цинкового карбоната, называемого патиной. |
4. Титановые сплавы. Материаловедение: конспект лекций [litres]
Читайте также
Медь и сплавы
Медь и сплавы
Довольно часто домашние слесари отдают предпочтение меди (удельный вес 9,0 г/см2), поскольку ее мягкость и пластичность позволяют добиваться точности и высокого качества при изготовлении всевозможных деталей и изделий. Чистая (красная) медь – прекрасный
Чистая (красная) медь – прекрасный
ЛЕКЦИЯ № 5. Сплавы
ЛЕКЦИЯ № 5. Сплавы 1. Строение металлов Металлы и их сплавы – основной материал в машиностроении. Они обладают многими ценными свойствами, обусловленными в основном их внутренним строением. Мягкий и пластичный металл или сплав можно сделать твердым, хрупким, и наоборот.
2. Медные сплавы
2. Медные сплавы Медь относится к числу металлов, известных с глубокой древности. Раннему знакомству человека с медью способствовало то, что она встречается в природе в свободном состоянии в виде самородков, которые иногда достигают значительных размеров. В настоящее
3. Алюминиевые сплавы
3. Алюминиевые сплавы Название «алюминий» происходит от латинского слова alumen – так за 500 лет до н. э. называли алюминиевые квасцы, которые использовались для протравливания при крашении тканей и дубления кож.По распространенности в природе алюминий занимает третье
5. Цинковые сплавы
5. Цинковые сплавы Сплав цинка с медью – латунь – был известен еще древним грекам и египтянам. Но выплавка цинка в промышленных масштабах началась лишь в XVII в.Цинк – металл светло—серо—голубоватого цвета, хрупкий при комнатной температуре и при 200 °C, при нагревании до
Сплавы золота
Сплавы золота
Для изготовления ювелирных и других изделий далеко не всегда используют чистые металлы. Происходит это из-за высокой стоимости драгоценных металлов, недостаточной твердостью их и износоустойчивости, поэтому на практике чаще всего употребляют сплавы,
Происходит это из-за высокой стоимости драгоценных металлов, недостаточной твердостью их и износоустойчивости, поэтому на практике чаще всего употребляют сплавы,
7.4. Сплавы меди, имитирующие золотые и серебряные сплавы
7.4. Сплавы меди, имитирующие золотые и серебряные сплавы С целью удешевления художественных изделий при производстве недорогих украшений широко используются томпак, латунь, мельхиор, нейзильбер; при изготовлении художественных изделий – бронзы.Сплавы меди с цинком,
8. Сплавы на основе алюминия
8. Сплавы на основе алюминия Алюминиевые сплавы классифицируют по технологии изготовления (деформируемые и литейные), способности к термической обработке (упрочняемые и неупрочнямые) и свойствам (рис. 8.1). Рис. 8.1. Диаграмма состояния алюминий – легирующий элемент
10. Серебро и его сплавы
10. Серебро и его сплавы Серебро – химический элемент, металл. Атомный номер 47, атомный вес 107,8. Плотность 10,5 г/см3. Кристаллическая решетка – гранецентрированная кубическая (ГЦК). Температура плавления 963 °C, кипения 2865 °C. Твердость по Бринеллю 16,7.Серебро – металл белого
10.4. Сплавы серебра для припоев
10.4. Сплавы серебра для припоев Припой – весьма важный вспомогательный материал в ювелирном деле.Для соединения различных элементов ювелирных изделий между собой, при работе в технике скань и зернь применяют серебряные припои – сплавы на основе серебра. Основное
11.
 Золото и его сплавы
Золото и его сплавы
11. Золото и его сплавы Золото – химический элемент, металл. Атомный номер 79, атомный вес 196,97, плотность 19,32 г/см3. Кристаллическая решетка – кубическая гранецентрировапная (ГЦК). Температура плавления 1063 °C, кипения 2970 °C. Твердость по Бринеллю – 18,5.Золото – металл желтого
11.1. Двухкомпонентные сплавы золота
11.1. Двухкомпонентные сплавы золота В ювелирной промышленности иногда применяют двухкомпонентные сплавы: золото – медь и золото – серебро. Рис. 11.1. Диаграмма состояния Сu – Аu.Золото и медь обладают неограниченной растворимостью в жидком, а при высоких температурах и в
11.2. Многокомпонентные сплавы золота
11.2. Многокомпонентные сплавы золота В ювелирной промышленности для изготовления золотых изделий используют в большинстве случаев сплавы системы золото – серебро – медь, которые могут содержать добавки других металлов: никеля, палладия, цинка, платины. Химический
11.6. Золотые сплавы для припоев
11.6. Золотые сплавы для припоев При изготовлении ювелирных и художественных изделий из сплавов золота используется пайка. Состав и интервал температур плавки ювелирных припоев для пайки сплавов золота приведен в табл. 11.9. Маркировка золотых припоев осуществляется так
46. Магний и его сплавы
46. Магний и его сплавы Магний является химически активным металлом: образующаяся на воздухе оксидная пленка МдО в силу более высокой плотности, чем у самого магния, растрескивается и не имеет защитных свойств; порошок и стружка магния легко воспламеняются; горячий и
47.
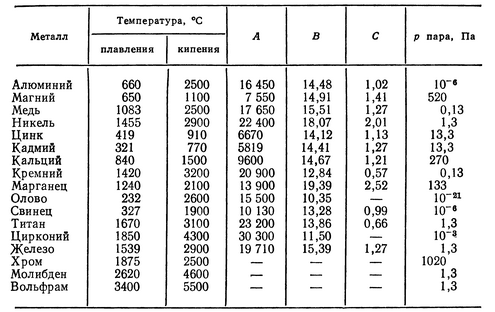 Титан и его сплавы
Титан и его сплавы
47. Титан и его сплавы Титан и сплавы на его основе обладают высокой коррозионной стойкостью и удельной прочностью. Недостатки титана: его активное взаимодействие с атмосферными газами, склонность к водородной хрупкости.Азот, углерод, кислород и водород, упрочняя титан,
Ученые увеличили прочность шва сварного соединения титана и алюминия более чем в два раза
Специалисты Института теоретической и прикладной механики им.
С. А. Христиановича (ИТПМ СО РАН) совместно с коллегами из Института
ядерной физики им. Г. И. Будкера СО РАН (ИЯФ СО РАН) и Института химии
твердого тела и механохимии СО РАН (ИХТТМ СО РАН) исследовали
особенности лазерной сварки разнородных материалов промышленных сплавов
на основе титана и алюминия.
Для ряда изделий в авиастроительной промышленности требуется
соединение титановых и алюминиевых сплавов, благодаря которому
производимые конструкции приобретают высокие прочностные характеристики и
при этом остаются легкими. Наиболее перспективным методом соединения
разнородных сплавов является лазерная сварка – она в 30 раз
производительнее традиционной автоматической клепки. Но различия в
химических и физических свойствах титана и алюминия (температура
плавления, плотность, теплопроводность) делают технологический процесс
сварки достаточно сложным.
По словам специалиста, переход к лазерной сварке взамен заклепочного соединения – ключевая задача авиастроения, а получение «сварного» самолета – голубая мечта авиастроителей. «Метод заклепочного соединения давно перестал быть технологичным. Сравните, скорость автоматической клепки около 0,2 – 0,3 метров в минуту, тогда как лазерная сварка позволяет сваривать в минуту четыре метра. Наша лаборатория имеет большой опыт работы с титановыми и алюминиевыми сплавами и давно пропагандирует внедрение лазерной сварки в авиастроение», – добавляет Александр Маликов.
Растровая электронная микроскопия и EDX анализ структуры соединения, полученного без смещения луча. Предоставлена И. Витошкиным.
Задача сварки разнородных материалов технологически достаточна сложна, в первую очередь, из-за различий в химических и физических свойствах: у свариваемых материалов отличаются температура плавления, плотность, теплопроводность. Так, разница в химическом составе может привести к появлению нежелательных соединений в ходе сварки и изменению свойств материалов в зоне шва, а различие в теплофизических свойствах приводит к неравномерному нагреву материалов, что является причиной возникновения остаточных термических напряжений. Все это ухудшает механические характеристики разнородных сварных соединений.
Комплекс
исследований, проводимых специалистами СО РАН, включал сварку листов,
применяемых в авиастроении алюминиевого и титанового сплавов,
исследование микроструктуры полученного сварного соединения, в том числе
изучение его структурно-фазового состава с применением СИ, а также
оптимизацию режимов лазерной сварки.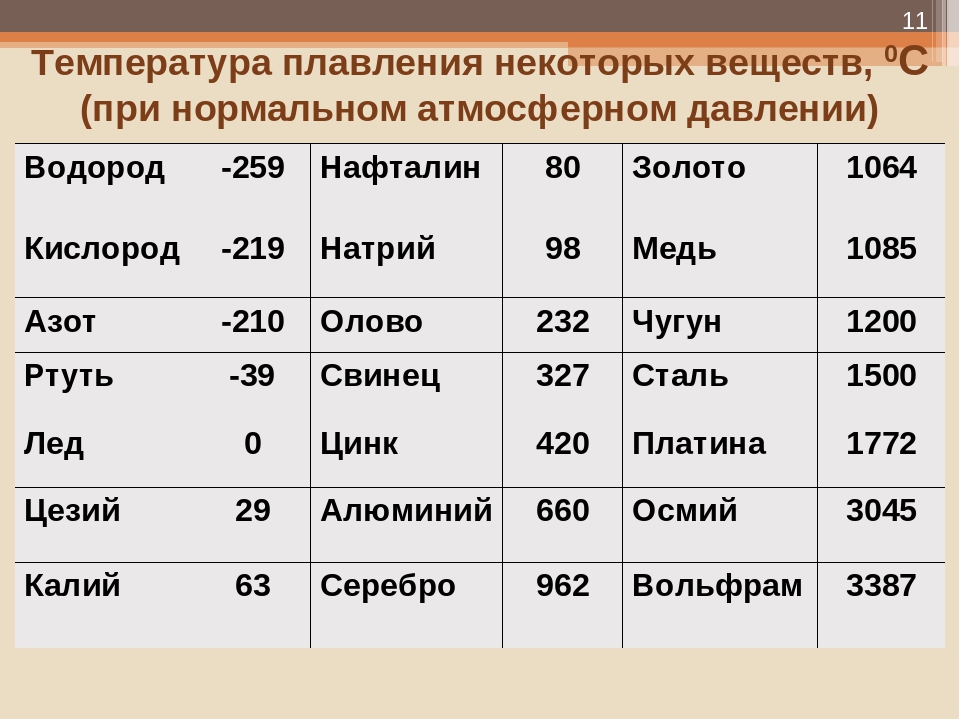
Лазерная сварка выполнялась на автоматизированном лазерном технологическом комплексе «Сибирь» ИТПМ СО РАН, дифракционные исследования проводились с использованием инфраструктуры Центра коллективного пользования «Сибирский центр синхротронного и терагерцового излучения» (ЦКП «СЦСТИ»).
«При помощи синхротронного излучения мы в деталях увидели, что происходит в шве после лазерной сварки встык, – рассказывает старший научный сотрудник ИХТТМ СО РАН, руководитель станции «Дифрактометрия в жестком рентгеновском излучении» ЦКП «СЦСТИ», кандидат химических наук Алексей Анчаров. – Высокоинтенсивным пучком с поперечным размером в сто микрон мы посмотрели семь точек в шве и получили полную дифракционную картину. Для данного сварного соединения структурно-фазовый состав, определенный с использованием СИ, был получен впервые. Мы увидели различные интерметаллидные образования (соединения двух металлов), большинство из которых оказались твердыми и хрупкими, что понизило прочность сварного шва. Следующей нашей задачей было получение однородного сплава».
Специалисты
сместили лазерное излучение в сторону титанового сплава, в результате
получив меньшее количество интерметаллидов и увеличив прочность сварного
шва в 2,25 раза.
Растровая электронная микроскопия и EDX анализ структуры соединения, полученного со смещением луча на 1 мм.
«Мы отрегулировали количество
интерметаллидов и получили хорошее прочное соединение, что и увидели
благодаря синхротронному излучению, – добавляет Александр Маликов. –
Теперь необходимо проанализировать все возможные варианты смещения
лазерного пучка – такие работы уже ведутся. Совместные исследования в
ЦКП «СЦСТИ» показали, что применение синхротронного излучения для
диагностики создаваемых материалов – это приоритет. Высокая
интенсивность и разрешающая способность источника СИ уже сейчас
позволяют нам на качественно новом уровне понимать, как взаимодействуют
сплавы. Источник СИ поколения 4+ (Центр коллективного пользования
«Сибирский кольцевой источник фотонов»), проект которого реализуется в
Новосибирске, улучшит эти возможности в разы. Наша конечная цель –
получить сварную технологию, которую можно будет внедрять в авиацию».
Источник СИ поколения 4+ (Центр коллективного пользования
«Сибирский кольцевой источник фотонов»), проект которого реализуется в
Новосибирске, улучшит эти возможности в разы. Наша конечная цель –
получить сварную технологию, которую можно будет внедрять в авиацию».
Химические и физические свойства титана
Титан — прочный металл, используемый в имплантатах человека, самолетах и многих других изделиях. Вот факты об этом полезном элементе:
Основные факты
Изотопы
Известно 26 изотопов титана от Ti-38 до Ti-63. Титан имеет пять стабильных изотопов с атомными массами 46-50. Самый распространенный изотоп — это Ti-48, составляющий 73,8% всего природного титана.
Недвижимость
Титан имеет температуру плавления 1660 +/- 10 ° C, точку кипения 3287 ° C, удельный вес 4.54, с валентностью 2, 3 или 4. Чистый титан — это блестящий белый металл с низкой плотностью, высокой прочностью и высокой коррозионной стойкостью. Он устойчив к разбавленным серной и соляной кислотам, влажному газообразному хлору, большинству органических кислот и растворам хлоридов. Титан пластичен только в том случае, если он не содержит кислорода. Титан горит на воздухе и является единственным элементом, который горит в азоте.
Титан диморфен, его гексагональная форма a медленно меняется на кубическую форму b около 880 ° C. Металл соединяется с кислородом при температуре красного каления и с хлором при 550 ° C.Титан прочен, как сталь, но на 45% легче. Металл на 60% тяжелее алюминия, но в два раза прочнее.
Металлический титан считается физиологически инертным. Чистый диоксид титана достаточно прозрачный, с чрезвычайно высоким показателем преломления и оптической дисперсией выше, чем у алмаза. Природный титан становится очень радиоактивным при бомбардировке дейтронами.
использует
Титан важен для легирования алюминия, молибдена, железа, марганца и других металлов. Титановые сплавы используются в ситуациях, когда требуется легкая прочность и способность выдерживать экстремальные температуры (например, в аэрокосмической отрасли). Титан можно использовать в опреснительных установках. Металл часто используется для деталей, которые должны подвергаться воздействию морской воды. Титановый анод, покрытый платиной, может использоваться для обеспечения катодной защиты от коррозии от морской воды.
Титановые сплавы используются в ситуациях, когда требуется легкая прочность и способность выдерживать экстремальные температуры (например, в аэрокосмической отрасли). Титан можно использовать в опреснительных установках. Металл часто используется для деталей, которые должны подвергаться воздействию морской воды. Титановый анод, покрытый платиной, может использоваться для обеспечения катодной защиты от коррозии от морской воды.
Поскольку металлический титан инертен в организме, он может применяться в хирургии. Диоксид титана используется для изготовления искусственных драгоценных камней, хотя получаемый камень относительно мягкий.Астеризм звездчатых сапфиров и рубинов является результатом присутствия TiO 2 . Диоксид титана используется в красках для дома и художников. Краска стойкая и обеспечивает хорошее покрытие. Это отличный отражатель инфракрасного излучения. Краска также используется в солнечных обсерваториях.
Пигменты оксида титана составляют наибольшее использование элемента. Оксид титана используется в некоторых косметических средствах для рассеивания света. Тетрахлорид титана используется для иридирования стекла. Поскольку соединение сильно дымится на воздухе, оно также используется для создания дымовых завес.
Источники
Титан — 9-й элемент земной коры по распространенности. Он почти всегда находится в магматических породах. Он встречается в рутиле, ильмените, сфене и многих железных рудах и титанатах. Титан содержится в угольной золе, растениях и в организме человека. Титан содержится на солнце и в метеоритах. Камни с миссии Аполлона 17 на Луну содержали до 12,1% TiO 2 . Скалы из более ранних миссий показали более низкий процент диоксида титана. Полосы оксида титана видны в спектрах звезд M-типа.В 1946 году Кролл показал, что титан можно производить в промышленных масштабах, восстанавливая тетрахлорид титана магнием.
Физические данные
Общая информация
- Титан был обнаружен в черном песке, известном как ильменит.
 Ильменит представляет собой смесь оксидов железа и оксидов титана.
Ильменит представляет собой смесь оксидов железа и оксидов титана. - Уильям Грегор был пастором прихода Маннакан, когда он обнаружил титан. Он назвал свой новый металл «манакканит».
- Немецкий химик Мартин Клапрот заново открыл новый металл Грегора и назвал его титаном в честь Титанов, греческих мифологических существ Земли.Название «титан» было предпочтительнее и в конечном итоге было принято другими химиками, но признал Грегора как первого первооткрывателя.
- Чистый металлический титан не был выделен Мэтью Хантером до 1910 года — через 119 лет после его открытия.
- Примерно 95% всего титана используется в производстве диоксида титана TiO 2 . Диоксид титана — чрезвычайно яркий белый пигмент, используемый в красках, пластмассах, зубной пасте и бумаге.
- Титан используется в медицинских процедурах, потому что он не токсичен и не реагирует на организм.
Список литературы
- Лос-Аламосская национальная лаборатория (2001)
- Crescent Chemical Company (2001)
- Справочник Ланге по химии (1952)
- Справочник CRC по химии и физике (18-е изд.)
- База данных ENSDF Международного агентства по атомной энергии (октябрь 2010 г.)
Низкоплавкие припои на основе титана — часть 1: Характеристики двух-, трех- и четырехкомпонентных присадочных металлов
Р.Ю. Ки, Л. Бернетт, С. Иноуе, Титановая структурная пайка, сварка . Res. Приложение ., Том 53 (№ 10), 1974 г., стр. 426–431
Google Scholar
H.I. МакГенри и Р. Ключ, паяные титановые отказобезопасные конструкции, сварной шов . Res. Приложение ., Том 53 (№ 10), 1974 г., стр. 432–439
Google Scholar
W.T. Kaarlela and W.S. Марголис, Разработка припоя Ag-Al-Mn для титана, сварной шов . J ., Vol. 53 (№ 10), 1974, с. 629–636
J ., Vol. 53 (№ 10), 1974, с. 629–636
КАС Google Scholar
, низкотемпературная пайка большой площади устойчивых к повреждениям титановых конструкций, сварной шов . Res. Приложение ., Том 54 (№ 10), 1975 г., стр. 348–356
Google Scholar
D.G. Хауден и Р.В. Монро, Сплавы, подходящие для пайки титановых теплообменников, Weld. J ., Том 51 (№ 1), 1972, с. 31–36
CAS Google Scholar
S.W. Lan, Ламинированные припои для титановых сборок, Weld. J ., Vol 61 (No. 10), 1982, p 23–28
CAS Google Scholar
Т. Онзава, А. Сузумура и М. В. Ко, Пайка титана с использованием присадочных металлов на основе титана с низкой температурой плавления, Weld. Res. Дополнение ., Vol. 69 (№ 12), 1990, с. 462–467
Google Scholar
J.C. Chesnutt, C.G. Родс и Дж. К. Уильямс, Взаимосвязь между механическими свойствами, микроструктурой и топографией разрушения в α + β-титановых сплавах, Титан и титановые сплавы, Справочник , MJ Donachie, Jr., Ed., Американское общество металлов, 1982, стр. –139
SD Кук, Ф. Жоржетт, Х. Скиннер, Р.Дж. Хаддэ, Усталостные свойства углерода и сплава Ti-6Al-4V с пористым покрытием, J.Биомед. Матер. Res ., Vol 18, 1984, p 497–512
CAS Статья Google Scholar
М.М. Schwartz, Пайка , ASM International, 1985
Y.C. Чен, «Исследования новых присадочных металлов Ti-Cu-Ni для пайки титановых пластин», M.S. Диссертация, Национальный университет Сунь Ятсена, Тайвань, 1990 г. (на китайском языке)
Google Scholar

Стандартная практика стандартного эталонного метода для проведения измерений потенциостатической и потенциодинамической анодной поляризации, G5-82, Ежегодный сборник стандартов ASTM , том 03.02, ASTM, 1983
G.I. Огунделе и В. Уайт, Исследования поляризации хирургических нержавеющих сталей в растворе Хэнка , STP 859, ASTM, 1985, стр. 17–135
М. Поурбэ, Атлас электрохимического равновесия в водных растворах , Pergamon Press, 1966
A.C. Fraker, A.W. Рафф, П. Сунг, А.К. Ван Орден, К.М. Speck, Подготовка поверхности и коррозионное поведение титановых сплавов для хирургических имплантатов, Титановые сплавы в хирургических имплантатах , STP 796, ASTM, 1983, стр. 206–219
Свойства титана — Kyocera SGS Europe
| Имущество | Значение |
| Атомный номер | 22 |
| Атомный вес | 47.9 |
| Атомный объем | 10,6 Вт / Г |
| Ковалентный радиус | 1,32 Å |
| Потенциал ионизации | 6,8282 В |
| Сечение поглощения тепловых нейтронов | 5,6 барн / атом |
| Кристаллическая структура | |
| Альфа (= 882,5 ° C или 1620 ° F) | Плотный шестигранник |
| Бета (= 882,5 ° C или 1620 ° F) | Телоцентрированная кубическая |
| Цвет | Темно-серый |
| Плотность | 4.51 г / см3 (0,163 фунт / дюйм3) |
| Температура плавления | 1668 ± 10 ° C (3035 ° F) |
| Солидус / ликвидус | 1725 ° С (3135 ° F) |
| Температура кипения | 3260 ° С (5900 ° F) |
| Удельная теплоемкость (при 25 ° C) | 0,5223 кДж / кг K |
| Теплопроводность | 11,4 Вт / м K |
| Теплота плавления | 440 кДж / кг (расчетная) |
| Теплота испарения | 9. 83 МДж / кг 83 МДж / кг |
| Удельный вес | 4,5 |
| Твердость | от 70 до 74 HRB |
| Прочность на разрыв | мин. 240 МПа (35 фунтов на кв. Дюйм) |
| Модуль Юнга | 120 ГПа (17 × 106 фунтов на кв. Дюйм) |
| Коэффициент Пуассона | 0,361 |
| Коэффициент трения | |
| При 40 м / мин (125 фут / мин) | 0,8 |
| При 300 м / мин (1000 фут / мин) | 0.68 |
| Коэффициент линейного теплового расширения | 8,41 мкм / м K |
| Электропроводность | 3% IACS (где медь = 100% IACS) Удельное электрическое сопротивление (при 20 ° C) |
| Электроотрицательность | 1,5 Полинга |
| Температурный коэффициент электрического сопротивления | 0,0026 / ° С |
| Магнитная восприимчивость (объемная, при комнатной температуре) | 180 (± 1.7) × 10–6 мкс |
Цвет и физические свойства
Pure Titanium — белый металлик с нежным блеском. Он расположен в четвертой группе периодической таблицы и имеет самое высокое отношение прочности к весу среди всех элементов. Его удельная прочность составляет 288 кНм / кг. Его плотность 4,5 г / см3 значительно меньше плотности стали 7,8 г / см3. Именно эти свойства объясняют, почему титан был ответственен за значительное улучшение отношения тяги к массе реактивных двигателей.
Механические свойства
Титан обладает отличной пластичностью и прочностью на разрыв. Его минимальный предел текучести составляет от 240 до 241 МПа для технически чистого сорта 1. Ti-10V-2Fe-3Al имеет самый высокий предел текучести среди всех титановых сплавов при 1260 МПа.
Технически чистый титан марки 1 имеет твердость по шкале В по Роквеллу 70–74 и вязкость разрушения 66 МПа-м½. Его модуль упругости для чистого титана составляет 120 ГПа при модуле сдвига 45 ГПа.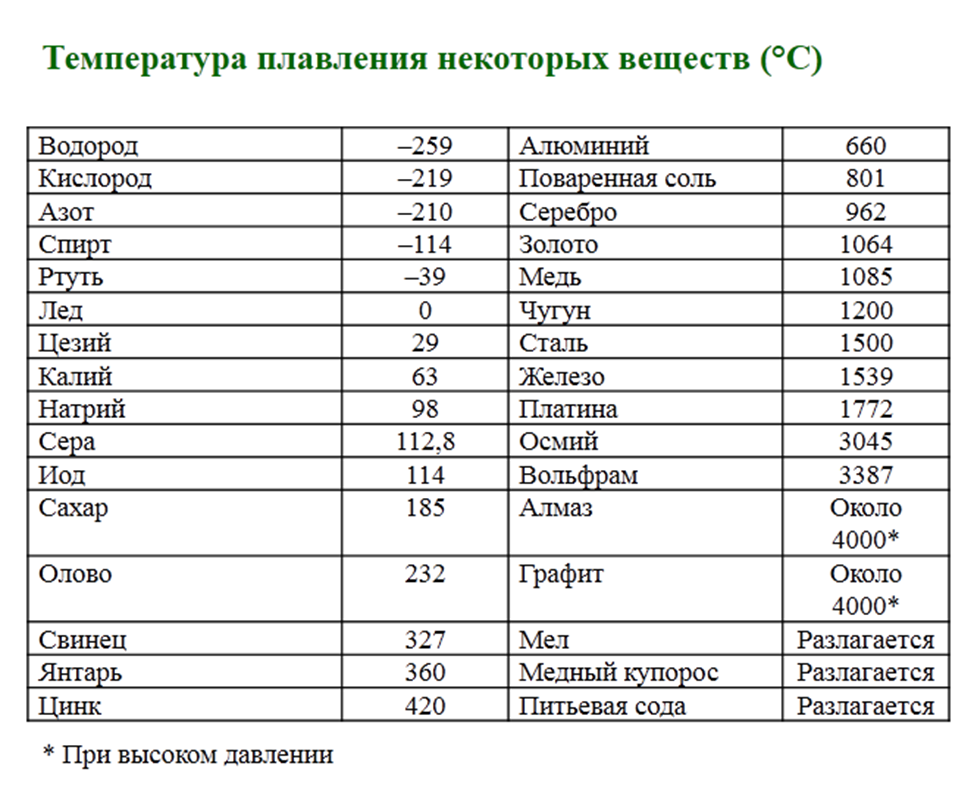
Электрические характеристики
Титан имеет низкую электропроводность 3.1% IACS (Международный стандарт отожженной меди). Это делает его неподходящим для применений, где желательна электрическая проводимость. Однако его физические и механические свойства с лихвой компенсируют это.
Тепловые свойства
Титан имеет низкую теплопроводность — 11,4 Вт / м · К, что является важным фактором во время обработки. Титан имеет тенденцию нагревать инструмент вместо того, чтобы распределять тепло по металлу, что сокращает срок службы инструмента и может привести к ухудшению характеристик металла.
- Температура плавления 1668 ± 10 ° C (3035 ° F)
- Солидус / ликвидус 1725 ° C (3135 ° F)
- Точка кипения 3260 ° C (5900 ° F)
- Удельная теплоемкость (при 25 ° C) 0,5223 кДж / кг K
- Теплопроводность 11,4 Вт / м · К
- Теплота плавления 440 кДж / кг (расчетная)
- Теплота испарения 9,83 МДж / кг
Химические свойства
Как и алюминий, чистый титан обладает высокой реакционной способностью. Атмосферная пассивация формирует оксидный слой на поверхности металла, делая его инертным.Этот процесс происходит не только в воздухе, но и под водой. Слой толщиной 1-2 нанометра образуется мгновенно и через 4 года становится более толстым до 25 нанометров.
Благодаря этому оксидному слою титан невосприимчив к воздействию соляной и серной кислоты. Дальнейшее улучшение химической стойкости связано с добавлением палладия марок 11 и 17 для применения в соленой воде и на химических предприятиях.
При температуре выше 800 градусов титан будет гореть в азоте с образованием нитрида титана.Титан без оксидного покрытия представляет высокий риск возгорания в кислороде. Чтобы узнать о свойствах наиболее часто используемого титанового сплава Ti 6Al 4V, просмотрите наш технический паспорт класса 5.
MatWeb, ваш источник информации о материалахЧто такое MatWeb? MatWeb’s база данных свойств материалов с возможностью поиска включает паспорта термопластов и термореактивных полимеров, таких как АБС, нейлон, поликарбонат, полиэстер, полиэтилен и полипропилен; металлы, такие как алюминий, кобальт, медь, свинец, магний, никель, сталь, суперсплавы, сплавы титана и цинка; керамика; плюс полупроводники, волокна и другие инженерные материалы. Преимущества регистрации в MatWeb Как найти данные о собственности в MatWebНажмите здесь, чтобы узнать, как войти материалы вашей компании в MatWeb. У нас есть более 150 000 материалы в нашей базе данных, и мы постоянно добавляем их, чтобы обеспечить Вам доступен самый полный бесплатный источник данных о собственности материалов в Интернете. Для вашего удобства в MatWeb также есть несколько конвертеров. и калькуляторы, которые делают общие инженерные задачи доступными одним щелчком мыши. кнопки. MatWeb находится в стадии разработки.Мы постоянно стремимся найти лучшее способы служить инженерному сообществу. Пожалуйста, не стесняйтесь свяжитесь с нами с любыми комментариями или предложениями. База данных MatWeb состоит в основном из предоставленных таблиц данных и спецификаций. производителями и дистрибьюторами — сообщите им, что вы видели их данные о материалах на MatWeb. |
|
Титан vs.
 Алюминий | Центр обработки титана
Алюминий | Центр обработки титанаТитан — прочный и легкий материал, который используется во многих областях. Однако из-за цены его по-прежнему часто сравнивают с алюминием, который также является очень прочным металлом, но предлагает более низкую цену. Однако существует множество факторов, которые могут повлиять на окончательный выбор приложения, и необходимо учитывать как стоимость, так и характеристики металла. Простое сравнение химических и механических свойств этих металлов покажет, чем они отличаются и что может быть лучше для данной задачи.
Титан
Титан — один из наиболее распространенных металлов, встречающихся в природе. Он легкий, прочный и устойчивый к коррозии, что делает его очень желанным материалом. К сожалению, его трудно добывать и обрабатывать, что может сделать его более дорогим, чем другие металлы. Он обладает хорошей теплопроводностью, немагнитен и нетоксичен. Помимо этого, титан также имеет следующие характеристики:
- Предел прочности при растяжении — от 3000 до 200000 фунтов на квадратный дюйм, в зависимости от сплава
- Коэффициент линейного теплового расширения — 8.6 х 10-6 К-1 (это немного меньше стали, но вдвое меньше алюминия)
- Точка плавления — 1668 C (или 3135 F, что на 400 градусов выше стали и на 2000 градусов выше алюминия)
- Температура кипения — 3287 ° C
- Плотность — 4,506 г · см − 3 (около 60% плотности железа)
- Теплопроводность — 21,9 Вт м-1 K-1
- На 45% легче стали и на 60% тяжелее алюминия
Поскольку титан настолько прочен и нетоксичен, он часто используется в медицинском оборудовании, например, в заменителях коленного сустава, кардиостимуляторах, черепных пластинах и даже в качестве корневого устройства для дентальных имплантатов.С другой стороны, его способность противостоять коррозии делает его ценным материалом в химической и морской промышленности. Однако, поскольку это очень плохой проводник электричества, его использование в качестве проводника ограничено.
Хотя титан тяжелее алюминия, разница в прочности означает, что для выполнения этой работы потребуется гораздо меньше титана. Другими словами, можно использовать меньшее количество титана для получения тех же результатов на меньшем пространстве.
Алюминий
Алюминий — это экономичный вариант, который предлагает хорошее соотношение веса и прочности при сравнительно невысокой цене.Это надежный, прочный металл с хорошей коррозионной стойкостью и высокой вязкостью разрушения. Он имеет тускло-серебристый вид, что является результатом тонкого слоя оксида алюминия, который образуется почти сразу после воздействия воздуха. Его больше, чем титана, но что действительно снижает цену, так это простота изготовления.
- Предел прочности на разрыв — в чистом виде алюминий не обладает очень высокой прочностью на разрыв, поэтому обычно его легируют с другими металлами.
- Коэффициент линейного теплового расширения — 23.1 х 10-6 К-1
- Точка плавления — 660,4 ° C
- Температура кипения — 2467 ° C
- Плотность — 2,7 г / см -3 (около 1/3 стали или меди, поэтому он сравнительно легкий)
- Теплопроводность — 235 Вт м-1 K-1
Алюминий обладает хорошей устойчивостью к большинству кислот, но менее устойчив к щелочам. У него действительно хорошая теплопроводность (в 3 раза лучше, чем у стали), поэтому его часто используют в кулинарии, а поскольку он нетоксичен, мы также используем его для изготовления посуды и других продуктов, которые мы используем для еды.Он также имеет хорошую электропроводность (примерно в 10 раз лучше, чем у титана), поэтому его регулярно используют в качестве проводника.
Изучение точечных дефектов и примесей в титане из первых принципов
Титан в чистом виде при комнатной температуре и атмосферном давлении кристаллизуется в ГПУ-структуре с симметрией пространственной группы P6 3 / mmc (международная космическая группа № 194). Кристаллическая структура содержит два атома на примитивную ячейку. 32 Параметры решетки, определенные в результате экспериментов и теоретических исследований, показаны в таблице 1, где вычисленные значения с использованием функционалов обменно-корреляции, таких как приближение локальной плотности (LDA 33 ) и две различные параметризации приближения обобщенного градиента (GGA ), PW’91 34 и PBE.
32 Параметры решетки, определенные в результате экспериментов и теоретических исследований, показаны в таблице 1, где вычисленные значения с использованием функционалов обменно-корреляции, таких как приближение локальной плотности (LDA 33 ) и две различные параметризации приближения обобщенного градиента (GGA ), PW’91 34 и PBE.
Чтобы сравнить относительную стабильность различных дефектов, мы вычисляем энергию образования, которая получается из полные энергии рассчитываются из DFT. Энергия формации задается как: 35,36,37
$$ E_f \ left ({\ mathrm {D}} \ right) = E _ {{\ mathrm {Supercell}}} \ left ({\ mathrm { D}} \ right) — E _ {{\ mathrm {Ti}} — {\ mathrm {host}}} — pn_X \ mu _X $$
(1)
Здесь E f (D) — это энергия образования дефекта D, которая измеряется в эВ / суперячейка, E Supercell (D) и E Ti-host — это полная энергия дефекта и чистая ячейка. суперячейки соответственно. мкм X — химический потенциал видов X и n X — количество таких примесей в дефектной суперячейке. p = ± 1 в зависимости от того, удаляется ли атом из суперячейки-хозяина или добавляется к ней для создания дефектной суперячейки. Концентрация точечных дефектов пропорциональна экспоненте энергии образования. Энергия образования также помогает определить коэффициент диффузии для кинематики дефектов. 38 Однако первые принципы определения энергии формации, рассчитанной по формуле. (1) зависит от выбора μ X ; следовательно, правильный выбор химических потенциалов улучшает интерпретацию энергий формации. В нашем исследовании мкм X Значения выбираются из чистого состояния примесей, называемых химическими потенциалами «элементов», а оксиды соответствующих примесных элементов называются химическими потенциалами «оксидов».Подробности об источниках μ X и их роль в термодинамике представлена во вспомогательной информации.
В нашем исследовании мкм X Значения выбираются из чистого состояния примесей, называемых химическими потенциалами «элементов», а оксиды соответствующих примесных элементов называются химическими потенциалами «оксидов».Подробности об источниках μ X и их роль в термодинамике представлена во вспомогательной информации.
Отметим, что LDA и GGA не позволяют предсказывать свойства основного состояния сильно коррелированных систем, в первую очередь оксидов переходных металлов, проявляющих сегнетоэлектричество, сверхпроводимость, переходы металл-изолятор и магнетизм. Проблема является более острой для свойств полупроводников и магнитных свойств, а не для простых металлических элементов.Ситуацию в идеале можно преодолеть, включив термин «кулоновское отталкивание», специфичный для конкретного элемента и орбитально-селективный, под названием Hubbard U (метод DFT + U ). Однако нет единого мнения об использовании конкретного значения U для всех расчетов, поскольку значения не подлежат передаче. Фактическое значение U меняется в зависимости от элементов переходных металлов и их соответствующих соединений. Это дополнительно осложняется тем фактом, что не ожидается, что значение U будет одинаковым для разных кристаллических структур одного и того же элемента или соединения.Таким образом, полная энергия зависит от значения U в методе DFT + U . Поскольку полная энергия является основой нашего анализа, мы пытаемся здесь избежать неоднозначностей, которые могут возникнуть из-за включения двух различных уровней теории, DFT и DFT + U и изменения значения U индивидуально для каждого элемента.
Межузельные атомы
Атомы титана, занимающие межузельные узлы решетки, являются межузельными атомами. В кристаллической решетке ГПУ межузельный дефект может располагаться в шести узлах элементарной ячейки, как показано на рис. 1. 39 Они называются ортогональными (O) и тетраэдрическими (T) узлами. Примеси в базально-тетраэдрических (BT) и базально-октаэдрических (BO) узлах лежат в базисной плоскости, на полпути между двумя соседними узлами T и узлами O вдоль направления c, соответственно. Краудионы представляют собой интерстициальные позиции между центром связи Ti – Ti, и были идентифицированы две различные конфигурации: базальный (CB) и небазальный (CN) краудионы. В отличие от этих примесных узлов, которые могут содержать только один примесный атом на узел, димероподобные межузельные точечные дефекты содержат два атома.Два атома димероподобной примеси симметрично смещены относительно вакантного узла решетки. Из-за гексагональной симметрии существуют две ориентации димероподобных точечных дефектов. Конфигурация гантели, ориентированная в направлении c (DC), и конфигурация гантели, лежащая в базовой плоскости (DB), являются уникальным выбором. Конфигурации DC и DB представляют собой разделенные межстраничные объявления, которые являются разновидностями самостоятельных межстраничных объявлений. Расположение всех восьми межузельных конфигураций показано на схематическом изображении рис.1. Энергии образования суммированы для восьми межузельных конфигураций в Ti, перечисленных в Таблице 2. Сверхъячейка состоит из периодического повторения элементарных ГПУ элементарных решеток, внутри которых размещены примесные атомы. Эта суперячейка геометрически оптимизирована схемой сопряженного градиента, чтобы минимизировать внутреннюю деформацию. Характерные положения примесей в оптимизированной суперячейке устанавливаются путем исследования ближайшего соседа. Разность энергий образования и разность полной энергии для изолированных межузельных дефектов идентичны.Однако энергия образования имеет преимущество, поскольку она позволяет сравнивать расщепленную межузельную энергетику со случаями конфигураций дефектов замещения и межузельных дефектов.
1. 39 Они называются ортогональными (O) и тетраэдрическими (T) узлами. Примеси в базально-тетраэдрических (BT) и базально-октаэдрических (BO) узлах лежат в базисной плоскости, на полпути между двумя соседними узлами T и узлами O вдоль направления c, соответственно. Краудионы представляют собой интерстициальные позиции между центром связи Ti – Ti, и были идентифицированы две различные конфигурации: базальный (CB) и небазальный (CN) краудионы. В отличие от этих примесных узлов, которые могут содержать только один примесный атом на узел, димероподобные межузельные точечные дефекты содержат два атома.Два атома димероподобной примеси симметрично смещены относительно вакантного узла решетки. Из-за гексагональной симметрии существуют две ориентации димероподобных точечных дефектов. Конфигурация гантели, ориентированная в направлении c (DC), и конфигурация гантели, лежащая в базовой плоскости (DB), являются уникальным выбором. Конфигурации DC и DB представляют собой разделенные межстраничные объявления, которые являются разновидностями самостоятельных межстраничных объявлений. Расположение всех восьми межузельных конфигураций показано на схематическом изображении рис.1. Энергии образования суммированы для восьми межузельных конфигураций в Ti, перечисленных в Таблице 2. Сверхъячейка состоит из периодического повторения элементарных ГПУ элементарных решеток, внутри которых размещены примесные атомы. Эта суперячейка геометрически оптимизирована схемой сопряженного градиента, чтобы минимизировать внутреннюю деформацию. Характерные положения примесей в оптимизированной суперячейке устанавливаются путем исследования ближайшего соседа. Разность энергий образования и разность полной энергии для изолированных межузельных дефектов идентичны.Однако энергия образования имеет преимущество, поскольку она позволяет сравнивать расщепленную межузельную энергетику со случаями конфигураций дефектов замещения и межузельных дефектов.
 1
1 Схематическая кристаллическая структура, показывающая положения различных типов собственных междоузлий в решетке ГПУ Ti. Положения тетраэдрической (T), ортогональной (O), базовой тетраэдрической (BT), базовой ортогональной (BO), краудиона в базальной (CB) и небазальной (CN) плоскостях, а также разделенного интерстициального пространства вдоль c Обозначены -направления (DC) и в базисной плоскости (DB).В таблице 2 приведена относительная стабильность этих дефектов в Ti-матрице
Таблица 2 Сравнение E f (в эВ на суперячейку) для восьми конфигураций межузельных связей (показанных на рис. 1) Длина связи рассыпавшихся межузелий была рассчитана как 1,663 и 1,930 Å для DC и DB, соответственно. Начальная геометрия была выбрана путем выбора конфигурации с наименьшей полной энергией после выполнения проверки полной энергии как функции длины связи пары примесей в чистой решетке.Энергии пласта показаны в Таблице 2 для начальных ( E f U ) и расслабленный ( E f R ) суперячейки для различных конфигураций. Другими словами, E f U указывает энергию примесных межузельных димеров, когда основные атомы не релаксированы. Разница в энергии (Δ E f UR = E f U — E f R ) объясняет выигрыш химической энергии за счет локальных искажений решетки.Длины связей Ti – Ti составляют 1,430 и 1,463 Å для конфигураций CN и CB, соответственно, что составляет примерно половину постоянной равновесной решетки. Δ E f UR кажется большим для краудонных межстраничных объявлений; 9,4 и 9,8 эВ для CB и CN соответственно из-за величины E f U , который уже является большим из-за дополнительного атома Ti между равновесными связями Ti – Ti. По сравнению с этим, разница в энергии Δ E f UR является минимальным для разделенных межузельных конфигураций, DC и DB, так как два примесных атома расположены в межузельной области близко к их равновесному разделению из-за способа приготовления моделей DC и DB.
По сравнению с этим, разница в энергии Δ E f UR является минимальным для разделенных межузельных конфигураций, DC и DB, так как два примесных атома расположены в межузельной области близко к их равновесному разделению из-за способа приготовления моделей DC и DB.
Мы обнаружили, что конфигурация BO является наиболее подходящей внутренней конфигурацией. Энергия конфигурации CB аналогична энергии конфигурации BO.{\ mathrm {U}} \) в таблице 2).
Вакансия-межузельные пары
Энергия образования атома, отсутствующего в узле решетки, т. Е. Вакансии ( V Ti , не путать с ванадием, замещенным в узле Ti, V Ti ), составляет вычисляется как
$$ E_f \ left ({V _ {{\ mathrm {Ti}}}} \ right) = E \ left ({{\ mathrm {Ti}} + V _ {{\ mathrm {Ti}}}}} \ right) — \ mu _ {{\ mathrm {Ti}}} $$
(2)
, где E — полная энергия, а значение μ Ti , полученное из массы Ti, оказывается равным 1.94 эВ, что аналогично значению, полученному при расчетах сверхмягких псевдопотенциалов. 40 Энергии вакансий Ti получены в аналогичном диапазоне с другими обменно-корреляционными функционалами, 41 , которые завышены, чем указано в эксперименте (1,55 эВ в ссылке 42 и 1,27 эВ по спектроскопии аннигиляции позитронов в ссылке. 43 ). Расхождение связано с отсутствием обменной корреляции на основе плотности для точной обработки электронной корреляции. 44 Есть способ преодолеть ограничения GGA, добавив поправочный член Хаббарда U . Однако в нашем исследовании это не использовалось из-за неоднозначности, которую он вносит в обработку химических потенциалов, влияющих на расчет энергий формации. Энергетика показывает, что величина энергии образования вакансий сравнима с величиной энергии межузельных связей, см. Таблицу 2. Таким образом, можно предположить, что и вакансии, и межузельные частицы, вероятно, будут одновременно реагировать на термодинамические возмущения, которые могут быть объединены для получения механизм миграции для перехода атома Ti из положения решетки в ближайшее межузельное положение.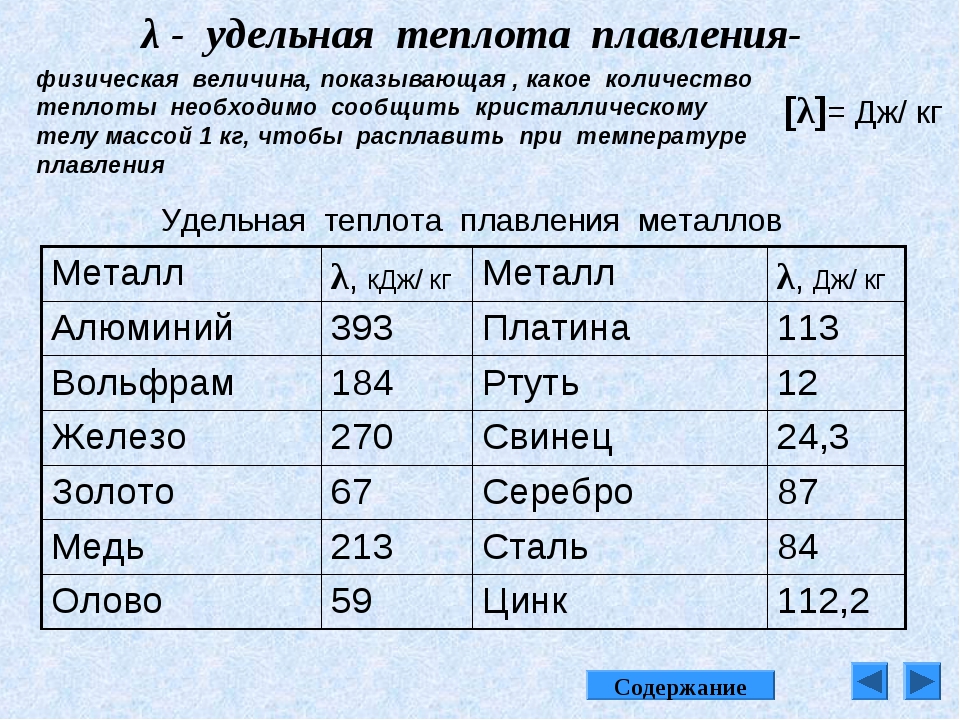 Рассмотрение мкм Ti , полученного из объемных моделей Ti, включает ситуацию, когда решетка вакансий находится в термодинамическом равновесии с идеальным объемным Ti. Однако это может быть нереалистично в технологических процессах, особенно если интересующий смещенный атом Ti остается глубоко в объеме образца, образуя вторичные фазы с другими дефектами / примесями в решетке. Наиболее тривиальным случаем для нашего обсуждения были бы комплексы дефектов, состоящие из вакансии и собственной межузельной примеси.
Рассмотрение мкм Ti , полученного из объемных моделей Ti, включает ситуацию, когда решетка вакансий находится в термодинамическом равновесии с идеальным объемным Ti. Однако это может быть нереалистично в технологических процессах, особенно если интересующий смещенный атом Ti остается глубоко в объеме образца, образуя вторичные фазы с другими дефектами / примесями в решетке. Наиболее тривиальным случаем для нашего обсуждения были бы комплексы дефектов, состоящие из вакансии и собственной межузельной примеси.
Чтобы получить представление о дефектных комплексах, мы рассчитали энергию образования пары V Ti — межузельный Ti как функцию разделения отдельных компонентов, то есть вакансии титана, V Ti и межузельный атом титана. Модели Supercell были подготовлены с промежуточным Ti в конфигурации BO и V Ti , созданным в различных положениях, так что расстояние V Ti от промежуточного Ti равно 2.15, 4.20, 4.58, 6.44 и 9.23 Å. После минимизации внутренних сил в суперячейках (геометрическая оптимизация) было обнаружено, что для первых трех более коротких парных разделений ожидается, что межузельный Ti будет притягиваться к пустому узлу решетки, что может привести к устранению дефекта. Однако при больших расстояниях 6,44 и 9,23 Å взаимодействие между V Ti и межузельным атомом титана экранируется атомами хозяина между ними. В результате V Ti и межузельный атом Ti захватываются в локальные энергетические минимумы без какого-либо заметного изменения расстояния между ними.Энергии образования для трех самых коротких разделительных расстояний идентичны и почти на 3,9 эВ ниже энергии образования двух больших расстояний. В идеале из энергетики можно было бы ожидать, что вакансии и межузельные частицы должны аннигилировать друг друга и, таким образом, восстановить среду идеальной ГПУ-решетки, если эти дефекты находятся в непосредственной близости.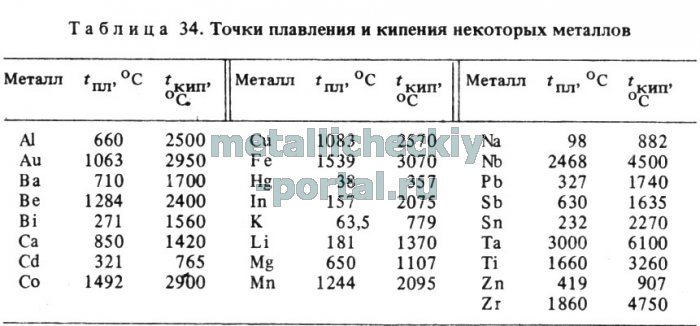
Примеси внедрения и замещения
Энергии образования примесей для позиций внедрения и замещения в решетке ГПУ Ti рассчитываются на основе «элементарных» химических потенциалов ( мкм элемент ) и химических потенциалов «оксида» ( мкм оксид ), см. Дополнительную информацию, которая указана в таблицах 3 и 4 соответственно.Например, на рис. 2а показаны рассчитанные энергии образования примеси O в Ti. Энергии образования в нижнем диапазоне получены из полной энергии молекулы O 2 , что можно интерпретировать как термодинамическое состояние с богатой кислородом окружающей средой, в то время как энергии образования в направлении верхнего диапазона получены из TiO 2 в структура рутила, которую можно интерпретировать как термодинамическое состояние с дефицитом кислорода в среде. Горизонтальные пунктирные линии на этом рисунке обозначают конфигурацию с самыми низкими энергиями формации в каждом случае.Наблюдается, что атом O предпочитает октаэдрическое межузельное положение, когда окружающая среда является дефицитной по кислороду. С другой стороны, в среде с богатым поступлением кислорода термодинамически стабильной фазой являются пары примесей кислорода, приводящие к конфигурациям DB и DC (см. Рис. 1). Относительные различия в энергиях образования позиций внедрения и замещения для двух типов химического окружения можно оценить по данным рис. 2а.
Таблица 3 Энергии образования (в эВ на сверхъячейку) примесей в различных положениях в ГПУ Ti (см. Рис.1) Таблица 4 Энергии образования (в эВ на сверхъячейку) примесей в различных положениях в ГПУ Ti (см. Рис. 1) Рис. 2 Сравнение энергий образования примесных элементов в различных положениях внедрения и на замещающей сайт. Примесь O выбрана в качестве примера в ( a ). Нижний и верхний диапазоны энергий пласта получены с использованием μ оксида и μ элемента , полученного из молекулы O 2 и твердого вещества TiO 2 , соответственно, значения которых показаны пунктирными горизонтальными линиями. b Минимальное значение энергии образования исследуемых примесей от двух источников химических потенциалов. Символы соответствуют конфигурациям примесей, как в ( a ). Энергии формирования данных для выбранных элементов 3d, 4d и 5d показаны на заштрихованном (желтом) фоне.
b Минимальное значение энергии образования исследуемых примесей от двух источников химических потенциалов. Символы соответствуют конфигурациям примесей, как в ( a ). Энергии формирования данных для выбранных элементов 3d, 4d и 5d показаны на заштрихованном (желтом) фоне.
Чем ниже энергия образования конфигурации дефекта, тем выше вероятность обнаружения такого дефекта в образце. На рис. 2b показаны самые низкие значения энергии образования, полученные для различных элементов, от H (атомный номер = 1) до Ca (атомный номер = 20), за исключением элементов из благородных газов He и Ne.Дополнительные выбранные элементы из элементов переходных металлов серий 3d, 4d и 5d, V, Ni, Cu, Zr, Mo, Ag, Ta, W, Au и Pb, рассматриваются для сравнения тенденции энергий образования элементов для относительно больший размер атома. Энергии образования в этих случаях показаны заштрихованной областью на рис. 2б. Тенденция самых низких энергий образования (среди различных конфигураций примесей) на фиг. 2b, которая получена из элемента мкм, , отмечена красной линией.Энергии образования, полученные из мкм оксида , отмечены синей линией на том же рисунке. Было обнаружено, что эти обработки химическим потенциалом приводят к двум различным тенденциям наименьшей энергии пласта.
В общем, металлические примеси, независимо от их атомных размеров и воздействия химического окружения (учет двух различных химических потенциалов), благоприятствуют центрам замещения. С другой стороны, обычные высоко электроотрицательные элементы, такие как C, N, O, F, S и Cl, не благоприятствуют замещающему сайту.Вместо этого элементы C, N и Cl предпочитают октаэдрические межузельные участки для двух химических сред. H, O и S стабилизируют различные конфигурации примесей при различной обработке химическим потенциалом: октаэдрические конфигурации примесей для μ оксида и конфигурации примесных димеров (DB и DC) для μ элемента . Фтор — единственный элемент, который образует примесный димер в Ti для обоих типов химических потенциалов. Следует подчеркнуть, что H, который может легко потерять свой электрон, образуя катион H + , на самом деле ведет себя аналогично электроотрицательным элементам при введении в качестве примеси в Ti.Этот результат подтверждает анализ переноса заряда, в котором H приобретает электроны от соседних атомов Ti, что обсуждается в следующем разделе.
Фтор — единственный элемент, который образует примесный димер в Ti для обоих типов химических потенциалов. Следует подчеркнуть, что H, который может легко потерять свой электрон, образуя катион H + , на самом деле ведет себя аналогично электроотрицательным элементам при введении в качестве примеси в Ti.Этот результат подтверждает анализ переноса заряда, в котором H приобретает электроны от соседних атомов Ti, что обсуждается в следующем разделе.
Анализ заряда
Химическая гибридизация играет важную роль для конфигурации примесных атомов в решетках хозяина. Идеальной мерой силы орбитальной гибридизации является перенос заряда между примесью и атомами хозяина. Анализ заряда Бадера 45,46 обеспечивает количественную оценку сопровождаемого переноса заряда.{{\ mathrm {hybridized}}} \) — это рассчитанный заряд Бейдера после того, как были получены решения самосогласованного поля. Согласно этому определению отрицательные значения для Δ q B ( X ) будет означать накопление заряда от соседства к атомному узлу X (определение согласуется с определением заряда электрона, рассматриваемого как отрицательный), тогда как положительное значение будет означать потерю заряда из атомного узла X к окружающему.Тенденция Δ q B Ожидается, что значение ( X ) для примесных и основных атомов будет обратно пропорционально, так как потеря или накопление заряда в примесном узле должны коррелировать с изменениями заряда в соседних основных атомах. Отрицательные значения Δ q B являются характеристикой, общей для электроотрицательных примесей, таких как C, N, O и F. Перенос заряда на соседний основной Ti (<Δ q B (Ti)>) усредняется по координации 4, 6 и 12 ближайших соседей для примесного атома, расположенного в тетраэдрических, октаэдрических и замещающих примесных узлах соответственно.
Перенос заряда между примесными атомами и ближайшими соседними основными атомами Ti показан как функция атомного номера (кроме благородных газов) на рис. 3а для октаэдрических и замещающих примесных узлов. Перенос заряда следует той же тенденции периодов в периодической таблице для обоих примесных сайтов. Средний перенос заряда на Ti меньше по величине, потому что несколько атомов Ti из соседней связи связаны с атомом примеси. Перенос заряда примесным атомам в октаэдрических межузельных узлах и позициях замещения различается в зависимости от среднего переноса заряда Ti, как показано на рис.3b. Синие и черные сплошные линии представляют собой линии тренда для данных о примесях в октаэдрических положениях внедрения и замещения, соответственно. Из рис. 3b видно, что перенос заряда на примеси в случаях замещения (наклон черной линии) обычно больше, чем для октаэдрических позиций примеси (наклон синей линии). Та же информация также изображена на рис. 3a, где мы отмечаем разницу в значениях переноса заряда между случаями замещения (закрашенные квадраты) и промежуточными (белый кружок) случаями.Как уже указывалось в предыдущем разделе, H в металлическом Ti имеет отрицательные значения Δ q B . как для случая замещения, так и для случая внедрения (см. Рис. 3a, b), предполагая, что он действует как примесь, притягивающая электроны, аналогично C, O и F.
Рис. 3a Перенос заряда между примесью и соседние атомы Ti. b Сравнение тенденции переноса заряда для примесей в октаэдрических положениях внедрения и замещения
Предпочтительные конфигурации для рассмотренных элементов приведены на рис.4, где энергии образования примесей замещения сравниваются с минимальной энергией образования из межузельных конфигураций. Установлено, что высоко электроотрицательные элементы, H, C, N, O, F, S и Cl, благоприятствуют межузельным положениям (см. Рис. 2b. Химическая гибридизация играет более решающую роль, чем другие конкурирующие термины. Линия y = x — случай, когда как примеси замещения, так и примеси замещения равновероятны.Чем дальше от этой линии, тем выше вероятность появления примесей замещения или замещения.Случаи примесей P и Ni отклоняются от ожидаемого поведения. Другими словами, их энергии образования лежат относительно близко к линии y = x . Интуитивно ожидается, что P будет благоприятствовать промежуточному положению, тогда как ожидается, что Ni будет благоприятствовать замещающему сайту. Пересмотр исходных соединений, из которых происходит химический потенциал, потенциально может помочь исправить это несоответствие. Кроме того, для Ni трудность может заключаться в величине химического потенциала, который является производным оксидного соединения NiO.NiO является примером соединения, в котором приближение GGA не учитывает сильные эффекты электронной корреляции. 47
Линия y = x — случай, когда как примеси замещения, так и примеси замещения равновероятны.Чем дальше от этой линии, тем выше вероятность появления примесей замещения или замещения.Случаи примесей P и Ni отклоняются от ожидаемого поведения. Другими словами, их энергии образования лежат относительно близко к линии y = x . Интуитивно ожидается, что P будет благоприятствовать промежуточному положению, тогда как ожидается, что Ni будет благоприятствовать замещающему сайту. Пересмотр исходных соединений, из которых происходит химический потенциал, потенциально может помочь исправить это несоответствие. Кроме того, для Ni трудность может заключаться в величине химического потенциала, который является производным оксидного соединения NiO.NiO является примером соединения, в котором приближение GGA не учитывает сильные эффекты электронной корреляции. 47
Сравнение энергий образования между сайтом замещения (по оси абсцисс) и наиболее подходящей межузельной конфигурацией (по оси ординат). Линия y = x показывает четкое разделение и предлагает благоприятную конфигурацию точечного дефекта
All About Titanium
химический элемент в периодической таблице, который имеет символ Ti и атомный номер 22.Это легкий, прочный, блестящий, коррозионно-стойкий (в том числе стойкий к морской воде и хлору) переходный металл бело-серебристо-металлического цвета. Титан используется в прочных легких сплавах (особенно с железом и алюминием), а также в порошковой форме для других материалов, таких как графитовые композиты. Его наиболее распространенное соединение, диоксид титана, используется в белых пигментах. Примерами использования белого пигмента, состоящего из оксида титана, являются корректирующая жидкость и обычно используемая белая краска для перекраски стен.Он также используется в зубной пасте, белых красках для разметки дорог и в белых фейерверках. Вещества, содержащие титан, называют титаносодержащими.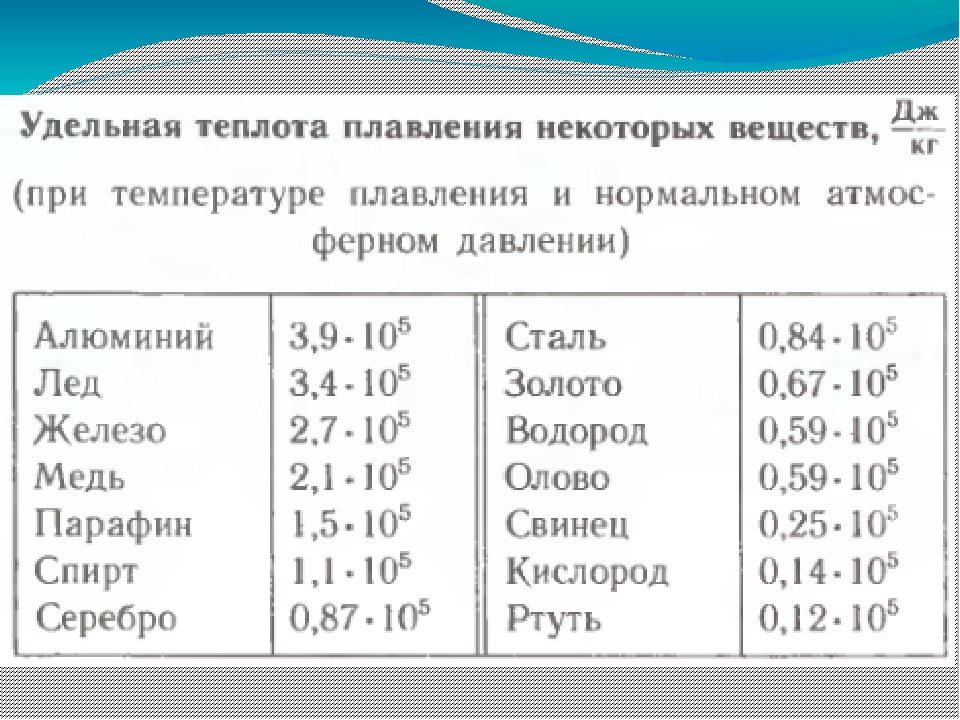
Этот элемент встречается во многих минералах, основными источниками которых являются рутил и ильменит, которые широко распространены на Земле. Есть две аллотропные формы и пять встречающихся в природе изотопов этого элемента; От 46Ti до 50Ti, причем 48Ti является наиболее распространенным (73,8%). Одна из самых примечательных характеристик титана — то, что он прочен, как сталь, но составляет всего 60% от его плотности.Свойства титана химически и физически подобны цирконию.
Известные характеристики
Титан хорошо известен своей превосходной устойчивостью к коррозии; он почти так же устойчив, как платина, и способен противостоять воздействию кислот, влажного газообразного хлора и растворов обычных солей. Чистый титан не растворяется в воде, но растворяется в концентрированных кислотах. Металлический элемент, он также известен своим высоким отношением прочности к весу. Это легкий, прочный металл с низкой плотностью, который в чистом виде является довольно пластичным (особенно в бескислородной среде), легким в обработке, блестящим и металлически-белым цветом.Относительно высокая температура плавления этого элемента делает его полезным в качестве тугоплавкого металла. Технически чистые сорта титана имеют предел прочности на растяжение, равный пределу прочности при растяжении высокопрочных низколегированных сталей, но на 43% легче. Титан на 60% тяжелее алюминия, но более чем в два раза прочнее алюминиевого сплава 6061-T6; эти числа могут существенно различаться из-за различных составов сплавов и технологических параметров.
Этот металл образует пассивное и защитное оксидное покрытие (ведущее к коррозионной стойкости) при воздействии повышенных температур на воздухе, но при комнатной температуре он сопротивляется потускнению.Металл, который горит при нагревании на воздухе до 610 ° C или выше (образуя диоксид титана), также является одним из немногих элементов, который горит в чистом газообразном азоте (он горит при 800 ° C и образует нитрид титана).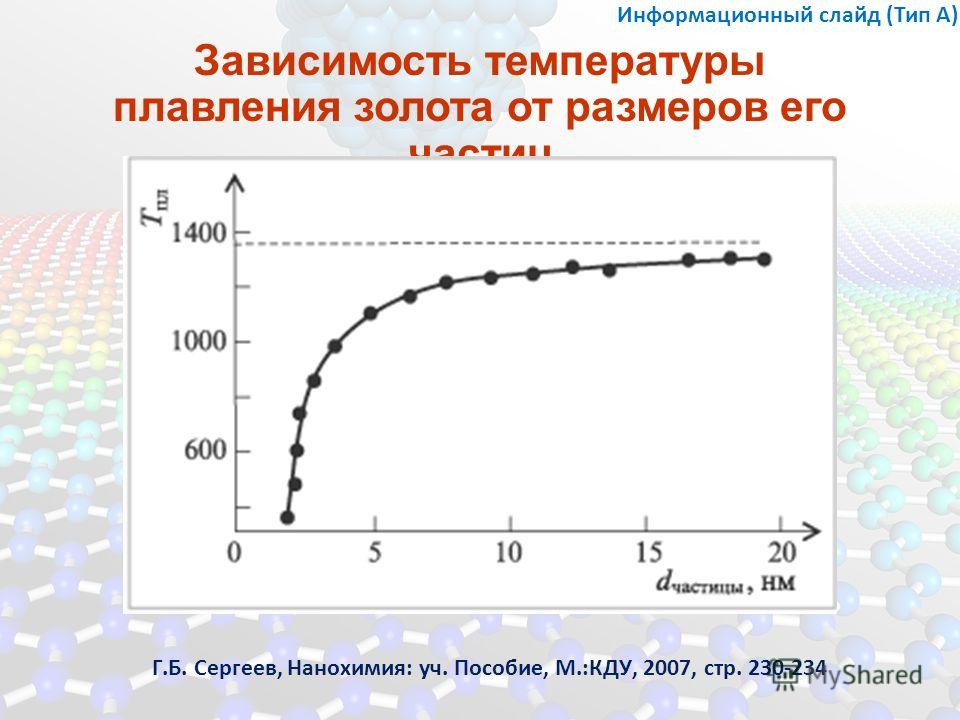 Титан устойчив к разбавленной серной и соляной кислоте, а также к газообразному хлору, растворам хлоридов и большинству органических кислот. Он парамагнитен (слабо притягивается к магнитам) и имеет очень низкое электрическое сопротивление и теплопроводность.
Титан устойчив к разбавленной серной и соляной кислоте, а также к газообразному хлору, растворам хлоридов и большинству органических кислот. Он парамагнитен (слабо притягивается к магнитам) и имеет очень низкое электрическое сопротивление и теплопроводность.
Эксперименты показали, что природный титан становится радиоактивным после бомбардировки дейтронами, излучающими в основном позитроны и жесткие гамма-лучи.Металл представляет собой диморфный аллотроп с гексагональной альфа-формой, очень медленно превращающейся в кубическую бета-форму при температуре около 880 C. Когда он раскалывается докрасна, металл соединяется с кислородом, а когда он достигает 550 C, он соединяется с хлором. Он также реагирует с другими галогенами и поглощает водород.
Приложения
Около 95% производства титана потребляется в виде диоксида титана (TiO2), интенсивно белого перманентного пигмента с хорошей укрывистостью в красках, бумаге, зубной пасте и пластмассах.Краски, содержащие диоксид титана, отлично отражают инфракрасное излучение и поэтому широко используются астрономами и в красках для наружных работ. Он также используется в цементе, в драгоценных камнях, в качестве оптического глушителя для бумаги (Smook 2002) и в качестве упрочняющего агента в графитовых композитных удилищах и клюшках для гольфа. В последнее время его стали использовать в очистителях воздуха (в качестве фильтрующего покрытия) или в оконной пленке на зданиях, которые при воздействии ультрафиолетового излучения (солнечного или искусственного) и содержания влаги в воздухе превращают нефильтрованные загрязнения воздуха в гидроксильные радикалы. .
Благодаря высокой прочности на разрыв (даже при высоких температурах), небольшому весу, исключительной коррозионной стойкости и способности выдерживать экстремальные температуры титановые сплавы используются в самолетах, бронировании, военно-морских кораблях, космических кораблях и ракетах. Он используется в стальных сплавах для уменьшения размера зерна и в качестве раскислителя, а также в нержавеющей стали для уменьшения содержания углерода. Титан часто легируют алюминием (для уменьшения размера зерна), ванадием, медью (для упрочнения), железом, марганцем, молибденом и другими металлами.
Титан часто легируют алюминием (для уменьшения размера зерна), ванадием, медью (для упрочнения), железом, марганцем, молибденом и другими металлами.
Сварные титановые трубы используются в химической промышленности из-за их коррозионной стойкости и все чаще используются при бурении нефтяных скважин, особенно на шельфе, благодаря своей прочности, легкому весу и коррозионной стойкости.
Титан, легированный ванадием, используется в наружной обшивке самолетов, противопожарных стенках, шасси и гидравлических трубах. Согласно годовому отчету Titanium Metals за 2004 год, около 58 тонн металла используется в Boeing 777, 43 в 747, 18 в 737, 24 в Airbus A340, 17 в A330 и 12 в A320. Корпорация.Как правило, более новые модели используют больше, а широкофюзеляжные — больше всего. A380 может использовать 77 тонн, в том числе около 10 или 11 тонн в двигателях.
Использование титана в потребительских товарах, таких как теннисные ракетки, клюшки для гольфа, велосипеды, лабораторное оборудование, наручные часы, обручальные кольца и портативные компьютеры, становится все более распространенным.
Другое использование:
- Благодаря отличной устойчивости к морской воде, он используется для изготовления гребных валов и оснастки, а также в теплообменниках опреснительных установок и в нагревателях-охладителях для аквариумов с соленой водой, а в последнее время и в водолазных ножах.
- Благодаря своей прочности и инертности по отношению к морской воде, а также значительным запасам руды в России, он был основным материалом, который использовался при строительстве многих современных российских подводных лодок, в том числе самых глубоких на сегодняшний день военных подводных лодок класса «Альфа» и «Майк». а также класс Тайфун.
- Используется для производства относительно мягких искусственных драгоценных камней.
- Тетрахлорид титана (TiCl4), бесцветная жидкость, используется для радужной окраски стекла и, поскольку он сильно дымится во влажном воздухе, его также используют для изготовления дымовых завес и для рисования на небе.

- Помимо того, что это очень важный пигмент, диоксид титана также используется в солнцезащитных кремах из-за его устойчивости к ультрафиолетовому излучению.
- Поскольку этот металл считается физиологически инертным, этот металл используется в имплантатах для замены суставов, таких как тазобедренные суставы и впадины, а также для изготовления медицинского оборудования и футеровки труб / резервуаров в пищевой промышленности. Поскольку титан неферромагнитен, пациентов с титановыми имплантатами можно безопасно обследовать с помощью магнитно-резонансной томографии (удобно для долгосрочных имплантатов).
- Титан также используется для изготовления хирургических инструментов, используемых в хирургии под визуальным контролем.
- Его инертность и способность красиво окрашиваться делают его популярным металлом для пирсинга.
- Титан обладает необычной способностью к остеоинтеграции, что позволяет использовать его в дентальных имплантатах. Эта способность также используется некоторыми ортопедическими имплантатами. В ортопедических применениях также используется более низкий модуль упругости титания, чтобы более точно соответствовать модулю упругости кости, для восстановления которой такие устройства предназначены.В результате скелетные нагрузки более равномерно распределяются между костью и имплантатом, что снижает вероятность деградации кости из-за защиты от напряжения и перипротезных переломов кости, которые возникают на границах ортопедических имплантатов, которые действуют как концентраторы напряжения. Однако жесткость титановых сплавов по-прежнему более чем в два раза превышает жесткость кости, что в конечном итоге приводит к разрушению суставов.
- Титановые сплавы также используются для изготовления оправ для очков. В результате получается довольно дорогой, но очень прочный и долговечный каркас.В этом приложении находят применение как традиционные сплавы, так и сплавы с памятью формы.
- Многие туристы используют титановое снаряжение, включая кухонную утварь, столовые приборы, фонари и колья для палаток.
 Хотя эти изделия из титана немного дороже традиционных стальных или алюминиевых альтернатив, они могут быть значительно легче без ущерба для прочности. Однако некоторые утверждают, что тепловые свойства титановой посуды делают ее непригодной для серьезных кулинарных применений.
Хотя эти изделия из титана немного дороже традиционных стальных или алюминиевых альтернатив, они могут быть значительно легче без ущерба для прочности. Однако некоторые утверждают, что тепловые свойства титановой посуды делают ее непригодной для серьезных кулинарных применений. - Титан все чаще используется в валах клюшек для лакросса.
- Титан все чаще используется в решетках для крикетных шлемов.
- Титан может быть анодирован для получения различных цветов. [1] [2]
- Титан также присутствует в фейерверках.
- Титан выпускается в форме фольги, листа, проволоки, гранул, губки, наноразмерного активированного порошка, порошка, сетки и стержня.
Время от времени при строительстве использовался титан: 150-футовый (45-метровый) мемориал Юрию Гагарину, первому человеку, отправившемуся в космос, в Москве, сделан из титана из-за привлекательного цвета металла и его ассоциации с ракетной техникой.Музей Гуггенхайма в Бильбао и библиотека Серритоса были первыми зданиями в Европе и Северной Америке, соответственно, которые были обшиты титановыми панелями.
История
Титан был обнаружен в Криде, Корнуолл, в Англии геологом-любителем преподобным Уильямом Грегором в 1791 году. Он обнаружил присутствие нового элемента в ильмените и назвал его менахитом (альтернативно пишется манакканитом) в честь близлежащего прихода Манаккан [3]. Примерно в то же время Франц Йозеф Мюллер также произвел подобное вещество, но не смог его идентифицировать.Этот элемент был независимо открыт несколько лет спустя немецким химиком Мартином Генрихом Клапротом в рутиловой руде. Клапрот подтвердил, что это новый элемент, и в 1795 году назвал его в честь титанов греческой мифологии.
Металл всегда было трудно извлечь из различных руд. Чистый металлический титан (99,9%) был впервые получен в 1910 году Мэтью А. Хантером путем нагревания TiCl4 с натрием в стальной бомбе при 700-800 ° C в процессе Хантера. Металлический титан не использовался за пределами лаборатории до 1946 года, когда Уильям Джастин Кролл доказал, что титан может быть коммерчески произведен путем восстановления тетрахлорида титана магнием в процессе Кролла, который используется до сих пор.
В 1950-1960-х годах Советский Союз пытался захватить мировой рынок титана в качестве тактики холодной войны, чтобы помешать американским военным использовать его. Несмотря на эти усилия, США получили большие объемы титана, когда европейская компания создала прикрытие для закупок его иностранными спецслужбами США. Действительно, титан для очень успешного американского разведывательного самолета SR-71 был приобретен у Советского Союза в разгар холодной войны.
К 1956 г.S. производство изделий из титана составляло более 6 млн кг / год (1).
происшествие
Металлический титан всегда связан с другими элементами в природе. Он является девятым по распространенности элементом в земной коре (0,63% по массе) и присутствует в большинстве вулканических пород и в образовавшихся из них отложениях (а также в живых существах и естественных водоемах). Он широко распространен и встречается главным образом в минералах анатаз, брукит, ильменит, перовскит, рутил, титанит (сфен), а также во многих железных рудах.Из этих минералов только ильменит и рутил имеют важное экономическое значение, но даже их трудно найти в высоких концентрациях. Поскольку он легко реагирует с кислородом и углеродом при высоких температурах, трудно получить чистый металлический титан, кристаллы или порошок. Значительные месторождения титановой руды существуют в Австралии, Новой Зеландии, Скандинавии, Северной Америке и Малайзии. Большие количества были также обнаружены в районе Квале в Кении, месторождениях, права на разработку которых имеет канадская компания Tiomin.
Этот металл содержится в метеоритах и был обнаружен на Солнце и в звездах M-типа. Камни, привезенные с Луны во время миссии «Аполлон-17», состоят на 12,1% из TiO2. Титан также содержится в угольной золе, растениях и даже человеческом теле (хотя он безвреден, но не считается важным элементом).
Изоляция
Поскольку металл вступает в реакцию с воздухом при высоких температурах, его нельзя получить путем восстановления его диоксида. Таким образом, металлический титан коммерчески производится с помощью процесса Кролла, сложного и дорогостоящего периодического процесса, разработанного в 1946 году Уильямом Джастином Кроллом.В процессе Кролла оксид сначала превращается в хлорид посредством карбохлорирования, в результате чего газообразный хлор пропускается над раскаленным рутилом или ильменитом в присутствии углерода с образованием TiCl4. Его конденсируют и очищают фракционной перегонкой, а затем восстанавливают расплавленным магнием при температуре 800 ° C в атмосфере аргона.
Таким образом, металлический титан коммерчески производится с помощью процесса Кролла, сложного и дорогостоящего периодического процесса, разработанного в 1946 году Уильямом Джастином Кроллом.В процессе Кролла оксид сначала превращается в хлорид посредством карбохлорирования, в результате чего газообразный хлор пропускается над раскаленным рутилом или ильменитом в присутствии углерода с образованием TiCl4. Его конденсируют и очищают фракционной перегонкой, а затем восстанавливают расплавленным магнием при температуре 800 ° C в атмосфере аргона.
Более новый процесс, FFC Cambridge Process, может заменить старый процесс Kroll. В этом методе используется порошок диоксида титана (который представляет собой очищенную форму рутила) для получения конечного продукта, который представляет собой порошок или губку.Если используются порошки смешанных оксидов, продукт представляет собой сплав с гораздо более низкой стоимостью, чем традиционный многоступенчатый процесс плавления. Есть надежда, что Кембриджский процесс FFC сделает титан менее редким и дорогим материалом для аэрокосмической промышленности и рынка предметов роскоши, и его можно будет увидеть во многих продуктах, которые в настоящее время производятся с использованием алюминия и специальных марок стали.
Титан был очищен до сверхвысокой чистоты в небольших количествах, когда в 1925 году Антон Эдуард ван Аркель и Ян Хендрик де Бур открыли процесс йодида, или кристаллического стержня, путем реакции с йодом и разложения образовавшихся паров над горячей нитью до чистого металла.
Оксид титана получают в промышленных масштабах путем измельчения минеральной руды и смешивания ее с карбонатом калия и водной фтористоводородной кислотой. Это дает фтортитанат калия (K2TiF6), который экстрагируют горячей водой и разлагают аммиаком, образуя гидратированный оксид аммиака. Он, в свою очередь, воспламеняется в платиновом сосуде, в результате чего образуется чистый диоксид титана.
Обычные титановые сплавы получают восстановлением. Например; восстанавливаются купротитан (восстанавливается рутил с добавлением меди), железоуглеродистый титан (ильменит, восстановленный коксом в электрической печи) и манганотитан (рутил с оксидами марганца или марганца).
Например; восстанавливаются купротитан (восстанавливается рутил с добавлением меди), железоуглеродистый титан (ильменит, восстановленный коксом в электрической печи) и манганотитан (рутил с оксидами марганца или марганца).
Соединения
Степень окисления +4 преобладает в химии титана, но соединения со степенью окисления +3 также распространены. Из-за этой высокой степени окисления многие соединения титана имеют высокую степень ковалентной связи.
Хотя металлический титан относительно редко встречается, из-за стоимости добычи диоксид титана (также называемый титаном (IV), титановым белилом или даже диоксидом титана) дешев, нетоксичен, легко доступен оптом и очень широко используется в качестве белого пигмента в краска, эмаль, лак, пластмасса и строительный цемент.Порошок TiO2 химически инертен, устойчив к выцветанию на солнце и очень непрозрачен: это позволяет ему придавать чистый и блестящий белый цвет коричневым или серым химическим веществам, которые образуют большинство бытовых пластиков. В природе это соединение содержится в минералах анатазе, бруките и рутиле.
Краска, изготовленная из диоксида титана, хорошо себя чувствует при суровых температурах, в некоторой степени самоочищается и выдерживает воздействие морской среды. Чистый диоксид титана имеет очень высокий показатель преломления и оптическую дисперсию выше, чем у алмаза.Звездчатые сапфиры и рубины получают свой астеризм из-за присутствующего в них диоксида титана. Титанаты — это соединения, состоящие из диоксида титана. Титанат бария обладает пьезоэлектрическими свойствами, что позволяет использовать его в качестве преобразователя при взаимном преобразовании звука и электричества. Сложные эфиры титана образуются в результате реакции спиртов и тетрахлорида титана и используются для водонепроницаемости тканей.
Нитрид титана часто используется для покрытия режущих инструментов, например сверл. Он также находит применение в качестве декоративной отделки золотого цвета и в качестве барьерного металла при производстве полупроводников.
Хлорид титана (IV) (тетрахлорид титана, TiCl4, иногда называемый «щекоткой») представляет собой бесцветную слабокислую жидкость, которая используется в качестве промежуточного продукта при производстве оксида титана (IV) для красок. Он широко используется в органической химии в качестве кислоты Льюиса, например, при альдольной конденсации Мукаямы. Титан также образует низший хлорид, хлорид титана (III) (TiCl3), который используется в качестве восстановителя.
Дихлорид титаноцена является важным катализатором образования углерод-углеродной связи.Изопропоксид титана используется для эпоксидирования по Шарплесу. Другие соединения включают; Бромид титана (используется в металлургии, суперсплавах, высокотемпературной электропроводке и покрытиях) и карбид титана (содержится в высокотемпературных режущих инструментах и покрытиях).
Изотопы
Встречающийся в природе титан состоит из 5 стабильных изотопов; 46Ti, 47Ti, 48Ti, 49Ti и 50Ti, причем 48Ti является наиболее распространенным (естественное содержание 73,8%). Было охарактеризовано одиннадцать радиоизотопов, наиболее стабильным из которых является 44Ti с периодом полураспада 63 года, 45Ti с периодом полураспада 184 года.8 минут, 51Ti с периодом полураспада 5,76 минуты и 52Ti с периодом полураспада 1,7 минуты. Все оставшиеся радиоактивные изотопы имеют период полураспада менее 33 секунд, а у большинства из них период полураспада составляет менее половины секунды.
Изотопы титана имеют атомный вес от 39,99 а.е.м. (40Ti) до 57,966 а.е.м. (58Ti). Первичной модой распада перед наиболее распространенным стабильным изотопом 48Ti является захват электронов, а после первичной моды — бета-излучение. Первичные продукты распада до 48Ti — изотопы элемента 21 (скандий), а первичные продукты после — изотопы элемента 23 (ванадий).
Эта статья находится под лицензией GNU Free Documentation License. Он использует материал из статьи Википедии «Титан».
.

 При контакте с воздухом образуется соляная кислота. Разъедает многие металлы в присутствии воды.
При контакте с воздухом образуется соляная кислота. Разъедает многие металлы в присутствии воды. 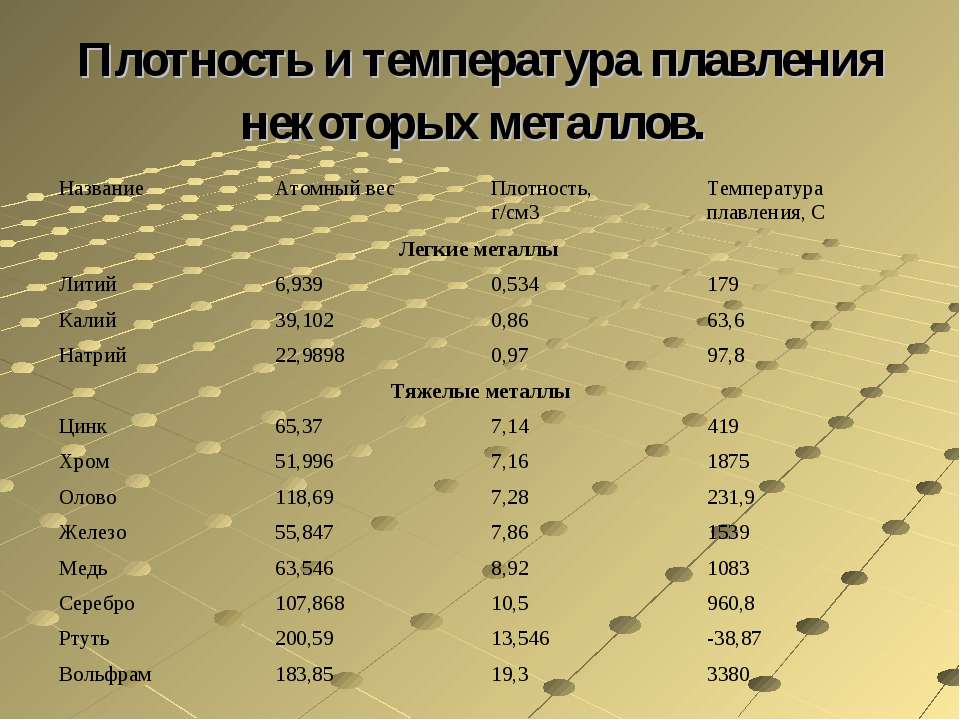 у.)
у.) Через 10 лет открытие титана состоялось в третий раз: французский учёный Л. Воклен обнаружил титан в анатазе и доказал, что рутил и анатаз — идентичные оксиды титана.
Через 10 лет открытие титана состоялось в третий раз: французский учёный Л. Воклен обнаружил титан в анатазе и доказал, что рутил и анатаз — идентичные оксиды титана.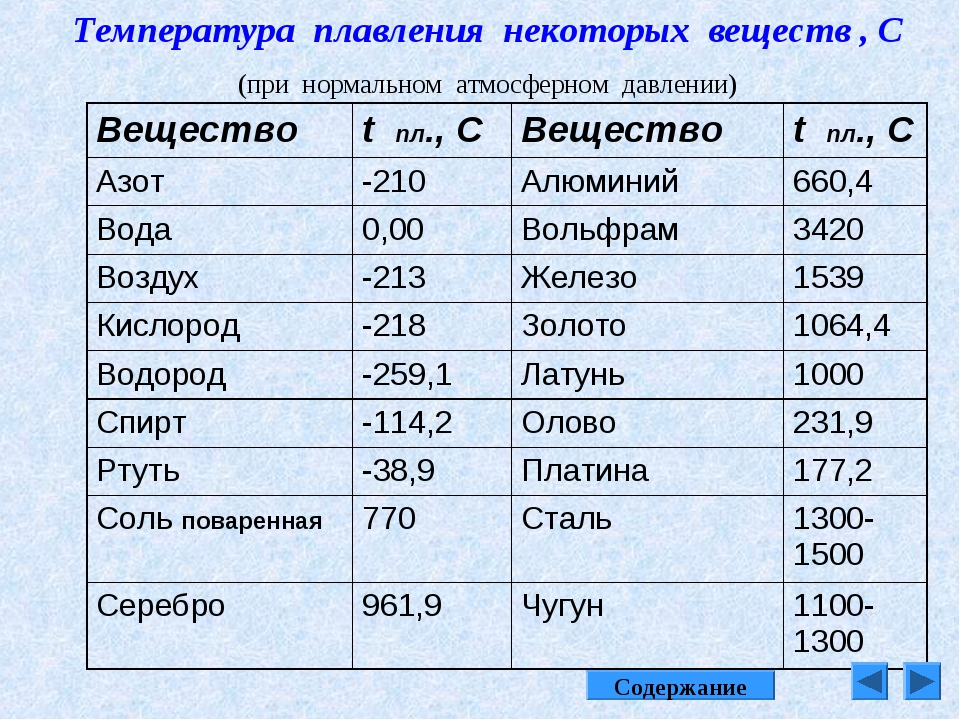 До 30 % TiO2 по весу накапливается в некоторых глинах. Минералы титана устойчивы к выветриванию и образуют крупные концентрации в россыпях. Известно более 100 минералов, содержащих титан. Важнейшие из них: рутил TiO2, ильменит FeTiO3, титаномагнетит FeTiO3 + Fe3O4, перовскит CaTiO3, титанит (сфен) CaTiSiO5. Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые[3].
До 30 % TiO2 по весу накапливается в некоторых глинах. Минералы титана устойчивы к выветриванию и образуют крупные концентрации в россыпях. Известно более 100 минералов, содержащих титан. Важнейшие из них: рутил TiO2, ильменит FeTiO3, титаномагнетит FeTiO3 + Fe3O4, перовскит CaTiO3, титанит (сфен) CaTiSiO5. Различают коренные руды титана — ильменит-титаномагнетитовые и россыпные — рутил-ильменит-цирконовые[3]. Запасы месторождения оцениваются в 2 миллиарда тонн руды со средним содержанием диоксида титана около 10 %[9].
Запасы месторождения оцениваются в 2 миллиарда тонн руды со средним содержанием диоксида титана около 10 %[9].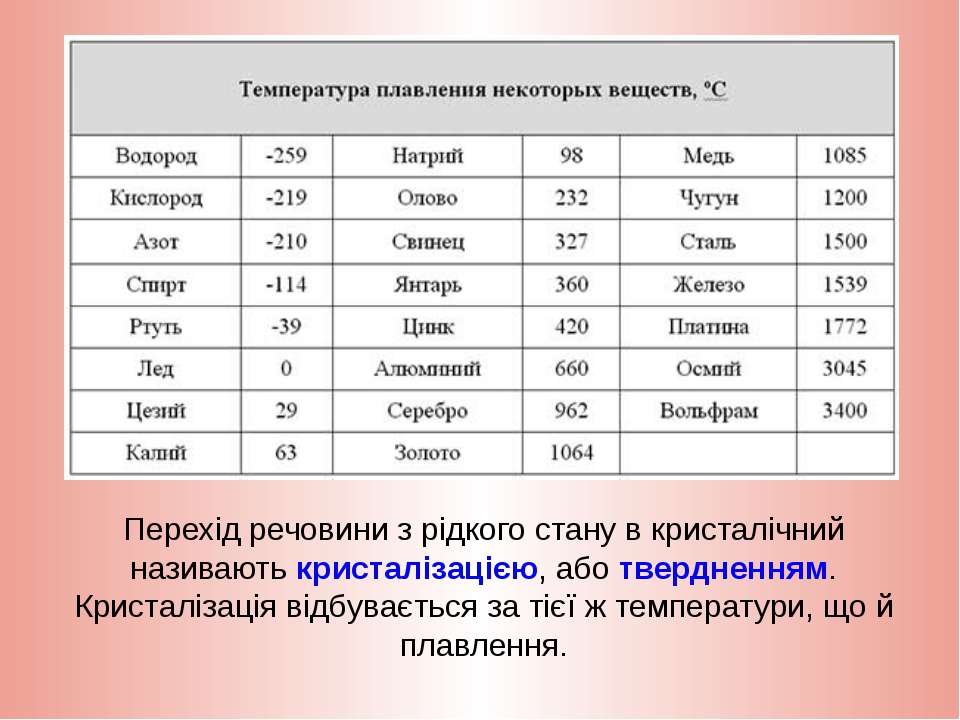 При пропускании через ванну тока температура быстро достигает ~1000—1100 °C, и расплав оксида кальция разлагается на аноде на кислород и металлический кальций:
При пропускании через ванну тока температура быстро достигает ~1000—1100 °C, и расплав оксида кальция разлагается на аноде на кислород и металлический кальций: Большинство металлов при растворении в титане стабилизируют β-фазу и снижают температуру перехода α↔β[3]. При давлении выше 9 ГПа и температуре выше 900 °C титан переходит в гексагональную фазу (ω-Ti)[11]. Плотность α-Ti и β-Ti соответственно равна 4,505 г/см³ (при 20 °C) и 4,32 г/см³ (при 900 °C)[3]. Атомная плотность α-титана 5,67⋅1022 ат/см³[12][13].
Большинство металлов при растворении в титане стабилизируют β-фазу и снижают температуру перехода α↔β[3]. При давлении выше 9 ГПа и температуре выше 900 °C титан переходит в гексагональную фазу (ω-Ti)[11]. Плотность α-Ti и β-Ti соответственно равна 4,505 г/см³ (при 20 °C) и 4,32 г/см³ (при 900 °C)[3]. Атомная плотность α-титана 5,67⋅1022 ат/см³[12][13]. Для технического титана твёрдость по Виккерсу составляет 790—800 МПа, модуль нормальной упругости 103 ГПа, модуль сдвига 39,2 ГПа[11]. У высокочистого предварительно отожжённого в вакууме титана предел текучести 140—170 МПа, относительное удлинение 55—70%, твёрдость по Бринеллю 716 МПа[3].
Для технического титана твёрдость по Виккерсу составляет 790—800 МПа, модуль нормальной упругости 103 ГПа, модуль сдвига 39,2 ГПа[11]. У высокочистого предварительно отожжённого в вакууме титана предел текучести 140—170 МПа, относительное удлинение 55—70%, твёрдость по Бринеллю 716 МПа[3].
 Легирующие элементы разделяют на три группы, в зависимости от их влияния на температуру полиморфного превращения: на бета-стабилизаторы, альфа-стабилизаторы и нейтральные упрочнители. Первые понижают температуру превращения, вторые повышают, третьи не влияют на неё, но приводят к растворному упрочнению матрицы. Примеры альфа-стабилизаторов: алюминий, кислород, углерод, азот. Бета-стабилизаторы: молибден, ванадий, железо, хром, никель. Нейтральные упрочнители: цирконий, олово, кремний. Бета-стабилизаторы, в свою очередь, делятся на бета-изоморфные и бета-эвтектоидообразующие.
Легирующие элементы разделяют на три группы, в зависимости от их влияния на температуру полиморфного превращения: на бета-стабилизаторы, альфа-стабилизаторы и нейтральные упрочнители. Первые понижают температуру превращения, вторые повышают, третьи не влияют на неё, но приводят к растворному упрочнению матрицы. Примеры альфа-стабилизаторов: алюминий, кислород, углерод, азот. Бета-стабилизаторы: молибден, ванадий, железо, хром, никель. Нейтральные упрочнители: цирконий, олово, кремний. Бета-стабилизаторы, в свою очередь, делятся на бета-изоморфные и бета-эвтектоидообразующие.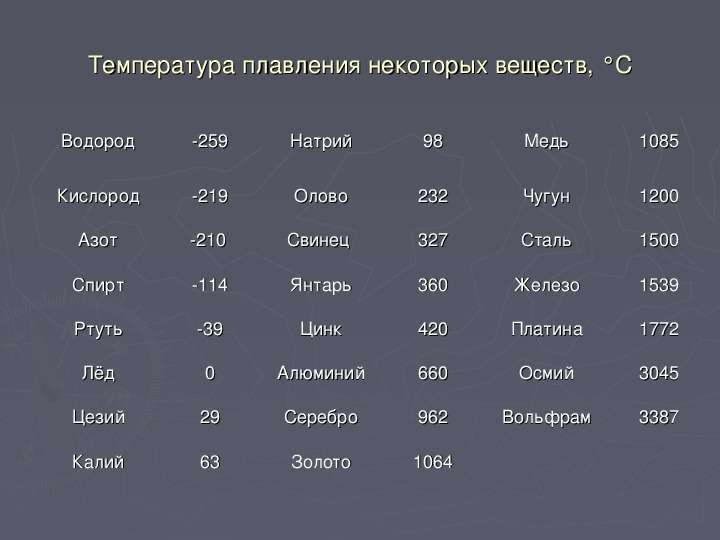
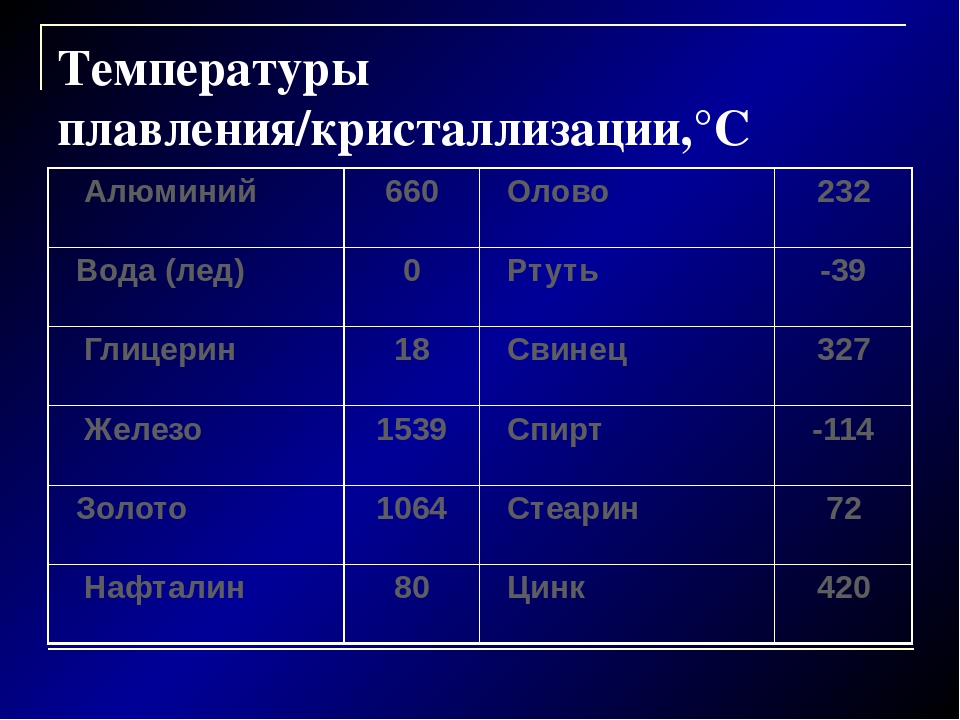 R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — 2828 p. — ISBN 1420090844.
R. Lide (Ed.). — 90th edition. — CRC Press; Taylor and Francis, 2009. — 2828 p. — ISBN 1420090844. Г. В. Самсонова. М.: Металлургия, 1976. 600 с.
Г. В. Самсонова. М.: Металлургия, 1976. 600 с. Ильменит представляет собой смесь оксидов железа и оксидов титана.
Ильменит представляет собой смесь оксидов железа и оксидов титана.
 Хотя эти изделия из титана немного дороже традиционных стальных или алюминиевых альтернатив, они могут быть значительно легче без ущерба для прочности. Однако некоторые утверждают, что тепловые свойства титановой посуды делают ее непригодной для серьезных кулинарных применений.
Хотя эти изделия из титана немного дороже традиционных стальных или алюминиевых альтернатив, они могут быть значительно легче без ущерба для прочности. Однако некоторые утверждают, что тепловые свойства титановой посуды делают ее непригодной для серьезных кулинарных применений.